Method Article
Farelerde Akciğer Adenokarsinomu Ksenogreft Modelinin Oluşturulması ve MAPK Yolağı ile XY Kaynatma Etkinliğinin Değerlendirilmesi
Bu Makalede
Özet
Bu çalışma, XY kaynatma işleminin MAPK yolağını düzenleyerek akciğer adenokarsinomuna karşı terapötik etkiler gösterdiğini göstermektedir.
Özet
Akciğer adenokarsinomu dünya çapında artmakta ve etkili tedavi yöntemlerinin araştırılmasına ve geliştirilmesine yol açmaktadır. Son yıllarda, geleneksel Çin tıbbının XiaoYi (XY) kaynatma gibi akciğer adenokarsinomu için terapötik potansiyeli giderek daha fazla kabul görmektedir. Geleneksel Çin tıbbının akciğer adenokarsinomunun tedavisinde etki mekanizması aydınlatılmaya devam etmektedir. Bu çalışmada, akciğer adenokarsinomu tedavisinde XY kaynatma işleminin terapötik etkilerini araştırmak için hayvan modelleri kullanılmıştır. Farelerde XY kaynatma işleminin kan giriş kimyasal bileşenleri, UHPLC-QE-MS kullanılarak hem pozitif hem de negatif iyon modlarında ayrıldı ve analiz edildi. Bulgular daha sonra tümör boyutunun azaldığını, patolojik değişikliklerin arttığını ve apoptozun arttığını gösteren in vivo deneylerle doğrulandı. Sonuç olarak, XY kaynatma uygulamasını takiben kana emilen on beş bileşen tanımlandı: Stachyose, Quercetin-3-O-beta-glukopiranosil-7-O-alfa-ramnopiranozid; İmparatorluk; Spinosin B; Peimine; Flavon tabanı + 3O, 2MeO, O-Hex; Pikropodofilotoksin; (2S,3R,4S,5S,6R)-2-[(2R,3R,4S,5S,6R)-4,5-dihidroksi-2 [[(3S,5R,8R,10R,12R,13R,14R,17S)-12-hidroksi-17-(2-hidroksi-6-metilhept-5-en-2-il) 4,4,8,10,14-pentametil-2,3,5,6,7,9,11,12,13,15,16,17-dodekahidro-1H siklopenta[a]fenantren-3-il]oksi]-6-(hidroksimetil)oksan-3-il]oksi-6-(hidroksimetil)oksan-3,4,5-triol; Trisin; Ginsenosit Rg1; (20R)-Ginsenosit Rh1; Jujuboside B; Aucubin; Ginsenosid Rg3; ve beta-Elemonik asit. Hayvan deneyleri, XY kaynatma işleminin tümör büyümesini inhibe ettiğini, patolojik değişiklikleri iyileştirdiğini ve doza bağlı bir şekilde tümör hücresi apoptozunu teşvik ettiğini gösterdi. İlgili mekanizmalar, MAPK yolağındaki p-JNK ve p-P38 protein ekspresyonunun yukarı regülasyonu ve MAPK yolağındaki p-ERK protein ekspresyonunun aşağı regülasyonu ile ilişkili olabilir. Sonuç olarak, XY kaynatma, MAPK yolunu düzenleme ve akciğer adenokarsinomuna karşı terapötik etkiler gösterme potansiyeline sahiptir.
Giriş
Akciğer kanseri insidansı dünya çapında artmaktadır. Tüm malignitelerin %18'ini oluşturur ve kansere bağlı ölümlerin önemli bir kısmından sorumludur 1,2. Küçük hücreli dışı akciğer kanseri (KHDAK), ana patolojik tip3 adenokarsinom olan yaygın bir akciğer kanseri türüdür. Sinsi semptomları nedeniyle, NSCLC sıklıkla ileri bir aşamada teşhis edilir ve yüksek mortalite oranına sahiptir 4,5. Evre IV KHDAK hastalarının beş yıllık sağkalım oranı sadece %5'tir6, cerrahi olarak rezeke edilebilir erken evre KHDAK bile beş yıllık sağkalım oranı sadece %50'dir7.
Günümüzde akciğer adenokarsinomunun tedavisi cerrahi, radyoterapi, kemoterapi, immünoterapi ve hedefe yönelik tedaviyi içermektedir. Ek olarak, akciğer adenokarsinomu için geleneksel Çin tıbbı (TCM) giderek daha fazla tanınmakta ve değer görmektedir8. TCM'nin uzun bir geçmişi vardır ve etkili terapötik sonuçları olan çeşitli onkolojik hastalıkların tedavisinde kullanılmaktadır 9,10. İnsan vücudunu bir bütün olarak kabul eder, terapötik prensip Qi'nin hareketini geri kazanmaya odaklanır (Qi, kan ve vücut sıvılarının dolaşımını teşvik eden, NSCLC hastalarında bağışıklığın artmasına ve inflamasyonun azalmasına katkıda bulunan hayati enerjiyi ifade eder) genel dengeyi yeniden sağlamak ve kanserin ilerlemesini engellemek için iç organlarda.
TCM sadece düşük toksisiteli, çoklu hedefli ve yüksek verimli11 onkolojik hastalıkları tedavi etmekle kalmaz, aynı zamanda radyoterapi ve kemoterapinin neden olduğu hasarın onarımını kolaylaştırır ve böylece sağkalımı uzatır12.
Sıvı kromatografisi-kütle spektrometresi (LC-MS) teknolojisi, karmaşık bileşik karışımlarındaki bileşenlerin ayrılmasını ve algılanmasını sağlamak için sıvı kromatografisini kütle spektrometresi ile entegre eder13. LC-MS, geleneksel Çin tıbbı (TCM) kaynatmalarında çeşitli kimyasal bileşenlerin ayrılmasına ve tanımlanmasına olanak tanıyan yüksek çözünürlük, yüksek hassasiyet ve yüksek özgüllük sunar. Oral uygulamadan14,15 sonra kan giriş aktif bileşenlerini ayıran ve tespit eden serum tıbbi kimyası ile birleştirildiğinde, LC-MS potansiyel ilaç etki mekanizmalarının tahmin edilmesini ve analiz edilmesini sağlar. Bu yaklaşım, TCM kaynatmalarının kimyasal bileşiminin ve farmakolojik bileşenlerinin anlaşılmasına yardımcı olur, farmakolojik etkileri ve klinik uygulamaları hakkında derinlemesine araştırmalar için gerekli verileri sağlar ve TCM araştırmasında oldukça uygulanabilir hale getirir16,17.
MAPK sinyal yolu, akciğer kanserinin oluşumunda, ilerlemesinde, metastazında ve invazyonunda çok önemli bir rol oynar ve Erk, p38 ve JNK önemli alt ailelerdir. TCM kaynatmalarının, MAPK yolu18'deki proteinlerin ekspresyonunu etkilediği gösterilmiştir. XiaoYi (XY) kaynatma, YiGuan kaynatma işleminden türetilmiştir ve Changchun Çin Tıbbı Üniversitesi'nin Birinci Bağlı Hastanesi'nde akciğer adenokarsinomunu tedavi etmek için kullanılır (Şekil 1), bu da kesin klinik etkinlik gösterir. Bununla birlikte, terapötik mekanizması belirsizliğini korumaktadır.
Bu çalışmada, akciğer adenokarsinomuna karşı XY kaynatma işleminin olası terapötik mekanizmasını aydınlatmak için Q-Exactive Orbitrap kütle spektrometresi (UHPLC-QE-MS) ile birleştirilmiş ultra yüksek performanslı sıvı kromatografisi kullanıldı ve etkileri in vivo çalışmalarla doğrulandı.
Protokol
Tüm hayvan prosedürleri, Changchun Geleneksel Çin Tıbbı Üniversitesi Hayvan Etik Komitesi (Etik No. 2024008) tarafından onaylanmıştır. Spesifik patojen içermeyen (SPF) koşullar altında yetiştirilen altı haftalık C57BL / 6 erkek fareler (20 ± 2 g), sabit sıcaklık ve nem ile kontrollü bir ortamda tipik fiziksel aktivite modelleri sergiledi. Yiyecek ve suya ad libitum erişimleri vardı ve 12 saatlik bir aydınlık / karanlık döngüsü altında tutuldular. Bu çalışmada kullanılan reaktiflerin ve ekipmanın ayrıntıları Malzeme Tablosunda verilmiştir.
1. XY kaynatma sulu ekstraktının hazırlanması
- Panax ginseng C.A. Mey (Renshen, 15 g), Chinemys reevesii (Gri) (Guiban, 30 g) ve Trionyx sinensis Wiegmann'ı (Biejia, 30 g) bir kaynatma kabına koyun. 1000 mL deiyonize su ekleyin ve oda sıcaklığında 30 dakika bekletin.
- Adım 1.1'deki üç otu 1 saat kaynatın. Aynı zamanda, Rehmannia glutinosa Libosch (Dihuang, 30 g), Trichosanthes kirilowii Maxim'i ıslatın. (Tianhuafen, 30 g), Coix lacryma-jobi L. var. mayuen (Roma.) Stapf (Yiyiren, 20 g), Paeonia lactiflora Pall. (Baishao, 30 g), Boswellia carterii Birdw. (Ruxiang, 7 g), Commiphora myrrha Engl. (Moyao, 7 g), Agrimonia pilosa Ledeb. (Xianhecao, 20 g), Alpinia oxyphylla Miq. (Yizhiren, 20 g), Ziziphus hünnap Değirmeni. spinosa (Bunge) (Suanzaören, 30 g), Melia toosendan Sieb. et Zucc. (Chuanlianzi, 5 g), Fritillaria thunbergii Miq. (Zhebeimu, 15 g), Anemarrhena asphodeloides Bge. (Zhimu, 10 g), Platycodon grandiflorum (Jacq.) (Jiegeng, 10 g), Polygala tenuifolia Willd. (Yuanzhi, 15 g) ve Phragmites communis Trin. (Lugen, 30 g) başka bir kapta 30 dakika. Suya batırdıktan sonra, 1.1 adımındaki kaynatma kabına aktarın.
- Adım 1.1 ve adım 1.2'deki 18 bitkinin tümünü 30 dakika kaynatın. Bitkisel sıvıyı dökün, 1000 mL deiyonize su ekleyin ve 30 dakika daha kaynatın. Üç porsiyon bitkisel sıvı elde etmek için bu kaynatma işlemini üç kez tekrarlayın, ardından birleştirin ve iyice karıştırın.
- Karıştırılmış bitkisel sıvıyı 400 gözenekli bir bezden süzün. Süzüntüyü düşük basınç altında konsantre edin, ardından konsantre bitkisel sıvıyı daha sonraki işlemler için soğutma ekipmanına aktarın.
- Konsantre bitkisel sıvıyı bir liyofilizasyon tepsisine dökün ve bir vakumlu liyofilizatörün ön dondurma odasına yerleştirin. Ön dondurma tamamlandıktan sonra, suyu çıkarmak için tepsiyi süblimasyon kurutma odasına aktarın.
- Yüksek sıcaklıkta kalan nemi temizleyin. İnce liyofilize XY kaynatma tozu elde etmek için dondurularak kurutulmuş bitki ekstraktını bir pulverizatör kullanarak toz haline getirin (Şekil 2).
2. İlaç içeren serum hazırlama
- Altı haftalık C57BL / 6 erkek fareyi (20 ± 2 g) rastgele XiaoYi (XY) grubuna veya kontrol grubuna atayın.
NOT: Fare dozu, insandan fareye dönüşüm faktörü kullanılarak hesaplanmıştır:
Fareler için eşdeğer deney dozu (g / kg) = {İnsan dozu (g / kg) / Vücut ağırlığı (70 kg)} x 9.1
Bu hesaplamaya dayanarak, fareler için dozaj 2.6 g / kg olarak belirlendi. - 0.9152 g liyofilize XY kaynatma tozunu tartın ve ilaç çözeltisini hazırlamak için 3.2 mL damıtılmış su içinde çözün.
NOT: Fareler oral uygulamadan önce 12 saat aç bırakıldı. - XY kaynatma işlemini XY grubundaki farelere gavaj yoluyla uygularken, kontrol grubunu eşdeğer hacimde deiyonize su ile uygulayın.
- Oral uygulamadan 2 saat sonra, fareleri pentobarbital sodyum ile uyuşturun (kurumsal olarak onaylanmış protokolleri izleyerek). Kan örneklerini toplamak için cımbız kullanarak gözbebeklerini enüklee edin, ardından fareleri CO2 boğulması ve ardından etik yönergeleri izleyerek servikal çıkık yoluyla ötenazi yapın19.
- Kan örneklerinin oda sıcaklığında 90 dakika stabilize olmasına izin verin. Süpernatanı toplamak için 3450 x g'da (4 ° C) 15 dakika santrifüjleyin.
3. UHPLC-QE-MS analizi
- 500 μL ekstraksiyon çözeltisine (metanol: su = 4: 1) 100 mg XY kaynatma liyofilize toz ekleyin. İyice karıştırın, sonikat yapın ve 1 saat boyunca buzlu su banyosunda inkübe edin.
- Karışımı 1 saat -40 °C'de tutun, ardından 13.800 x g'da (4 °C) 15 dakika santrifüjleyin. Süpernatanı 0,22 μm'lik bir filtre membranından süzün, ardından kalite kontrol (QC) numuneleri oluşturmak için her süpernatanın 100 μL'sini birleştirin.
- Plazma örnekleri çözüldükten sonra, kontrol grubu plazma örneğinden 400 μL ve XY grubu plazma örneklerinden 400 μL alın. Her numuneye 40 μL hidroklorik asit (2 mol/L) ekleyin. 1 dakika vorteksleyin ve karışımı 4 °C'de 15 dakika bekletin. Bu adımı dört kez tekrarlayın.
- 1.6 mL asetonitril ekleyin ve 5 dakika boyunca girdap yapın. 4 ° C'de 5 dakika boyunca 13.800 x g'da santrifüjleyin. 1.800 μL süpernatanı nitrojen kurutmaya tabi tutun.
- Kurutulmuş numuneleri, 5 dakika boyunca girdaplama yoluyla 10 μg/mL iç standart içeren 150 μL% 80 metanol içinde sulandırın. 4 ° C'de 5 dakika boyunca 13.800 × g'da santrifüjleyin, ardından 120 μL süpernatanı LC-MS analizi için taze bir cam şişeye aktarın (Şekil 3).
4. Hücre kültürü ve hayvan hazırlama
- %10 fetal sığır serumu ve %1 penisilin/streptomisin ile desteklenmiş Dulbecco'nun Modifiye Eagle Medium'unu (DMEM) içeren bir kültür kabında 1 mL Lewis akciğer karsinomu hücresi tohumlayın. Hücreleri kontrollü koşullar altında 37 ° C'de% 5 CO2 ile inkübe edin.
- Hücreler% 80 birleşmeye ulaştığında,% 0.25 tripsin kullanarak onları geçirin. Hücre durumu stabilize olana kadar pas vermeye devam edin, ardından hücre konsantrasyonunu 3 x 106 hücre / mL'ye ayarlayın.
- Akciğer adenokarsinomu modelini oluşturmak için hazırlanan hücre süspansiyonunun 0.1 mL'sini erkek C57BL / 6 farelerinin sağ aksillasına deri altından enjekte edin.
NOT: Tümör dokusu, aşılamadan 5 gün sonra farelerin aksillasında palpe edilebilir. - 5 gün sonra, fareleri rastgele beş gruba ayırın (grup başına n = 6): Model grubu (M) - Tedavi yok; XY kaynatma düşük doz grubu (XY-L) - 1.3 g / kg; XY kaynatma orta doz grubu (XY-Z) - 2.6 g / kg; XY kaynatma yüksek doz grubu (XY-H) - 5.2 g / kg; Sisplatin grubu (DDP) - Sisplatin20 ile tedavi edilir.
- XY kaynatma tozunu karşılık gelen dozda 200 μL damıtılmış su içinde çözün ve gavaj yoluyla uygulayın. M ve DDP grupları, gavaj yoluyla eşit hacimde damıtılmış su alır.
- Sisplatini DDP grubuna her 3 günde bir intraperitoneal enjeksiyon (3 mg / kg) yoluyla uygulayın. Aynı hacimde fizyolojik salini diğer gruplara enjekte edin.
5. Tümör dokusunun patolojik analizi
- 21 gün sonra, CO2 asfiksiasyonu ve ardından servikal çıkık (etik kurallara izleyerek) kullanarak tüm farelere ötenazi yapın ve tümör dokusunuçıkarın 21. Tümör hacmini ve ağırlığını ölçün (Şekil 4).
- Eksize edilen tümör dokularını 24 saat boyunca% 4 paraformaldehit içinde sabitleyin). Dereceli etanol çözeltileri kullanarak dokuyu kurutun.
- Susuz kalmış doku bloklarını ksilen kullanarak temizleyin, ardından erimiş parafin mumuna gömün. Balmumunun bir parafin bloğu halinde katılaşmasına izin verin. Doku bloğunu bir mikrotom kullanarak 5 μm kalınlığında dilimler halinde bölümlere ayırın.
- Doku bölümlerini ksilen içinde mumdan arındırın, ardından kademeli etanol çözeltilerinde rehidrasyon yapın. Bölümleri hematoksilen ile 5 dakika boyayın, ardından deiyonize su ile durulayın.
- Bölümleri 1 dakika boyunca% 0,5 eozin çözeltisi ile boyayın. Lekeli bölümleri optik mikroskop altında gözlemleyin ve analiz için görüntüleri yakalayın.
6. Tümör dokusunun immünohistokimyasal analizi
- Adım 5.2-5.4'te açıklanan prosedürleri izleyerek mum alma ve rehidrasyon gerçekleştirin.
- Bölümleri endojen bir peroksidaz blokerinde oda sıcaklığında 15 dakika inkübe edin. Bölümleri keçi serumu ile inkübe ederek spesifik olmayan bağlanmayı engelleyin.
- Birincil antikorları uygulayın: Ki-67 (1:600) ve Kaspaz-3 (1:100). Bölümleri gece boyunca 4 °C'de inkübe edin. PBS tamponu ile yıkayın), ardından genel amaçlı bir ikincil antikor (1:500) uygulayın ve 37 ° C'de 30 dakika inkübe edin.
- DAB çözeltisi ekleyerek renk reaksiyonunu geliştirin. Bölümleri hematoksilen çözeltisi ile lekeleyin.
- Lekeli bölümlerin dehidrasyonunu, temizlenmesini ve sızdırmazlığını gerçekleştirin. Optik mikroskop altında protein ekspresyonunu gözlemleyin ve analiz için görüntüler yakalayın.
7. Batı lekesi analizi
- Bir doku parçalayıcı kullanarak tümör dokularını homojenize edin. Toplam proteini ekstrakte edin ve bir bikinkoninik asit (BCA) tahlil kiti kullanarak konsantrasyonunu belirleyin (bkz. Malzeme Tablosu).
- Protein miktar tayinini gerçekleştirin, ardından SDS-PAGE elektroforezi ve bir zar üzerine protein transferi yapın.
- Membranı gece boyunca 4 ° C'de birincil antikorlarla inkübe edin: P38 (1:2000), p-P38 (1:1000), ERK (1:20000), p-ERK (1:500), JNK (1:2000), p-JNK (1:5000), β-aktin (1:200) (bkz.
- Ertesi gün, zarı yaban turpu peroksidaz (HRP) konjuge ikincil antikoru ile oda sıcaklığında 1.5 saat inkübe edin. Gelişmiş bir kemilüminesans (ECL) sistemi kullanarak protein bantlarını tespit edin.
NOT: Protein bant yoğunlukları ImageJ yazılımı kullanılarak ölçülmüştür.
Sonuçlar
Kontrol grubundan ve XY grubundan XY toz çözeltisi ve serum örnekleri UHPLC-QE-MS kullanılarak analiz edildi ve iyi ayrılmış pikler ortaya çıktı. Pozitif ve negatif iyon modları için toplam iyonizasyon diyagramları Şekil 3'te gösterilmiştir. XY kaynatma işleminin bileşimi, tutma süresi, edinme modu ve kütle spektrumu fragmanlarına dayalı olarak tanımlandı. Boş ve XY kaynatma oral uygulama gruplarının serumu XY toz çözeltisinin bileşenleri ile karşılaştırılarak on beş kan giriş bileşeni tanımlandı (Tablo 1).
Tümör hacmi çizgi grafiği, XY kaynatma ile 21 günlük gavajdan sonra, farelerde tümör hacminin M grubuna göre azaldığını ve doza bağlı bir etki gösterdiğini göstermektedir (Şekil 4). Tümör histopatolojisi H&E boyaması kullanılarak izlendi (Şekil 5). M grubunda, tümör hücreleri yoğun bir şekilde düzenlenmiş ve bol miktarda patolojik mitoz ile aktif proliferasyon sergilemiştir. XY kaynatma dozu arttıkça, tümör hücrelerinin düzenlenmesi yavaş yavaş seyrekleşti ve hücreler arası boşluk arttı. Tümör dokularında çeşitli derecelerde nekroz gözlendi ve patolojik mitoz nadirdi21.
XY kaynatma işleminin farelerde tümör dokularının proliferasyonu ve apoptozu üzerindeki etkilerini doğrulamak için immünohistokimya (IHC) deneyleri yapılmıştır. Ki-67 ve Kaspaz 3 antikorları ile boyandıktan sonra, tümör dokusu kesitlerinde dağınık kahverengimsi-sarı partiküller gözlendi. M grubu ile karşılaştırıldığında, XY ve DDP gruplarının tümör dokularındaki Ki-67 düzeyleri sırayla azalırken, Kaspaz 3 düzeyleri arttı (Şekil 6).
XY kaynatma işleminin MAPK yolu yoluyla akciğer adenokarsinomu üzerinde terapötik etkiler gösterip göstermediğini belirlemek için, farelerden alınan tümör dokuları üzerinde Western blot analizi yapıldı. Şekil 7'de gösterildiği gibi, XY kaynatma ile tedavi, p-ERK ekspresyonunda bir azalmaya yol açmıştır ve XY-H grubu, M grubuna kıyasla önemli bir fark göstermiştir (p < 0.001). p-JNK ve p-P38 düzeyleri XY-H grubunda M grubuna göre artmış, XY-H grubunda (p < 0.01) ve DDP grubunda (p < 0.05) M grubuna göre istatistiksel olarak anlamlı farklılıklar gözlenmiştir. Ek olarak, DDP ve XY-H grupları arasındaki fark istatistiksel olarak anlamlıydı.

Şekil 1: XY kaynatma bileşenleri. Bu şekil, XY kaynatmada bulunan bireysel ilaçları göstermektedir. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
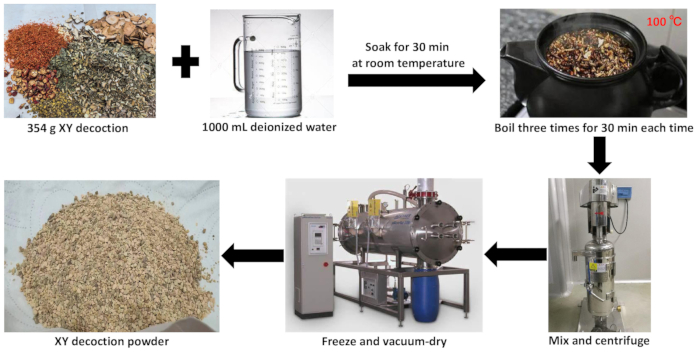
Şekil 2: XY kaynatma sulu ekstraktının hazırlanması. Bu şekil, XY kaynatma işleminin sulu ekstraktının hazırlanma sürecini göstermektedir. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
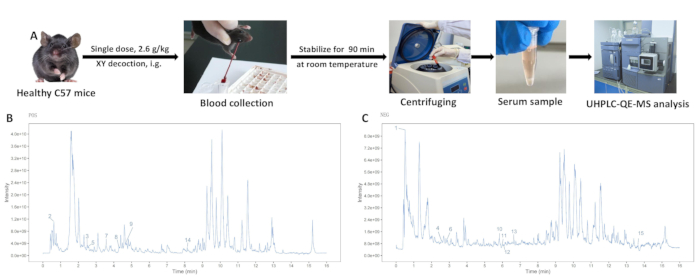
Şekil 3: XY kaynatma sulu ekstraktının analizi. (A) İlaç içeren serumun ekstraksiyon işlemi. (B) Pozitif iyon modunda kütle spektrometresi analizi. (C) Negatif iyon modunda kütle spektrometresi analizi. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 4: XY kaynatma işleminin fare tümör hacmi ve morfolojisi üzerindeki etkileri. (A) Hücre kültürü, tümör implantasyonu ve örnekleme prosedürleri. (B) Zaman içindeki tümör hacmini gösteren çizgi grafiği. (C) 21 günlük gavaj tedavisinden sonra tümör morfolojisi. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
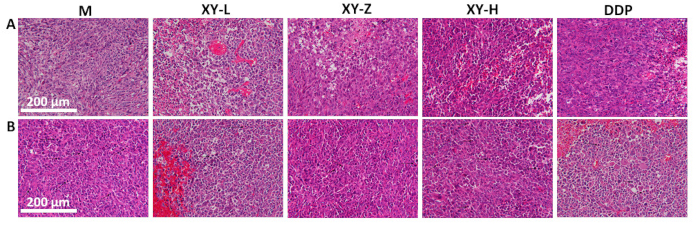
Şekil 5: Fare tümör dokularının histolojik analizi. (A) Tümör dokusu düzenlemesi, doza bağlı bir şekilde nekroz belirtileri ile artan dozlarda XY kaynatma ile daha seyrek hale gelir. (B) Tümör dokularında patolojik mitoz, artan dozlarda XY kaynatma ile patolojik mitozda bir azalma gösterir. Ölçek çubukları: 200 μm. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 6: Ki-67 ve Kaspaz-3 ekspresyon seviyeleri. (A) Ki-67 ifade seviyeleri. (B) Kaspaz-3 ekspresyon seviyeleri. Ölçek çubukları: 400 μm. (C) Ki-67 pozitif alanların miktar tayini, artan XY kaynatma dozları ile bir azalma gösteriyor. (D) Kaspaz-3 pozitif alanların miktarının belirlenmesi, artan XY kaynatma dozları ile bir artış gösterir. p < 0.001, ****p < 0.0001; ns, önemli değil. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 7: MAPK yolağındaki protein ekspresyon seviyeleri. (A) Protein ekspresyonunun Western blot analizi. (B) ERK ifade seviyeleri. (C) p-ERK ifade seviyeleri. (D) JNK ifade seviyeleri. (E) p-JNK ifade seviyeleri. (F) P38 ekspresyon seviyeleri. (G) p-P38 ekspresyon seviyeleri. XY kaynatma, p-JNK ve p-P38 proteinlerinin ekspresyonunu yukarı regüle ederken, p-ERK ekspresyonunu aşağı regüle etti. *p < 0.05, **p < 0.01, ***p < 0.001. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
| HAYIR. | Tanımlanan bileşikler | Formül | M/Z | RT (dk) | Kütle hatası (ppm) | Ekler | Kaynak | ||
| 1 | Stachyose (Stachyose) | C24H42O21 | 665.21 | 0.49 | 1.2 | [M-H]- | A | ||
| 2 | Kuersetin-3-O-beta-glukopiranosil-7-O-alfa-ramnopiranosid | C4H9HAYIR2 | 609.14 | 0.61 | 7.16 | [E+Y]+ | A, C | ||
| 3 | Emperyalizm | C27H43HAYIR3 | 430.33 | 2.5 | 0.13 | [E+Y]+ | B | ||
| 4 | Spinosin B | C38H40O18 | 783.22 | 2.55 | 0.47 | [M-H]- | F | ||
| 5 | Peimine | C27H45HAYIR3 | 432.35 | 2.62 | 1.19 | [E+Y]+ | B | ||
| 6 | Flavon tabanı + 3O, 2MeO, O-Hex | C23H24O12 | 491.12 | 2.86 | 0.27 | [M-H]- | G | ||
| 7 | Pikropodofilotoksin | C22H22O8 | 415.14 | 3.54 | 2.25 | [E+Y]+ | B, E | ||
| 8 | (2S,3R,4S,5S,6R)-2-[(2R,3R,4S,5S,6R)-4,5-dihidroksi-2-[[(3S,5R,8R,10R,12R,13R,14R,17S)-12-hidroksi-17-(2-hidroksi-6-metilhept-5-en-2-il)-4,4,8,10,14-pentametil-2,3,5,6,7,9,11,12,13,15,16,17-dodekahidro-1H-siklopenta[a]fenantren-3-il]oksi]-6-(hidroksimetil)oksan-3-il]oksi-6-(hidroksimetil)oksan-3,4,5-triol | C42H72O13 | 785.5 | 4.26 | 8.49 | [E+Y]+ | D | ||
| 9 | Tricin (Tricin) | C17H14O7 | 331.08 | 4.67 | 0.85 | [E+Y]+ | G | ||
| 10 | Ginsenosit Rg1 | C42H72O14 | 845.49 | 5.83 | 2.16 | [M+FA]- | D | ||
| 11 | (20R)-Ginsenosit Rh1 | C36H62O9 | 683.44 | 5.98 | 1.35 | [M+FA]- | D | ||
| 12 | Jujuboside B | C52H84O21 | 1089.55 | 6.11 | 1.3 | [M+FA]- | F | ||
| 13 | Aucubin Belediyesi | C15H22O9 | 391.12 | 6.71 | 1.11 | [M+FA]- | A | ||
| 14 | Ginsenosit Rg3 | C42H72O13 | 807.48 | 8.1 | 5.3 | [M+NA]+ | D | ||
| 15 | beta-Elemonik asit | C30H46O3 | 453.34 | 13.74 | 0.42 | [M-H]- | E | ||
Tablo 1: XY kaynatma uygulamasını takiben kana emilen bileşenler. Tablo, XY kaynatma işleminden sonra kanda tespit edilen aktif bileşenleri listeler: A: Rehmannia glutinosa Libosch (Dihuang), B: Fritillaria thunbergii Miq. (Zhebeimu), C: Trichosanthes kirilowii Maxim. (Tianhuafen), D: Panax ginseng C.A. Mey (Renshen), E: Boswellia carterii Birdw. (Ruxiang), F: Ziziphus hünnap Değirmeni. spinosa (Bunge) (Suanzaoren), G: Phragmites communis Trin. (Lugen).
Tartışmalar
Kanser insidansı her yıl artmakta ve önemli klinik ve araştırma ilgisi çekmektedir22,23. Son çalışmalar, geleneksel Çin tıbbının (TCM) akciğer kanseri tedavisinde etkinliğini göstermiştir 24,25,26. Örneğin, Maimendong kaynatma işleminin NK hücrelerinin sayısını ve aktivitesini arttırdığı ve böylece akciğer kanseri metastazını inhibe ettiği gösterilmiştir27. Benzer şekilde, Mahuang Fuzi Xixin kaynatma, çoklu sinyal yollarını28 etkileyerek akciğer kanseri üzerinde terapötik etkiler elde etmiştir. Bu çalışma, XY kaynatma işleminin akciğer adenokarsinomu üzerinde terapötik etkiler gösterdiği olası mekanizmaları tahmin etmek için LC-MS analizi ve in vivo deneyler kullanmaktadır.
LC-MS analizinde 15 kan giriş bileşeni tanımlanmıştır. Bunlar arasında trisin ve pikrodofiloksinin ilaç direncini inhibe ettiği ve p-PRKCA, SPHK1, SPHK2 ve EGFR ekspresyon seviyelerini azalttığı, böylece akciğer kanseri hücre aktivitesini baskıladığı gösterilmiştir29,30. Panax ginseng CA Meyer'in bileşenleri olan Ginsenoside Rg1 ve Ginsenoside Rg3, hücre mitozunu bloke edebilir, mTOR yol sinyalini inhibe edebilir, anti-anjiyojenik etkiler gösterebilir, bağışıklık fonksiyonunu artırabilir ve nihayetinde ilaç direncini azaltırken tümör büyümesini ve metastazı inhibe edebilir 31,32,33,34. Stachyose, pro-apoptotik proteinlerin ekspresyonunu modüle ederek bağırsak kanseri hücrelerinde apoptozu indükleyebilir35. Anti-inflamatuar ve anti-proliferatif özelliklere sahip bir alkaloid olan imperialine, erken evre bir antitümör ajan olarak potansiyele sahiptir36. Peimin, apoptozu indükleyerek hücre döngüsünü durdurabilir, endoplazmik retikulum stresi yoluyla hücre göçünü engelleyebilir ve meme ve mide kanseri hücrelerinin büyümesini baskılamak için NF-κB yolu ile ilgili protein ekspresyonunu düzenleyebilir37,38. Aucubin ve Jujuboside B'nin anjiyogenezi inhibe ederken tümör hücrelerinde otofaji ve apoptozu teşvik ettiği ve böylece antitümör etkileri gösterdiği bildirilmiştir 39,40,41.
MAPK yolu, hücre aktivasyonu, proliferasyon, otofaji ve apoptoz dahil olmak üzere çeşitli biyolojik süreçler için gereklidir. Ginsenoside Rg1, Ginsenoside Rg3, Peimin ve Jujuboside B gibi XY kaynatma işleminin kan giriş bileşenlerinde tespit edilen çeşitli bileşikler, MAPK yolu 42,43,44,45 yoluyla antitümör etkiler gösterebilir. MAPK yolu, ERK, JNK ve P38 sinyal kaskadlarını içerir ve MAP3K-MAP2K-MAPK 46,47'nin protein kaskad aktivasyonu yoluyla fizyolojik süreçlerin düzenlenmesindeki rolü nedeniyle kanser araştırmalarında geniş çapta incelenmiştir.
ERK yolunun aktivasyonu, transkripsiyonel ve translasyonel seviyelerde pro-apoptotik ve anti-apoptotik proteinlerin aktivitesini ve ekspresyonunu düzenleyerek hücre proliferasyonunu uyarır ve apoptozu inhibe eder48,49. ERK yolunu hedef alan protein inhibitörleri kapsamlı bir şekilde incelenmiştir ve kanser tedavisinde kullanılmaktadır50,51,52. Geleneksel Çin tıbbı (TCM) monomerleri ve formülasyonlarının da ERK yolunu modüle ederek antitümör etkiler gösterdiği gösterilmiştir. Örneğin, QYHJ formülü, p-P38 ve p-ERK1 / 253'ün ekspresyonunu düzenleyerek pankreas duktal adenokarsinom hücrelerinin proliferasyonunu inhibe eder ve apoptozunu teşvik eder. Ferulik asit türevleri proliferasyonu baskılar, hücre döngüsünü durdurur ve A549 insan akciğer kanseri hücre hattı54'te apoptozu indükler.
JNK/P38 yolu, fosforilasyon yoluyla farklı aşağı akış efektör proteinlerini düzenleyerek farklı roller oynar, böylece hücre döngüsünü, hücre proliferasyonunu ve apoptozu etkiler55,56. Çalışmalar, triptolidin p-P38 ve p-JNK ekspresyonunu modüle ettiğini ve A549 hücrelerinin proliferasyonunu inhibe ederek antitümör etkiler gösterdiğini göstermiştir57. Ek olarak, baicalein, p-P38 ve p-JNK ekspresyonunu58 etkileyerek HeLa hücrelerinde apoptozu indükler. İn vivo ve in vitro çalışmalar, Aidi enjeksiyonunun HepG2 hücrelerinde ve hepatoselüler karsinom fare modellerinde p-JNK ve p-P38 ekspresyonunu etkilediğini ve böylece tümör proliferasyonunu inhibe ettiğini göstermiştir59.
Ki-67 ve Kaspaz 3, tümör proliferasyonu ve apoptozun temel göstergeleridir. Ki-67, hücre proliferasyonu sırasında yüksek oranda eksprese edilen ve hareketsiz hücrelerde (G0 fazı) bulunmayan bir nükleer proteindir60. Tümör gelişimi hücre proliferasyonu ile yakından bağlantılı olduğundan, Ki-67 ve tümör oluşumu arasındaki korelasyon üzerine yapılan araştırmalar önemli bir ilgi görmüştür. Ki-67 ekspresyonu, tümör malignitesi, agresifliği ve prognozuile pozitif ilişkilidir 61,62, bu da onu kanser proliferasyonu için yaygın olarak kullanılan bir biyobelirteç haline getirir63. Gastrointestinal, akciğer, meme ve rahim ağzı kanserlerinin patogenezi ve prognozu hakkında kapsamlı olarak çalışılmıştır 64,65,66,67.
Kaspaz ailesi, apoptoz ve iltihabı düzenleyen proteolitik enzimlerden oluşur. Esas olarak sitoplazmada bulunan kaspaz 3, apoptozun önemli bir efektörüdür. Hücre iskeleti proteinlerini parçalayarak, apoptozu inhibe edici proteinleri inaktive ederek ve DNA onarım enzimleriniparçalayarak hücre ölümünü kolaylaştırır 68,69,70. Kaspaz 3 ekspresyonundaki değişiklikler, tümör hücresinin kemoterapiye duyarlılığını etkileyebilir, böylece istilayı, metastazı ve çeşitli kanserlerin ilerlemesini etkileyebilir 71,72,73,74.
Bu çalışma, XY kaynatmanın, LLC tümör taşıyan farelerde doza bağlı bir şekilde tümör proliferasyonunu inhibe ettiğini göstermiştir. XY ve DDP tedavi gruplarından tümör dokularının patolojik analizi, azalmış patolojik mitoz ile birlikte M grubuna kıyasla daha gevşek hücre düzenlemeleri ortaya çıkardı. Ek olarak, tedavi gruplarının tümör dokularında nekroz ve kanama gözlendi. İmmünohistokimya (IHC) sonuçları, XY kaynağının tümör hücresi proliferasyonunu inhibe ettiğini ve doza bağlı bir şekilde apoptozu teşvik ettiğini doğruladı. Tümör dokularının Western blot analizi, MAPK yolağındaki anahtar proteinlerin ekspresyon seviyelerinde önemli değişiklikler olduğunu gösterdi. Genel olarak, patolojik ve IHC bulguları, XY kaynatmanın, MAPK sinyal yolundaki proteinlerin ekspresyonunu modüle ederek akciğer adenokarsinomuna karşı terapötik etkiler gösterdiğini göstermektedir.
Açıklamalar
Yazarların ifşa edecek hiçbir şeyi yok.
Teşekkürler
Bu çalışma, Jilin Eyaleti Bilim ve Teknoloji Geliştirme Planı Maddesi (YDZJ202301ZYTS459) tarafından desteklenmiştir.
Malzemeler
| Name | Company | Catalog Number | Comments |
| Acetonitrile | CNW Technologies | 5/8/1975 | |
| 2-Chloro-L phenylalanine | Shanghai Hengbo Biotechnology Co., Ltd. | 103616-89-3 | |
| Ammonium Hydroxide Solution | China National Pharmaceutical Group Chemical Reagent Co., Ltd. | #2028 | |
| Antibody-β-actin | Abcam | ab8228 | |
| Anti-Erk1 (pT202/pY204) + Erk2 (pT185/pY187) Antibody | Abcam | ab4819 | |
| Anti-ERK1/ERK2 Antibody | Abcam | ab184699 | |
| Anti-JNK1 (pY185) + JNK2 (pY185) + JNK3 (pY223) Antibody | Abcam | ab76572 | |
| Anti-JNK1/JNK2/JNK3 Antibody | Abcam | ab208035 | |
| Anti-Ki67 Antibody | Cell Signaling Technology | GB121141 | |
| Anti-p38 (phospho T180) Antibody | Abcam | ab178867 | |
| Anti-p38 alpha/MAPK14 Antibody | Abcam | ab170099 | |
| BCA protein concentration assay kit | Boster Biological Technology | 17E17B46 | |
| Bovine Serum Albumin (BSA) | DAKO | BIOFROXX | |
| Broad-spectrum phosphatase inhibitor (100x) | Boster Biological Technology | AR1183 | |
| C57bl/6 mice | Liaoning Changsheng Biotechnology Co., Ltd. | SCXK2021-0006 | |
| Chromatographic column | Waters | ACQUITY UPLC BEH C18 1.7 μm2.1*100 mm | |
| Cisplatin | China National Pharmaceutical Group Chemical Reagent Co., Ltd. | 232120 | |
| Citrate (pH 6.0) Antigen Retrieval Solution | Wuhan Baiqiandu Biotechnology Co., Ltd. | B2010 | |
| Cover Slip | Jiangsu Shitai Laboratory Equipment Co., Ltd. | 10212432C | |
| Cryogenic Stage | Wuhan Junjie Electronics Co., Ltd. | JB-L5 | |
| DAB Chromogenic Kit | Jiangsu Shitai Laboratory Equipment Co., Ltd. | 2005289 | |
| Decolorization shaker | Beijing Liu Yi Instrument Factory | WD-9405A | |
| Dehydrator | Wuhan Junjie Electronics Co., Ltd. | JJ-12J | |
| Drying Oven | Shanghai Huitai Instrument Manufacturing Co., Ltd. | DHG-9140A | |
| Dulbecco's modified eagle medium | Gibco | 8121587 | |
| EDTA (pH 8.0) Antigen Retrieval Solution | Wuhan Baiqiandu Biotechnology Co., Ltd. | B2001 | |
| EDTA (pH 9.0) Antigen Retrieval Solution | Wuhan Baiqiandu Biotechnology Co., Ltd. | B2002 | |
| Electrophoresis buffer | NCM Biotech | 20230801 | |
| Embedding machine | Wuhan Junjie Electronics Co., Ltd. | JB-P5 | |
| Eosin | China National Pharmaceutical Group Chemical Reagent Co., Ltd. | 212954 | |
| Ethanol | China National Pharmaceutical Group Chemical Reagent Co., Ltd. | 493511 | |
| Fetal bovine serum | Gibco | 2166090RP | |
| Formic acid | SIGMA | 64-18-6 | |
| GraphPad Prism software | GraphPad software, LLC | Version 9.0.0 | |
| Hematoxylin | China National Pharmaceutical Group Chemical Reagent Co., Ltd. | H3136 | |
| High performance liquid chromatography | Agilent | 1260 Infinity II Prime | |
| High speed refrigerated centrifuge | Thermo Fisher Scientific | Legend Micro 17R | |
| High-Resolution Mass Spectrometry | Thermo Fisher Scientific | Q Exactive Focus | |
| HRP-conjugated Goat Anti-Mouse | SeraCare | 5220-0341 | |
| HRP-conjugated Goat Anti-Rabbit | SeraCare | 5220-0336 | |
| HRP-conjugated Goat Anti-Rabbit/Mouse Universal Secondary Antibody | DAKO | K5007 | |
| HRP-conjugated Goat Anti-Rat | SeraCare | 5220-0364 | |
| HRP-conjugated Rabbit Anti-Goat | SeraCare | 5220-0362 | |
| Hydrochloric acid | China National Pharmaceutical Group Chemical Reagent Co., Ltd. | H9892 | |
| Hydrogen Peroxide | China National Pharmaceutical Group Chemical Reagent Co., Ltd. | B12555 | |
| Hypersensitive ECL chemiluminescence kit | NCM Biotech | P10300 | |
| ImageJ software | National Institutes of Health | v1.8.0 | |
| Imaging System | Nikon (Japan) | NIKON DS-U3 | |
| Lewis lung carcinoma cells | China National Pharmaceutical Group Chemical Reagent Co., Ltd. | 90020104 | |
| Mesh cloth | Baijie | 100110779650 | |
| Metal heating temperature control instrument | Baiwan Electronictechnology Co., Ltd. | HG221-X3 | |
| Methanol | Aladdin | M116118 | |
| Micropipette | Dlab Scientific Co., Ltd. | KE0003087/KA0056573 | |
| Microscope Slide | Jiangsu Shitai Laboratory Equipment Co., Ltd. | 10212432C | |
| Microtome | Shanghai Leica Instruments Co., Ltd. | RM2016 | |
| Microwave Oven | Galanz Microwave Electrical Appliances Co., Ltd. | P70D20TL-P4 | |
| Neutral Balsam | China National Pharmaceutical Group Chemical Reagent Co., Ltd. | 10004160 | |
| Optical microscope | Nikon (Japan) | Nikon Eclipse CI | |
| Oven | Shanghai Huitai Instrument Manufacturing Co., Ltd. | DHG-9140A | |
| PAGE gel rapid preparation kit | Biosharp | PL566B-5 | |
| Paraformaldehyde | China National Pharmaceutical Group Chemical Reagent Co., Ltd. | 8.18715 | |
| Phosphate buffered saline (1x) | Gibco | 8120485 | |
| Pre-stained color protein marker (10-180 kDa) | Cywin Innovation (Beijing) Biotechnology Co., Ltd. | SW176-02 | |
| Protein loading buffer (5X) | Boster Biological Technology | AR1112 | |
| pulverizer | Shangzhiqiao Co., Ltd. | DFT-100A | |
| PVDF (0.45 μm) | Cywin Innovation (Beijing) Biotechnology Co., Ltd. | SW120-01 | |
| Rapid membrane transfer solution | Cywin Innovation (Beijing) Biotechnology Co., Ltd. | SW171-02 | |
| RIPA lysate | Boster Biological Technology Co., Ltd. | AR0105 | |
| TBS buffer | NCM Biotech | 23HA0102 | |
| Tissue Flotation Workstation | Jinhua Kedi Instrument Equipment Co., Ltd., Zhejiang Province. | KD-P | |
| Transmembrane buffer | NCM Biotech | 23CA2000 | |
| Trypsin (0.25%, 1x) | HyClone | J210045 | |
| Ultrasonic cell disruption apparatus | Ningbo Xinyi ultrasonic equipment Co., Ltd. | JY92-IIDN | |
| Upright Optical Microscope | Nikon (Japan) | Nikon Eclipse CI | |
| vacuum lyophilizer | Lanjing Co., Ltd. | HD-LG20D | |
| Vortex mixer | Kylin-Bell | XW-80A | |
| Xylene | China National Pharmaceutical Group Chemical Reagent Co., Ltd. | 214736 |
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır