Method Article
Construção do Modelo de Xenoenxerto de Adenocarcinoma de Pulmão em Camundongos e Avaliação da Eficiência da Decocção XY através da Via MAPK
Neste Artigo
Resumo
Este estudo demonstra que a decocção XY exerce efeitos terapêuticos contra o adenocarcinoma de pulmão, regulando a via MAPK.
Resumo
O adenocarcinoma de pulmão está aumentando em todo o mundo, levando à exploração e desenvolvimento de métodos de tratamento eficazes. Nos últimos anos, o potencial terapêutico da medicina tradicional chinesa para adenocarcinoma de pulmão, como a decocção XiaoYi (XY), tem sido cada vez mais reconhecido. O mecanismo de ação da medicina tradicional chinesa no tratamento do adenocarcinoma de pulmão continua a ser elucidado. Neste estudo, modelos animais foram usados para investigar os efeitos terapêuticos da decocção XY no tratamento do adenocarcinoma de pulmão. Os componentes químicos de entrada no sangue da decocção XY em camundongos foram separados e analisados nos modos de íons positivos e negativos usando UHPLC-QE-MS. Os resultados foram então validados por meio de experimentos in vivo , que demonstraram redução do tamanho do tumor, melhora das alterações patológicas e aumento da apoptose. Como resultado, quinze componentes absorvidos no sangue após a administração da decocção XY foram identificados: Estaquiose, quercetina-3-O-beta-glicopiranosil-7-O-alfa-ramnopiranosídeo; Imperialine; Espinosina B; Peimine; Base de flavona + 3O, 2MeO, O-Hex; Picropodofilotoxina; (2S,3R,4S,5S,6R)-2-[(2R,3R,4S,5S,6R)-4,5-di-hidroxi-2 [[(3S,5R,8R,10R,12R,13R,14R,17S)-12-hidroxi-17-(2-hidroxi-6-metilhept-5-en-2-il) 4,4,8,10,14-pentametil-2,3,5,6,7,9,11,12,13,15,16,17-dodecahidro-1H ciclopenta[a]fenantreno-3-il]oxi]-6-(hidroximetil)oxano-3-il]oxi-6-(hidroximetil)oxano-3,4,5-triol; Tricina; Ginsenosídeo Rg1; (20R)-ginsenosídeo Rh1; Jujubosídeo B; Aucubina; Ginsenosídeo Rg3; e ácido beta-elemonico. Experimentos com animais demonstraram que a decocção XY inibiu o crescimento do tumor, melhorou as alterações patológicas e promoveu a apoptose das células tumorais de maneira dose-dependente. Os mecanismos envolvidos podem estar relacionados à regulação positiva da expressão das proteínas p-JNK e p-P38 na via MAPK e à regulação negativa da expressão da proteína p-ERK na via MAPK. Em conclusão, a decocção XY tem o potencial de regular a via MAPK e exercer efeitos terapêuticos contra o adenocarcinoma de pulmão.
Introdução
A incidência de câncer de pulmão está aumentando em todo o mundo. É responsável por 18% de todas as neoplasias malignas e é responsável por um número significativo de mortes relacionadas ao câncer 1,2. O câncer de pulmão de células não pequenas (CPCNP) é uma forma prevalente de câncer de pulmão, sendo o adenocarcinoma o principal tipopatológico 3. Devido aos seus sintomas insidiosos, o CPCNP é frequentemente diagnosticado em estágio avançado e apresenta alta taxa de mortalidade 4,5. Pacientes com NSCLC em estágio IV têm uma taxa de sobrevida de cinco anos de apenas 5%6, enquanto mesmo NSCLC em estágio inicial ressecável cirurgicamente tem uma taxa de sobrevida de cinco anos de apenas 50%7.
Atualmente, o tratamento do adenocarcinoma de pulmão inclui cirurgia, radioterapia, quimioterapia, imunoterapia e terapia direcionada. Além disso, a medicina tradicional chinesa (MTC) para adenocarcinoma de pulmão está sendo cada vez mais reconhecida e valorizada8. A MTC tem uma longa história e tem sido utilizada no tratamento de várias doenças oncológicas com resultados terapêuticos efetivos 9,10. Considera o corpo humano como uma entidade inteira, com o princípio terapêutico focado em restaurar o movimento do Qi (Qi refere-se à energia vital que promove a circulação do sangue e dos fluidos corporais, contribuindo para aumentar a imunidade e reduzir a inflamação em pacientes com NSCLC) nos órgãos internos para restaurar o equilíbrio geral e inibir a progressão do câncer.
A MTC não apenas trata doenças oncológicas com baixa toxicidade, múltiplos alvos e alta eficiência11, mas também facilita o reparo de danos causados por radioterapia e quimioterapia, prolongando a sobrevida12.
A tecnologia de cromatografia líquida-espectrometria de massa (LC-MS) integra cromatografia líquida com espectrometria de massa para obter a separação e detecção de componentes em misturas complexasde compostos 13. O LC-MS oferece alta resolução, alta sensibilidade e alta especificidade, permitindo a separação e identificação de vários componentes químicos em decocções da medicina tradicional chinesa (MTC). Quando combinada com a química medicinal sérica, que separa e detecta os componentes ativos de entrada sanguínea após administração oral14,15, a LC-MS permite a previsão e análise de potenciais mecanismos de ação da droga. Essa abordagem ajuda a entender a composição química e os componentes farmacológicos das decocções da MTC, fornecendo dados essenciais para pesquisas aprofundadas sobre seus efeitos farmacológicos e aplicações clínicas, tornando-a altamente aplicável na pesquisa da MTC16,17.
A via de sinalização MAPK desempenha um papel crucial na gênese, progressão, metástase e invasão do câncer de pulmão, com Erk, p38 e JNK como subfamílias importantes. As decocções de MTC demonstraram influenciar a expressão de proteínas na via MAPK18. A decocção XiaoYi (XY) é derivada da decocção YiGuan e é usada para tratar adenocarcinoma de pulmão no Primeiro Hospital Afiliado da Universidade de Medicina Chinesa de Changchun (Figura 1), demonstrando eficácia clínica precisa. No entanto, seu mecanismo terapêutico permanece obscuro.
Neste estudo, a cromatografia líquida de ultra-alta eficiência acoplada à espectrometria de massas Q-Exactive Orbitrap (UHPLC-QE-MS) foi empregada para elucidar o possível mecanismo terapêutico da decocção XY contra o adenocarcinoma de pulmão, e seus efeitos foram validados por meio de estudos in vivo .
Protocolo
Todos os procedimentos em animais foram aprovados pelo Comitê de Ética Animal da Universidade de Medicina Tradicional Chinesa de Changchun (Ética nº 2024008). Camundongos machos C57BL/6 com seis semanas de idade (20 ± 2 g), criados em condições específicas livres de patógenos (FPS), exibiram padrões típicos de atividade física em um ambiente controlado com temperatura e umidade constantes. Eles tinham acesso ad libitum a comida e água e eram mantidos sob um ciclo claro/escuro de 12 horas. Detalhes dos reagentes e equipamentos usados neste estudo são fornecidos na Tabela de Materiais.
1. Preparação do extrato aquoso de decocção XY
- Coloque Panax ginseng C.A. Mey (Renshen, 15 g), Chinemys reevesii (Gray) (Guiban, 30 g) e Trionyx sinensis Wiegmann (Biejia, 30 g) em um pote de decocção. Adicione 1000 mL de água deionizada e deixe de molho por 30 min em temperatura ambiente.
- Ferva as três ervas da etapa 1.1 por 1 h. Simultaneamente, mergulhe Rehmannia glutinosa Libosch (Dihuang, 30 g), Trichosanthes kirilowii Maxim. (Tianhuafen, 30 g), Coix lacryma-jobi L. var. mayuen (Roman.) Stapf (Yiyiren, 20 g), Paeonia lactiflora Pall. (Baishao, 30 g), Boswellia carterii Birdw. (Ruxiang, 7 g), Commiphora myrrha Engl. (Moyao, 7 g), Agrimonia pilosa Ledeb. (Xianhecao, 20 g), Alpinia oxyphylla Miq. (Yizhiren, 20 g), Ziziphus jujuba Mill. var. spinosa (Bunge) (Suanzaoren, 30 g), Melia toosendan Sieb. et Zucc. (Chuanlianzi, 5 g), Fritillaria thunbergii Miq. (Zhebeimu, 15 g), Anemarrhena asphodeloides Bge. (Zhimu, 10 g), Platycodon grandiflorum (Jacq.) (Jiegeng, 10 g), Polygala tenuifolia Willd. (Yuanzhi, 15 g) e Phragmites communis Trin. (Lugen, 30 g) em outro recipiente por 30 min. Após a imersão, transfira-os para a panela de decocção da etapa 1.1.
- Ferva todas as 18 ervas das etapas 1.1 e 1.2 por 30 min. Despeje o líquido de ervas, adicione 1000 mL de água deionizada e ferva por mais 30 min. Repita este processo de fervura três vezes para obter três porções de líquido de ervas, depois misture e misture bem.
- Filtre o líquido de ervas misturado através de um pano de 400 malhas. Concentre o filtrado sob pressão reduzida e, em seguida, transfira o líquido de ervas concentrado para o equipamento de resfriamento para processamento posterior.
- Despeje o líquido concentrado de ervas em uma bandeja de liofilização e coloque-o na câmara de pré-congelamento de um liofilizador a vácuo. Quando o pré-congelamento estiver concluído, transfira a bandeja para a câmara de secagem por sublimação para remover a água.
- Remova qualquer umidade residual em alta temperatura. Pulverize o extrato de ervas liofilizado usando um pulverizador para obter pó de decocção XY liofilizado fino (Figura 2).
2. Preparação de soro contendo medicamento
- Atribua aleatoriamente camundongos machos C57BL/6 de seis semanas de idade (20 ± 2 g) no grupo XiaoYi (XY) ou no grupo controle.
NOTA: A dose do camundongo foi calculada usando o fator de conversão de humano para camundongo:
Dose experimental equivalente para camundongos (g/kg) = {Dose humana (g/kg) / Peso corporal (70 kg)} x 9,1
Com base neste cálculo, a dosagem para camundongos foi determinada em 2,6 g / kg. - Pese 0,9152 g de pó de decocção XY liofilizado e dissolva-o em 3,2 mL de água destilada para preparar a solução do medicamento.
NOTA: Os camundongos foram jejuados por 12 h antes da administração oral. - Administre a decocção XY aos camundongos do grupo XY por meio de gavagem, enquanto administra ao grupo controle um volume equivalente de água deionizada.
- 2 h após a administração oral, anestesiar os camundongos com pentobarbital sódico (seguindo protocolos aprovados institucionalmente). Enuclear os globos oculares usando uma pinça para coletar amostras de sangue e, em seguida, sacrificar os camundongos por asfixia por CO2 seguida de luxação cervical seguindo as diretrizes éticas19.
- Deixe as amostras de sangue estabilizarem à temperatura ambiente por 90 min. Centrifugar a 3450 x g (4 °C) durante 15 min para recolher o sobrenadante.
3. Análise UHPLC-QE-MS
- Adicionar 100 mg de pó liofilizado por decocção XY a 500 μL de solução de extracção (metanol: água = 4:1). Misture bem, sonicate e incube em banho de água gelada por 1 h.
- Mantenha a mistura a -40 °C por 1 h e, em seguida, centrifugue a 13.800 x g (4 °C) por 15 min. Filtre o sobrenadante através de uma membrana de filtro de 0,22 μm e, em seguida, combine 100 μL de cada sobrenadante para criar amostras de controle de qualidade (CQ).
- Após descongelar as amostras de plasma, retire 400 μL da amostra de plasma do grupo controle e 400 μL das amostras de plasma do grupo XY. Adicione 40 μL de ácido clorídrico (2 mol/L) a cada amostra. Vortex por 1 min e deixe a mistura repousar a 4 °C por 15 min. Repita esta etapa quatro vezes.
- Adicione 1,6 mL de acetonitrila e vórtice por 5 min. Centrifugue a 13.800 x g por 5 min a 4 °C. Submeter 1.800 μL do sobrenadante à secagem de nitrogênio.
- Reconstituir as amostras secas em 150 μL de metanol a 80% contendo 10 μg/mL do padrão interno por vórtice por 5 min. Centrifugue a 13.800 × g por 5 min a 4 ° C e, em seguida, transfira 120 μL do sobrenadante para um frasco de vidro fresco para análise de LC-MS (Figura 3).
4. Cultura celular e preparação animal
- Semear 1 mL de células de carcinoma de pulmão de Lewis em uma placa de cultura contendo o meio de Eagle modificado de Dulbecco (DMEM) suplementado com 10% de soro fetal bovino e 1% de penicilina/estreptomicina. Incubar as células em condições controladas a 37 °C com 5% de CO2.
- Quando as células atingirem 80% de confluência, passe-as com tripsina a 0,25%. Continue passando até que o estado da célula se estabilize e, em seguida, ajuste a concentração da célula para 3 x 106 células/mL.
- Injete 0,1 mL da suspensão celular preparada por via subcutânea na axila direita de camundongos C57BL / 6 machos para estabelecer o modelo de adenocarcinoma de pulmão.
NOTA: O tecido tumoral pode ser palpado na axila de camundongos 5 dias após a inoculação. - Após 5 dias, dividir aleatoriamente os camundongos em cinco grupos (n = 6 por grupo): Grupo modelo (M) - Sem tratamento; Grupo de baixa dose de decocção XY (XY-L) - 1,3 g/kg; grupo de dose média de decocção XY (XY-Z) - 2,6 g/kg; Grupo de alta dose de decocção XY (XY-H) - 5,2 g / kg; Grupo cisplatina (DDP) - Tratado com cisplatina20.
- Dissolva o pó de decocção XY em 200 μL de água destilada na dose correspondente e administre-o por gavagem. Os grupos M e DDP recebem um volume igual de água destilada por gavagem .
- Administre cisplatina ao grupo DDP por injeção intraperitoneal (3 mg/kg) uma vez a cada 3 dias. Injete o mesmo volume de solução salina fisiológica nos outros grupos.
5. Análise patológica do tecido tumoral
- Após 21 dias, eutanasiar todos os camundongos usando asfixia por CO2 seguida de luxação cervical (seguindo as diretrizes éticas) e excisar o tecido tumoral21. Meça o volume e o peso do tumor (Figura 4).
- Fixe os tecidos tumorais excisados em paraformaldeído a 4% por 24 h). Desidrate o tecido usando soluções graduadas de etanol.
- Limpe os blocos de tecido desidratado usando xileno e incorpore-os em cera de parafina derretida. Deixe a cera solidificar em um bloco de parafina. Corte o bloco de tecido em fatias de 5 μm de espessura usando um micrótomo.
- Desparafinar as seções de tecido em xileno, seguido de reidratação em soluções graduadas de etanol. Pinte as seções com hematoxilina por 5 min e depois enxágue com água deionizada.
- Contra-corar as seções com solução de eosina a 0,5% por 1 min. Observe as seções coradas sob um microscópio óptico e capture imagens para análise.
6. Análise imuno-histoquímica do tecido tumoral
- Realize a desparafinação e a reidratação seguindo os procedimentos descritos nas etapas 5.2-5.4.
- Incubar as seções em um bloqueador de peroxidase endógena em temperatura ambiente por 15 min. Bloqueie a ligação não específica incubando as seções com soro de cabra.
- Aplique os anticorpos primários: Ki-67 (1:600) e Caspase-3 (1:100). Incubar as secções durante a noite a 4 °C. Lavar com tampão PBS), aplicar um anticorpo secundário de uso geral (1:500) e incubar a 37 °C durante 30 min.
- Desenvolva a reação de cor adicionando a solução DAB. Contra-corar as seções com solução de hematoxilina.
- Realize a desidratação, limpeza e selagem das seções manchadas. Observe a expressão da proteína sob um microscópio óptico e capture imagens para análise.
7. Análise de Western blot
- Homogeneizar os tecidos tumorais usando um lisador de tecidos. Extraia a proteína total e determine sua concentração usando um kit de ensaio de ácido bicinconínico (BCA) (consulte a Tabela de Materiais).
- Realize a quantificação de proteínas, seguida de eletroforese SDS-PAGE e transferência de proteínas para uma membrana.
- Incubar a membrana durante a noite a 4 °C com anticorpos primários: P38 (1:2000), p-P38 (1:1000), ERK (1:20000), p-ERK (1:500), JNK (1:2000), p-JNK (1:5000), β-actina (1:200) (ver Tabela de Materiais).
- No dia seguinte, incube a membrana com anticorpo secundário conjugado com peroxidase de rábano (HRP) à temperatura ambiente por 1,5 h. Detecte bandas de proteínas usando um sistema de quimioluminescência aprimorada (ECL).
NOTA: As intensidades das bandas proteicas foram quantificadas usando o software ImageJ.
Resultados
A solução em pó XY e as amostras de soro do grupo controle e do grupo XY foram analisadas usando UHPLC-QE-MS, revelando picos bem separados. Os diagramas de ionização total para os modos de íons positivos e negativos são mostrados na Figura 3. A composição da decocção XY foi identificada com base no tempo de retenção, modo de aquisição e fragmentos do espectro de massa. Quinze componentes de entrada de sangue foram identificados comparando-se o soro dos grupos de administração oral de decocção em branco e XY com os componentes da solução de pó XY (Tabela 1).
O gráfico de linhas de volume tumoral indica que após 21 dias de gavagem com decocção XY, o volume tumoral em camundongos diminuiu em comparação com o grupo M e exibiu um efeito dose-dependente (Figura 4). A histopatologia do tumor foi observada usando coloração H&E (Figura 5). No grupo M, as células tumorais estavam densamente dispostas e exibiam proliferação ativa, com abundante mitose patológica. À medida que a dose de decocção XY aumentava, o arranjo das células tumorais gradualmente se tornava esparso e o espaço intercelular aumentava. Vários graus de necrose foram observados nos tecidos tumorais, e a mitose patológica foi rara21.
Para verificar os efeitos da decocção XY na proliferação e apoptose de tecidos tumorais em camundongos, foram realizados experimentos de imuno-histoquímica (IHQ). Após a coloração com anticorpos Ki-67 e Caspase 3, foram observadas partículas amarelo-acastanhadas espalhadas nas seções de tecido tumoral. Em comparação com o grupo M, os níveis de Ki-67 nos tecidos tumorais dos grupos XY e DDP diminuíram sequencialmente, enquanto os níveis de Caspase 3 aumentaram (Figura 6).
Para determinar se a decocção XY exerce efeitos terapêuticos no adenocarcinoma de pulmão através da via MAPK, a análise de Western blot foi realizada em tecidos tumorais de camundongos. Conforme mostrado na Figura 7, o tratamento com decocção XY levou a uma diminuição na expressão de p-ERK, com o grupo XY-H apresentando uma diferença significativa em relação ao grupo M (p < 0,001). Os níveis de p-JNK e p-P38 aumentaram no grupo XY-H em comparação com o grupo M, com diferenças estatisticamente significativas observadas no grupo XY-H (p < 0,01) e no grupo DDP (p < 0,05) em comparação com o grupo M. Além disso, a diferença entre os grupos DDP e XY-H foi estatisticamente significativa.

Figura 1: Componentes da decocção XY. Esta figura apresenta os medicamentos individuais contidos na decocção XY. Clique aqui para ver uma versão maior desta figura.
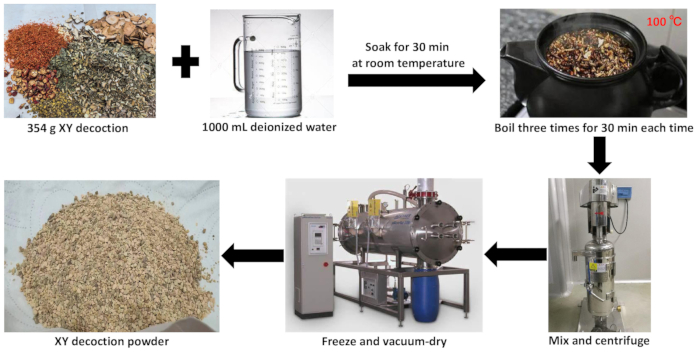
Figura 2: Preparação do extrato aquoso de decocção XY. Esta figura ilustra o processo de preparação do extrato aquoso da decocção XY. Clique aqui para ver uma versão maior desta figura.
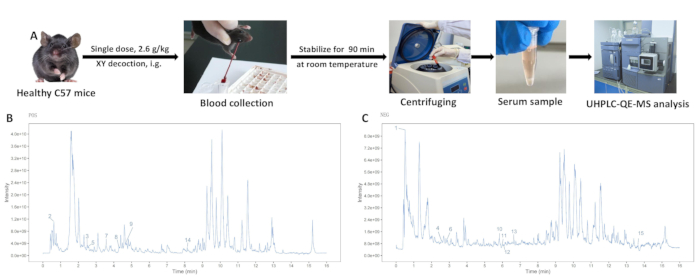
Figura 3: Análise do extrato aquoso de decocção XY. (A) O processo de extração do soro contendo drogas. (B) Análise por espectrometria de massa em modo de íons positivos. (C) Análise por espectrometria de massa em modo de íons negativos. Clique aqui para ver uma versão maior desta figura.

Figura 4: Efeitos da decocção XY no volume e morfologia do tumor de camundongo. (A) Cultura de células, implantação de tumor e procedimentos de amostragem. (B) Gráfico de linhas representando o volume do tumor ao longo do tempo. (C) Morfologia do tumor após 21 dias de tratamento por gavagem. Clique aqui para ver uma versão maior desta figura.
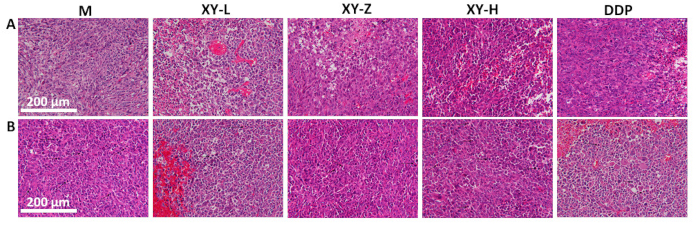
Figura 5: Análise histológica de tecidos tumorais de camundongos. (A) Arranjo do tecido tumoral tornando-se mais esparso com doses crescentes de decocção XY, com sinais de necrose de maneira dose-dependente. (B) Mitose patológica em tecidos tumorais, mostrando uma diminuição na mitose patológica com doses crescentes de decocção XY. Barras de escala: 200 μm. Clique aqui para ver uma versão maior desta figura.

Figura 6: Níveis de expressão de Ki-67 e Caspase-3. (A) Níveis de expressão de Ki-67. (B) Níveis de expressão de caspase-3. Barras de escala: 400 μm. (C) Quantificação de áreas positivas para Ki-67, mostrando uma diminuição com o aumento das doses de decocção XY. (D) Quantificação de áreas positivas para Caspase-3, mostrando um aumento com o aumento das doses de decocção XY. p < 0,001, **** p < 0,0001; ns, não significativo. Clique aqui para ver uma versão maior desta figura.

Figura 7: Níveis de expressão de proteínas na via MAPK. (A) Análise de Western blot da expressão de proteínas. (B) Níveis de expressão de ERK. (C) níveis de expressão de p-ERK. (D) Níveis de expressão de JNK. (E) níveis de expressão de p-JNK. (F) Níveis de expressão de P38. (G) níveis de expressão de p-P38. A decocção XY regulou positivamente a expressão das proteínas p-JNK e p-P38 enquanto regulava negativamente a expressão de p-ERK. *p < 0,05, **p < 0,01, ***p < 0,001. Clique aqui para ver uma versão maior desta figura.
| NÃO. | Compostos identificados | Fórmula | m/z | RT (min) | Erro de massa (ppm) | Adutos | Fonte | ||
| 1 | Estaquiose | C24H42O21 | 665.21 | 0.49 | 1.2 | [MH]- | Um | ||
| 2 | Quercetina-3-O-beta-glucopiranosil-7-O-alfa-ramnopiranosídeo | C4H9Nº2 | 609.14 | 0.61 | 7.16 | [M+H]+ | A, C | ||
| 3 | Imperialino | C27H43N.º3 | 430.33 | 2.5 | 0.13 | [M+H]+ | B | ||
| 4 | Espinosina B | C38H40O18 | 783.22 | 2.55 | 0.47 | [MH]- | F | ||
| 5 | Peimine | C27H45N.º3 | 432.35 | 2.62 | 1.19 | [M+H]+ | B | ||
| 6 | Base de flavona + 3O, 2MeO, O-Hex | C23H24O12 | 491.12 | 2.86 | 0.27 | [MH]- | G | ||
| 7 | Picropodofilotoxina | C22H22O8 | 415.14 | 3.54 | 2.25 | [M+H]+ | B, E | ||
| 8 | (2S,3R,4S,5S,6R)-2-[(2R,3R,4S,5S,6R)-4,5-dihidroxi-2-[[(3S,5R,8R,10R,12R,13R,14R,17S)-12-hidroxi-17-(2-hidroxi-6-metilhept-5-en-2-il)-4,4,8,10,14-pentametil-2,3,5,6,7,9,11,12,13,15,16,17-dodecahidro-1H-ciclopenta[a]fenantreno-3-il]oxi]-6-(hidroximetil)oxano-3-il]oxi-6-(hidroximetil)oxano-3,4,5-triol | C42H72O13 | 785.5 | 4.26 | 8.49 | [M+H]+ | D | ||
| 9 | Tricina | C17H14O7 | 331.08 | 4.67 | 0.85 | [M+H]+ | G | ||
| 10 | Ginsenosídeo Rg1 | C42H72O14 | 845.49 | 5.83 | 2.16 | [M+FA]- | D | ||
| 11 | (20R) -Ginsenosídeo Rh1 | C36H62O9 | 683.44 | 5.98 | 1.35 | [M+FA]- | D | ||
| 12 | Jujubosídeo B | C52H84O21 | 1089.55 | 6.11 | 1.3 | [M+FA]- | F | ||
| 13 | Aucubina | C15H22O9 | 391.12 | 6.71 | 1.11 | [M+FA]- | Um | ||
| 14 | Ginsenosídeo Rg3 | C42H72O13 | 807.48 | 8.1 | 5.3 | [M+NA]+ | D | ||
| 15 | ácido beta-elemonico | C30H46O3 | 453.34 | 13.74 | 0.42 | [MH]- | E | ||
Tabela 1: Componentes absorvidos pelo sangue após a administração de decocção XY. A tabela lista os componentes ativos detectados no sangue após a administração da decocção XY: A: Rehmannia glutinosa Libosch (Dihuang), B: Fritillaria thunbergii Miq. (Zhebeimu), C: Trichosanthes kirilowii Maxim. (Tianhuafen), D: Panax ginseng C.A. Mey (Renshen), E: Boswellia carterii Birdw. (Ruxiang), F: Ziziphus jujuba Mill. var. spinosa (Bunge) (Suanzaoren), G: Phragmites communis Trin. (Lugen).
Discussão
A incidência de câncer está aumentando anualmente, atraindo significativo interesse clínico e de pesquisa22,23. Estudos recentes demonstraram a eficácia da medicina tradicional chinesa (MTC) no tratamento do câncer de pulmão 24,25,26. Por exemplo, a decocção de Maimendong demonstrou aumentar o número e a atividade das células NK, inibindo assim a metástase do câncer de pulmão27. Da mesma forma, a decocção de Mahuang Fuzi Xixin alcançou efeitos terapêuticos no câncer de pulmão, influenciando várias vias de sinalização28. Este estudo utiliza análise de LC-MS e experimentos in vivo para prever os possíveis mecanismos pelos quais a decocção XY exerce efeitos terapêuticos no adenocarcinoma de pulmão.
A análise LC-MS identificou 15 componentes de entrada de sangue. Entre estes, a tricina e a picropodofilotoxina demonstraram inibir a resistência aos medicamentos e reduzir os níveis de expressão de p-PRKCA, SPHK1, SPHK2 e EGFR, suprimindo assim a atividade das células de câncer de pulmão29,30. O ginsenosídeo Rg1 e o ginsenosídeo Rg3, componentes do Panax ginseng CA Meyer, podem bloquear a mitose celular, inibir a sinalização da via mTOR, exercer efeitos antiangiogênicos, melhorar a função imunológica e, finalmente, inibir o crescimento e a metástase do tumor, reduzindo a resistência aos medicamentos 31,32,33,34. A estaquiose pode induzir a apoptose em células cancerígenas intestinais modulando a expressão de proteínas pró-apoptóticas35. A imperialina, um alcalóide com propriedades anti-inflamatórias e antiproliferativas, tem potencial como agente antitumoral em estágio inicial36. A peimina pode interromper o ciclo celular induzindo a apoptose, inibir a migração celular através do estresse do retículo endoplasmático e regular a expressão de proteínas relacionadas à via NF-κB para suprimir o crescimento de células de câncer de mama e gástrico37,38. Foi relatado que a aucubina e o jujubosídeo B promovem a autofagia e a apoptose nas células tumorais enquanto inibem a angiogênese, exercendo efeitos antitumorais 39,40,41.
A via MAPK é essencial para vários processos biológicos, incluindo ativação celular, proliferação, autofagia e apoptose. Vários compostos detectados nos componentes de entrada no sangue da decocção XY, como ginsenosídeo Rg1, ginsenosídeo Rg3, peimina e jujubosídeo B, podem exercer efeitos antitumorais através da via MAPK 42,43,44,45. A via MAPK envolve as cascatas de sinalização ERK, JNK e P38 e é amplamente estudada na pesquisa do câncer devido ao seu papel na regulação de processos fisiológicos por meio da ativação da cascata proteica de MAP3K-MAP2K-MAPK46,47.
A ativação da via ERK estimula a proliferação celular e inibe a apoptose, regulando a atividade e a expressão de proteínas pró-apoptóticas e antiapoptóticas nos níveis transcricional e translacional48,49. Os inibidores de proteínas direcionados à via ERK têm sido extensivamente estudados e são usados no tratamento do câncer 50,51,52. Os monômeros e formulações da medicina tradicional chinesa (MTC) também demonstraram exercer efeitos antitumorais modulando a via ERK. Por exemplo, a fórmula QYHJ inibe a proliferação e promove a apoptose de células de adenocarcinoma ductal pancreático, regulando a expressão de p-P38 e p-ERK1/253. Os derivados do ácido ferúlico suprimem a proliferação, interrompem o ciclo celular e induzem a apoptose na linha celular de câncer de pulmão humano A54954.
A via JNK / P38 desempenha papéis distintos ao regular diferentes proteínas efetoras a jusante por meio da fosforilação, influenciando assim o ciclo celular, a proliferação celular e a apoptose55,56. Estudos têm demonstrado que a triptolida modula a expressão de p-P38 e p-JNK e inibe a proliferação de células A549, exercendo efeitos antitumorais57. Além disso, a baicaleína induz apoptose em células HeLa, afetando a expressão de p-P38 e p-JNK58. Estudos in vivo e in vitro demonstraram que a injeção de Aidi influencia a expressão de p-JNK e p-P38 em células HepG2 e modelos de camundongos com carcinoma hepatocelular, inibindo assim a proliferação tumoral59.
O Ki-67 e a Caspase 3 são indicadores-chave da proliferação tumoral e da apoptose. Ki-67 é uma proteína nuclear altamente expressa durante a proliferação celular e ausente em células quiescentes (fase G0) 60 . Como o desenvolvimento do tumor está intimamente ligado à proliferação celular, a pesquisa sobre a correlação entre Ki-67 e tumorigênese ganhou atenção significativa. A expressão do Ki-67 está positivamente correlacionada com malignidade, agressividade e prognóstico do tumor 61,62, tornando-o um biomarcador amplamente utilizado para a proliferação do câncer63. Tem sido extensivamente estudada na patogênese e prognóstico dos cânceres gastrointestinal, pulmonar, de mama e cervical 64,65,66,67.
A família das caspases consiste em enzimas proteolíticas que regulam a apoptose e a inflamação. A caspase 3, encontrada principalmente no citoplasma, é um efetor chave da apoptose. Facilita a morte celular clivando proteínas do citoesqueleto, inativando proteínas inibidoras da apoptose e degradando enzimas de reparo de DNA 68,69,70. Alterações na expressão da Caspase 3 podem influenciar a sensibilidade das células tumorais à quimioterapia, afetando a invasão, metástase e a progressão de vários tipos de câncer 71,72,73,74.
Este estudo demonstrou que a decocção XY inibiu a proliferação tumoral em camundongos portadores de tumor LLC de maneira dose-dependente. A análise patológica dos tecidos tumorais dos grupos de tratamento XY e DDP revelou arranjos celulares mais frouxos em comparação com o grupo M, juntamente com mitose patológica reduzida. Além disso, necrose e hemorragia foram observadas nos tecidos tumorais dos grupos de tratamento. Os resultados da imuno-histoquímica (IHQ) confirmaram ainda que a decocção XY inibiu a proliferação de células tumorais e promoveu a apoptose de maneira dose-dependente. A análise de Western blot de tecidos tumorais indicou mudanças significativas nos níveis de expressão de proteínas-chave na via MAPK. No geral, os achados patológicos e de IHQ sugerem que a decocção XY exerce efeitos terapêuticos contra o adenocarcinoma de pulmão, modulando a expressão de proteínas na via de sinalização MAPK.
Divulgações
Os autores não têm nada a divulgar.
Agradecimentos
Este trabalho foi apoiado pelo Item do Plano de Desenvolvimento Científico e Tecnológico da Província de Jilin (YDZJ202301ZYTS459).
Materiais
| Name | Company | Catalog Number | Comments |
| Acetonitrile | CNW Technologies | 5/8/1975 | |
| 2-Chloro-L phenylalanine | Shanghai Hengbo Biotechnology Co., Ltd. | 103616-89-3 | |
| Ammonium Hydroxide Solution | China National Pharmaceutical Group Chemical Reagent Co., Ltd. | #2028 | |
| Antibody-β-actin | Abcam | ab8228 | |
| Anti-Erk1 (pT202/pY204) + Erk2 (pT185/pY187) Antibody | Abcam | ab4819 | |
| Anti-ERK1/ERK2 Antibody | Abcam | ab184699 | |
| Anti-JNK1 (pY185) + JNK2 (pY185) + JNK3 (pY223) Antibody | Abcam | ab76572 | |
| Anti-JNK1/JNK2/JNK3 Antibody | Abcam | ab208035 | |
| Anti-Ki67 Antibody | Cell Signaling Technology | GB121141 | |
| Anti-p38 (phospho T180) Antibody | Abcam | ab178867 | |
| Anti-p38 alpha/MAPK14 Antibody | Abcam | ab170099 | |
| BCA protein concentration assay kit | Boster Biological Technology | 17E17B46 | |
| Bovine Serum Albumin (BSA) | DAKO | BIOFROXX | |
| Broad-spectrum phosphatase inhibitor (100x) | Boster Biological Technology | AR1183 | |
| C57bl/6 mice | Liaoning Changsheng Biotechnology Co., Ltd. | SCXK2021-0006 | |
| Chromatographic column | Waters | ACQUITY UPLC BEH C18 1.7 μm2.1*100 mm | |
| Cisplatin | China National Pharmaceutical Group Chemical Reagent Co., Ltd. | 232120 | |
| Citrate (pH 6.0) Antigen Retrieval Solution | Wuhan Baiqiandu Biotechnology Co., Ltd. | B2010 | |
| Cover Slip | Jiangsu Shitai Laboratory Equipment Co., Ltd. | 10212432C | |
| Cryogenic Stage | Wuhan Junjie Electronics Co., Ltd. | JB-L5 | |
| DAB Chromogenic Kit | Jiangsu Shitai Laboratory Equipment Co., Ltd. | 2005289 | |
| Decolorization shaker | Beijing Liu Yi Instrument Factory | WD-9405A | |
| Dehydrator | Wuhan Junjie Electronics Co., Ltd. | JJ-12J | |
| Drying Oven | Shanghai Huitai Instrument Manufacturing Co., Ltd. | DHG-9140A | |
| Dulbecco's modified eagle medium | Gibco | 8121587 | |
| EDTA (pH 8.0) Antigen Retrieval Solution | Wuhan Baiqiandu Biotechnology Co., Ltd. | B2001 | |
| EDTA (pH 9.0) Antigen Retrieval Solution | Wuhan Baiqiandu Biotechnology Co., Ltd. | B2002 | |
| Electrophoresis buffer | NCM Biotech | 20230801 | |
| Embedding machine | Wuhan Junjie Electronics Co., Ltd. | JB-P5 | |
| Eosin | China National Pharmaceutical Group Chemical Reagent Co., Ltd. | 212954 | |
| Ethanol | China National Pharmaceutical Group Chemical Reagent Co., Ltd. | 493511 | |
| Fetal bovine serum | Gibco | 2166090RP | |
| Formic acid | SIGMA | 64-18-6 | |
| GraphPad Prism software | GraphPad software, LLC | Version 9.0.0 | |
| Hematoxylin | China National Pharmaceutical Group Chemical Reagent Co., Ltd. | H3136 | |
| High performance liquid chromatography | Agilent | 1260 Infinity II Prime | |
| High speed refrigerated centrifuge | Thermo Fisher Scientific | Legend Micro 17R | |
| High-Resolution Mass Spectrometry | Thermo Fisher Scientific | Q Exactive Focus | |
| HRP-conjugated Goat Anti-Mouse | SeraCare | 5220-0341 | |
| HRP-conjugated Goat Anti-Rabbit | SeraCare | 5220-0336 | |
| HRP-conjugated Goat Anti-Rabbit/Mouse Universal Secondary Antibody | DAKO | K5007 | |
| HRP-conjugated Goat Anti-Rat | SeraCare | 5220-0364 | |
| HRP-conjugated Rabbit Anti-Goat | SeraCare | 5220-0362 | |
| Hydrochloric acid | China National Pharmaceutical Group Chemical Reagent Co., Ltd. | H9892 | |
| Hydrogen Peroxide | China National Pharmaceutical Group Chemical Reagent Co., Ltd. | B12555 | |
| Hypersensitive ECL chemiluminescence kit | NCM Biotech | P10300 | |
| ImageJ software | National Institutes of Health | v1.8.0 | |
| Imaging System | Nikon (Japan) | NIKON DS-U3 | |
| Lewis lung carcinoma cells | China National Pharmaceutical Group Chemical Reagent Co., Ltd. | 90020104 | |
| Mesh cloth | Baijie | 100110779650 | |
| Metal heating temperature control instrument | Baiwan Electronictechnology Co., Ltd. | HG221-X3 | |
| Methanol | Aladdin | M116118 | |
| Micropipette | Dlab Scientific Co., Ltd. | KE0003087/KA0056573 | |
| Microscope Slide | Jiangsu Shitai Laboratory Equipment Co., Ltd. | 10212432C | |
| Microtome | Shanghai Leica Instruments Co., Ltd. | RM2016 | |
| Microwave Oven | Galanz Microwave Electrical Appliances Co., Ltd. | P70D20TL-P4 | |
| Neutral Balsam | China National Pharmaceutical Group Chemical Reagent Co., Ltd. | 10004160 | |
| Optical microscope | Nikon (Japan) | Nikon Eclipse CI | |
| Oven | Shanghai Huitai Instrument Manufacturing Co., Ltd. | DHG-9140A | |
| PAGE gel rapid preparation kit | Biosharp | PL566B-5 | |
| Paraformaldehyde | China National Pharmaceutical Group Chemical Reagent Co., Ltd. | 8.18715 | |
| Phosphate buffered saline (1x) | Gibco | 8120485 | |
| Pre-stained color protein marker (10-180 kDa) | Cywin Innovation (Beijing) Biotechnology Co., Ltd. | SW176-02 | |
| Protein loading buffer (5X) | Boster Biological Technology | AR1112 | |
| pulverizer | Shangzhiqiao Co., Ltd. | DFT-100A | |
| PVDF (0.45 μm) | Cywin Innovation (Beijing) Biotechnology Co., Ltd. | SW120-01 | |
| Rapid membrane transfer solution | Cywin Innovation (Beijing) Biotechnology Co., Ltd. | SW171-02 | |
| RIPA lysate | Boster Biological Technology Co., Ltd. | AR0105 | |
| TBS buffer | NCM Biotech | 23HA0102 | |
| Tissue Flotation Workstation | Jinhua Kedi Instrument Equipment Co., Ltd., Zhejiang Province. | KD-P | |
| Transmembrane buffer | NCM Biotech | 23CA2000 | |
| Trypsin (0.25%, 1x) | HyClone | J210045 | |
| Ultrasonic cell disruption apparatus | Ningbo Xinyi ultrasonic equipment Co., Ltd. | JY92-IIDN | |
| Upright Optical Microscope | Nikon (Japan) | Nikon Eclipse CI | |
| vacuum lyophilizer | Lanjing Co., Ltd. | HD-LG20D | |
| Vortex mixer | Kylin-Bell | XW-80A | |
| Xylene | China National Pharmaceutical Group Chemical Reagent Co., Ltd. | 214736 |
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados