Method Article
Построение модели ксенотрансплантата аденокарциномы легкого у мышей и оценка эффективности отвара XY через путь MAPK
В этой статье
Резюме
Это исследование демонстрирует, что отвар XY оказывает терапевтическое действие против аденокарциномы легкого, регулируя путь MAPK.
Аннотация
Аденокарцинома легкого растет во всем мире, что побуждает к исследованию и разработке эффективных методов лечения. В последние годы все больше признается терапевтический потенциал традиционной китайской медицины для лечения аденокарциномы легкого, такой как отвар СяоИ (XY). Механизм действия традиционной китайской медицины в лечении аденокарциномы легкого продолжает выясняться. В этом исследовании использовались животные модели для изучения терапевтических эффектов отвара XY в лечении аденокарциномы легкого. Входящие в кровь химические компоненты отвара XY у мышей разделяли и анализировали как в положительном, так и в отрицательном ионном режимах с использованием UHPLC-QE-MS. Затем результаты были подтверждены с помощью экспериментов in vivo , которые продемонстрировали уменьшение размера опухоли, улучшение патологических изменений и увеличение апоптоза. В результате были идентифицированы пятнадцать компонентов, всасывающихся в кровь после приема XY-отвара: Стахиоза, Кверцетин-3-О-бета-глюкопиранозил-7-О-альфа-рамнопиранозид; Империалин; Спинозин В; Пеймин; Флавоновая основа + 3O, 2MeO, O-Hex; Пикроподофиллотоксин; (2S,3R,4S,5S,6R)-2-[(2R,3R,4S,5S,6R)-4,5-дигидрокси-2 [[(3S,5R,8R,10R,12R,13R,14R,17S)-12-гидрокси-17-(2-гидрокси-6-метилгепт-5-ен-2-ил) 4,4,8,10,14-пентаметил-2,3,5,6,7,9,11,12,13,15,16,17-додекагидро-1H циклопента[a]фенантрен-3-ил]окси]-6-(гидроксиметил)оксан-3-ил]окси-6-(гидроксиметил)оксан-3,4,5-триол; Трицин; Гинзенозид Rg1; (20R)-гинзенозид Rh1; Джуджубозид В; Аукубин; гинзенозид Rg3; и бета-элемоновая кислота. Эксперименты на животных показали, что отвар XY подавляет рост опухоли, улучшает патологические изменения и способствует апоптозу опухолевых клеток дозозависимым образом. Задействованные механизмы могут быть связаны с повышением экспрессии белков p-JNK и p-P38 в пути MAPK и подавлением экспрессии белка p-ERK в пути MAPK. В заключение следует отметить, что XY-отвар обладает потенциалом для регулирования пути MAPK и оказания терапевтического эффекта против аденокарциномы легкого.
Введение
Заболеваемость раком легких растет во всем мире. На его долю приходится 18% всех злокачественных новообразований и он является причиной значительногочисла смертей, связанных с раком1,2. Немелкоклеточный рак легкого (НМРЛ) является распространенной формой рака легких, при этом аденокарцинома является основным патологическим типом3. Из-за своей коварной симптоматики НМРЛ часто диагностируется на поздней стадии и имеет высокий уровень летальности 4,5. Пациенты с НМРЛ IV стадии имеют пятилетнюю выживаемость всего 5%6, в то время как даже хирургически резектабельная ранняя стадия НМРЛ имеет пятилетнюю выживаемость всего 50%7.
В настоящее время лечение аденокарциномы легкого включает хирургическое вмешательство, лучевую терапию, химиотерапию, иммунотерапию и таргетную терапию. Кроме того, традиционная китайская медицина (ТКМ) для лечения аденокарциномы легкого получает все большее признание и ценится8. ТКМ имеет долгую историю и применяется в лечении различных онкологических заболеваний с эффективными терапевтическими результатами 9,10. Он рассматривает человеческое тело как единое целое, с терапевтическим принципом, направленным на восстановление движения Ци (Ци относится к жизненной энергии, которая способствует циркуляции крови и жидкостей организма, способствуя повышению иммунитета и уменьшению воспаления у пациентов с НМРЛ) во внутренних органах для восстановления общего баланса и замедления прогрессирования рака.
ТКМ не только лечит онкологические заболевания с низкой токсичностью, множественностью мишеней и высокойэффективностью11, но также облегчает восстановление повреждений, вызванных лучевой терапией и химиотерапией, тем самым продлевая выживаемость12.
Технология жидкостной хроматографии и масс-спектрометрии (ЖХ-МС) объединяет жидкостную хроматографию с масс-спектрометрией для достижения разделения и обнаружения компонентов в сложных смесях соединений13. LC-MS обладает высоким разрешением, высокой чувствительностью и высокой специфичностью, что позволяет разделять и идентифицировать различные химические компоненты в отварах традиционной китайской медицины (ТКМ). В сочетании с химическими веществами сыворотки, которые отделяют и обнаруживают активные компоненты, поступающие в кровь после перорального приема14,15, LC-MS позволяет прогнозировать и анализировать потенциальные механизмы действия лекарственных средств. Этот подход помогает понять химический состав и фармакологические компоненты отваров ТКМ, предоставляя важные данные для углубленных исследований их фармакологических эффектов и клинического применения, что делает его очень применимым в исследованиях ТКМ16,17.
Сигнальный путь MAPK играет решающую роль в генезе, прогрессировании, метастазировании и инвазии рака легких, при этом важными подсемействами являются Erk, p38 и JNK. Было показано, что отвары ТКМ влияют на экспрессию белков в пути MAPK18. Отвар XiaoYi (XY) получен из отвара YiGuan и используется для лечения аденокарциномы легкого в Первой аффилированной больнице Чанчуньского университета китайской медицины (Рисунок 1), демонстрируя точную клиническую эффективность. Однако его терапевтический механизм остается неясным.
В этом исследовании была использована ультравысокоэффективная жидкостная хроматография в сочетании с масс-спектрометрией Q-Exactive Orbitrap (UHPLC-QE-MS) для выяснения возможного терапевтического механизма применения отвара XY против аденокарциномы легкого, и его эффекты были подтверждены в ходе исследований in vivo .
протокол
Все процедуры на животных были одобрены Комитетом по этике животных Чанчуньского университета традиционной китайской медицины (Этика No 2024008). Шестинедельные самцы мышей C57BL/6 (20 ± 2 г), выведенные в специфических условиях, свободных от патогенов (SPF), демонстрировали типичные модели физической активности в контролируемой среде с постоянной температурой и влажностью. Они имели свободный доступ к пище и воде и поддерживались в течение 12-часового цикла свет/темнота. Подробная информация о реагентах и оборудовании, использованных в данном исследовании, представлена в Таблице материалов.
1. Приготовление XY отвара водного экстракта
- Положите в баночку для отвара женьшень Panax C.A. Mey (Renshen, 15 г), Chinemys reevesii (Gray) (Guiban, 30 г) и Trionyx sinensis Wiegmann (Biejia, 30 г). Добавьте 1000 мл деионизированной воды и замочите на 30 минут при комнатной температуре.
- Отварите три травы с шага 1.1 в течение 1 ч. Одновременно замочите Rehmannia glutinosa Libosch (Dihuang, 30 г), Trichosanthes kirilowii Maxim. (Тяньхуафэнь, 30 г), Coix lacryma-jobi L. var. mayuen (Roman.) Штапф (Yiyiren, 20 г), Paeonia lactiflora Pall. (Байшао, 30 г), Boswellia carterii Birdw. (Ruxiang, 7 г), Commiphora myrrha Engl. (Moyao, 7 г), Agrimonia pilosa Ledeb. (Xianhecao, 20 г), Alpinia oxyphylla Miq. (Yizhiren, 20 г), Ziziphus jujuba Mill. spinosa (Bunge) (Suanzaoren, 30 г), Melia toosendan Sieb. et Zucc. (Чуаньлянцзы, 5 г), Fritillaria thunbergii Miq. (Жебейму, 15 г), Anemarrhena asphodeloides Bge. (Жиму, 10 г), Platycodon grandiflorum (Jacq.) (Jiegeng, 10 г), Polygala tenuifolia Willd. (Юаньчжи, 15 г) и Phragmites communis Trin. (Люген, 30 г) в другую емкость на 30 мин. После замачивания переложите их в кастрюлю с отваром с шага 1.1.
- Отварите все 18 трав из шагов 1.1 и шага 1.2 в течение 30 минут. Вылейте травяную жидкость, добавьте 1000 мл деионизированной воды и кипятите еще 30 минут. Повторите этот процесс кипячения три раза, чтобы получить три порции травяной жидкости, затем соедините и тщательно перемешайте их.
- Перемешанную травяную жидкость процедите через ткань с плотностью 400 меш. Концентрируйте фильтрат под пониженным давлением, затем передайте концентрированную травяную жидкость в охлаждающее оборудование для дальнейшей обработки.
- Перелейте концентрированную травяную жидкость в лоток для лиофилизации и поместите его в камеру предварительного замораживания вакуумного лиофилизатора. После завершения предварительного замораживания перенесите лоток в сублимационную сушильную камеру для удаления воды.
- Удалите остатки влаги при высокой температуре. Измельчите лиофилизированный растительный экстракт с помощью пульверизатора, чтобы получить мелкодисперсный лиофилизированный порошок отвара XY (Рисунок 2).
2. Препарат из содержащей сыворотки
- Случайным образом распределите шестинедельных мышей-самцов C57BL/6 (20 ± 2 г) либо в группу XiaoYi (XY), либо в контрольную группу.
ПРИМЕЧАНИЕ: Мышиная доза была рассчитана с использованием коэффициента пересчета человека в мышь:
Эквивалентная экспериментальная доза для мышей (г/кг) = {Доза для человека (г/кг) / Масса тела (70 кг)} x 9,1
На основании этого расчета была определена дозировка для мышей в размере 2,6 г/кг. - Взвесьте 0,9152 г лиофилизированного порошка отвара XY и растворите его в 3,2 мл дистиллированной воды для приготовления раствора препарата.
Примечание: Мышей голодали в течение 12 ч перед пероральным введением. - Вводите отвар XY мышам в группе XY через зонд, в то время как контрольной группе вводите эквивалентный объем деионизированной воды.
- Через 2 ч после перорального приема обезболить мышей пентобарбиталом натрия (в соответствии с утвержденными в учреждении протоколами). Энуклеация глазных яблок с помощью пинцета для сбора образцов крови, затем эвтаназия мышей с помощью удушенияCO2 с последующим вывихом шейки матки в соответствии с этическимипринципами.
- Дайте образцам крови стабилизироваться при комнатной температуре в течение 90 минут. Центрифугируйте при 3450 x g (4 °C) в течение 15 минут для сбора надосадочной жидкости.
3. Анализ ВЭЖХЛХ-КЭ-МС
- Добавьте 100 мг лиофилизированного порошка отвара XY в 500 μл экстракционного раствора (метанол: вода = 4:1). Тщательно перемешать, обработать ультразвуком и выдерживать на ледяной водяной бане в течение 1 ч.
- Выдерживайте смесь при температуре -40 °C в течение 1 часа, затем центрифугируйте при 13 800 x g (4 °C) в течение 15 минут. Отфильтруйте надосадочную жидкость через фильтрующую мембрану толщиной 0,22 мкм, затем смешайте по 100 мкл каждой надосадочной жидкости для создания образцов для контроля качества (QC).
- После размораживания образцов плазмы отберите 400 мкл образца плазмы контрольной группы и 400 мкл образца плазмы группы XY. Добавьте 40 μL соляной кислоты (2 моль/л) в каждый образец. Вдохните в течение 1 минуты и дайте смеси настояться при температуре 4 °C в течение 15 минут. Повторите этот шаг четыре раза.
- Добавьте 1,6 мл ацетонитрила и вортекс на 5 минут. Центрифуга при 13 800 x g в течение 5 мин при 4 °C. Подвергнуть 1 800 мкл надосадочной жидкости азотной сушке.
- Восстановите высушенные образцы в 150 мкл 80% метанола, содержащего 10 мкг/мл внутреннего стандарта, путем вортексирования в течение 5 минут. Центрифугируйте при 13 800 × г в течение 5 мин при 4 °C, затем перенесите 120 мкл надосадочной жидкости в свежий стеклянный флакон для анализа LC-MS (рис. 3).
4. Клеточная культура и подготовка животных
- Засейте 1 мл клеток карциномы легкого Льюиса в чашке для культивирования, содержащей модифицированную орлиную среду Дульбекко (DMEM) с добавлением 10% эмбриональной бычьей сыворотки и 1% пенициллина/стрептомицина. Инкубируйте клетки в контролируемых условиях при 37 °C с 5%CO2.
- Когда клетки достигнут 80% слияния, пропустите их с помощью 0,25% трипсина. Продолжайте процеживание до тех пор, пока состояние клеток не стабилизируется, затем отрегулируйте концентрацию клеток до 3 x 106 клеток/мл.
- Введите 0,1 мл приготовленной клеточной суспензии подкожно в правую подмышечную впадину самцов мышей C57BL/6 для установления модели аденокарциномы легкого.
ПРИМЕЧАНИЕ: Опухолевая ткань может быть пальпирована в подмышечной впадине мышей через 5 дней после инокуляции. - Через 5 дней случайным образом разделите мышей на пять групп (n = 6 в группе): Модельная группа (M) - Без лечения; XY отвар низкодозированной группы (XY-L) - 1,3 г/кг; XY отвар средней дозы группы (XY-Z) - 2,6 г/кг; XY отвар высокодозированной группы (XY-H) - 5,2 г/кг; Группа цисплатина (ДДП) - обрабатывается цисплатином20.
- Растворите порошок отвара XY в 200 μл дистиллированной воды в соответствующей дозе и вводите через зонд. Группы M и DDP получают равный объем дистиллированной воды через зонд.
- Вводите цисплатин в группу ДДП путем внутрибрюшинной инъекции (3 мг/кг) один раз в 3 дня. Введите такой же объем физиологического раствора в другие группы.
5. Патологоанатомический анализ опухолевой ткани
- Через 21 день усыпить всех мышей с помощью удушения CO2 с последующим вывихом шейки матки (в соответствии с этическими нормами) и иссечь опухолевую ткань21. Измерьте объем и вес опухоли (рисунок 4).
- Зафиксировать иссеченные опухолевые ткани в 4% параформальдегиде на 24 ч). Обезвоживайте ткани с помощью градуированных растворов этанола.
- Очистите обезвоженные блоки ткани с помощью ксилола, затем погрузите их в расплавленный парафин. Дайте воску застыть в парафиновый блок. Разрежьте тканевый блок на срезы толщиной 5 мкм с помощью микротома.
- Депарафинизация срезов тканей в ксилоле с последующей регидратацией в дифференцированных растворах этанола. Срезы окрашивать гематоксилином в течение 5 минут, затем промыть деионизированной водой.
- Срезы закрасить 0,5% раствором эозина в течение 1 мин. Наблюдайте за окрашенными срезами под оптическим микроскопом и делайте снимки для анализа.
6. Иммуногистохимический анализ опухолевой ткани
- Выполните депарафинизацию и регидратацию в соответствии с процедурами, описанными в шагах 5.2-5.4.
- Инкубировать срезы в эндогенном блокаторе пероксидазы при комнатной температуре в течение 15 мин. Блокируйте неспецифическое связывание путем инкубации участков с козьей сывороткой.
- Применяют первичные антитела: Ki-67 (1:600) и Каспазу-3 (1:100). Инкубируйте секции в течение ночи при температуре 4 °C. Промойте буфером PBS), затем нанесите вторичное антитело общего назначения (1:500) и инкубируйте при 37 °C в течение 30 минут.
- Развивайте цветовую реакцию, добавляя раствор DAB. Срезы закрасьте раствором гематоксилина.
- Проведите обезвоживание, очистку и герметизацию испачканных участков. Наблюдайте за экспрессией белков под оптическим микроскопом и получайте изображения для анализа.
7. Вестерн-блоттинг
- Гомогенизируйте опухолевую ткань с помощью тканевого лизера. Извлеките общий белок и определите его концентрацию с помощью набора для анализа бицинхониловой кислоты (BCA) (см. Таблицу материалов).
- Выполните количественное определение белка с последующим электрофорезом SDS-PAGE и переносом белка на мембрану.
- Инкубировать мембрану в течение ночи при 4 °C с первичными антителами: P38 (1:2000), p-P38 (1:1000), ERK (1:20000), p-ERK (1:500), JNK (1:2000), p-JNK (1:5000), β-актином (1:200) (см. Таблицу материалов).
- На следующий день инкубируйте мембрану с конъюгированным вторичным антителом к пероксидазе хрена (HRP) при комнатной температуре в течение 1,5 ч. Обнаружение белковых полос с помощью системы усиленной хемилюминесценции (ECL).
ПРИМЕЧАНИЕ: Интенсивность белковой полосы была количественно определена с помощью программного обеспечения ImageJ.
Результаты
Порошковый раствор XY и образцы сыворотки из контрольной группы и группы XY были проанализированы с помощью UHPLC-QE-MS, выявив хорошо разделенные пики. Диаграммы суммарной ионизации для мод положительных и отрицательных ионов показаны на рисунке 3. Состав отвара XY был идентифицирован на основе времени удержания, режима получения и фрагментов масс-спектра. Пятнадцать компонентов кровотока были идентифицированы путем сравнения сыворотки группы холостого и XY отвара для перорального применения с компонентами порошкового раствора XY (табл. 1).
Линейный график объема опухоли показывает, что после 21 дня зондирования отваром XY объем опухоли у мышей уменьшился по сравнению с группой М и проявил дозозависимый эффект (рис. 4). Гистопатология опухоли наблюдалась с помощью H&E окрашивания (рис. 5). В группе М опухолевые клетки были плотно расположены и проявляли активную пролиферацию, с обильным патологическим митозом. По мере увеличения дозы XY-отвара расположение опухолевых клеток постепенно становилось разреженным, а межклеточное пространство увеличивалось. В опухолевых тканях наблюдались различные степени некроза, а патологический митоз был редким21.
Для проверки влияния отвара XY на пролиферацию и апоптоз опухолевых тканей у мышей были проведены иммуногистохимические эксперименты (ИГХ). После окрашивания антителами к Ki-67 и каспазе 3 в срезах опухолевой ткани наблюдались рассеянные коричневато-желтые частицы. По сравнению с М-группой, уровни Ki-67 в опухолевых тканях групп XY и DDP последовательно снижались, тогда как уровни каспазы 3 повышались (рис. 6).
Чтобы определить, оказывает ли XY отвар терапевтическое действие на аденокарциному легкого через путь MAPK, был проведен вестерн-блоттинг опухолевых тканей мышей. Как показано на рисунке 7, лечение отваром XY привело к снижению экспрессии p-ERK, при этом в группе XY-H наблюдалась значительная разница по сравнению с группой M (p < 0,001). Уровни p-JNK и p-P38 повысились в группе XY-H по сравнению с группой M, при этом статистически значимые различия наблюдались в группе XY-H (p < 0,01) и группе DDP (p < 0,05) по сравнению с группой M. Кроме того, разница между группами DDP и XY-H была статистически значимой.

Рисунок 1: Компоненты отвара XY. На этом рисунке представлены отдельные препараты, содержащиеся в отваре XY. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.
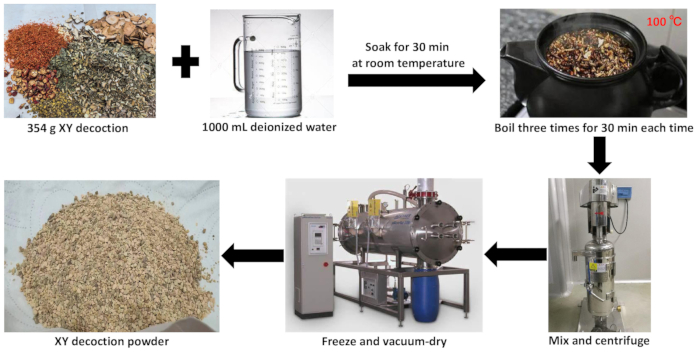
Рисунок 2: Приготовление XY отвара водного экстракта. На этом рисунке показан процесс приготовления водного экстракта отвара XY. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.
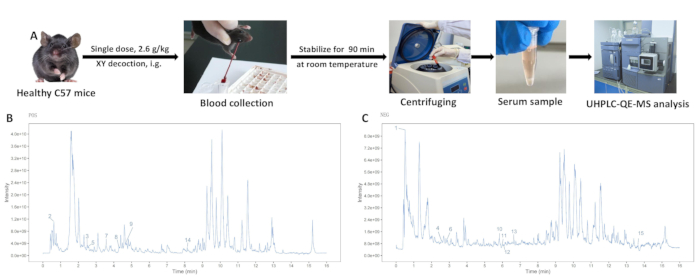
Рисунок 3: Анализ XY отвара водного экстракта. (А) Процесс экстракции лекарственно-содержащей сыворотки. (B) Масс-спектрометрический анализ в режиме положительных ионов. (В) Масс-спектрометрический анализ в режиме отрицательных ионов. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.

Рисунок 4: Влияние отвара XY на объем и морфологию опухоли мыши. (A) Культивирование клеток, имплантация опухоли и процедуры забора образцов. (B) Линейный график, отображающий объем опухоли с течением времени. (C) Морфология опухоли после 21 дня лечения зондовой зондацией. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.
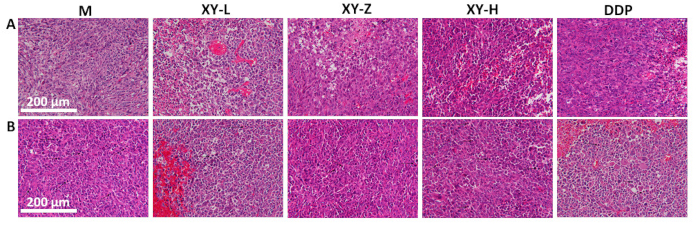
Рисунок 5: Гистологический анализ тканей опухоли мыши. (А) Расположение опухолевой ткани становится более редким с увеличением дозы отвара XY, с признаками некроза в зависимости от дозы. (Б) Патологический митоз в опухолевых тканях, демонстрирующий уменьшение патологического митоза с увеличением доз XY-отвара. Масштабные линейки: 200 μм. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.

Рисунок 6: Уровни экспрессии Ki-67 и каспазы-3. (А) Уровни экспрессии Ki-67. (В) Уровни экспрессии каспазы-3. Масштабные линейки: 400 мкм. (C) Количественная оценка Ki-67-положительных областей, показывающая уменьшение с увеличением доз XY-отвара. (D) Количественная оценка каспазы-3-положительных областей, показывающая увеличение с увеличением доз XY-отвара. p < 0,001, ****p < 0,0001; ns, не существенно. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.

Рисунок 7: Уровни экспрессии белка в пути MAPK. (A) Вестерн-блоттинг экспрессии белка. (B) Уровни экспрессии ERK. (C) уровни экспрессии p-ERK. (D) Уровни экспрессии JNK. (E) уровни экспрессии p-JNK. (F) Уровни экспрессии P38. (G) уровни экспрессии p-P38. Отвар XY повышал экспрессию белков p-JNK и p-P38 при одновременном подавлении экспрессии p-ERK. *p < 0,05, **p < 0,01, ***p < 0,001. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.
| НЕТ. | Идентифицированные соединения | Формула | м/з | RT (мин) | Погрешность массы (ppm) | Аддукторы | Источник | ||
| 1 | Стахиосе | С24В42О21 | 665.21 | 0.49 | 1.2 | [М-Х]- T | A | ||
| 2 | Кверцетин-3-О-бета-глюкопиранозил-7-О-альфа-рамнопиранозид | C4H9NO2 | 609.14 | 0.61 | 7.16 | [М+Ч]+ T | А, В | ||
| 3 | Империалина | C27H43NO3 | 430.33 | 2.5 | 0.13 | [М+Ч]+ T | B | ||
| 4 | Спинозин В | С38В40О18 | 783.22 | 2.55 | 0.47 | [М-Х]- T | F | ||
| 5 | Пеймин | C27H45NO3 | 432.35 | 2.62 | 1.19 | [М+Ч]+ T | B | ||
| 6 | Флавоновая основа + 3O, 2MeO, O-Hex | C23H24O12 | 491.12 | 2.86 | 0.27 | [М-Х]- T | G | ||
| 7 | Пикроподофиллотоксин | C22H22O8 | 415.14 | 3.54 | 2.25 | [М+Ч]+ T | В, Е | ||
| 8 | (2S,3R,4S,5S,6R)-2-[(2R,3R,4S,5S,6R)-4,5-дигидрокси-2-[[(3S,5R,8R,10R,12R,13R,14R,17S)-12-гидрокси-17-(2-гидрокси-6-метилгепт-5-ен-2-ил)-4,4,8,10,14-пентаметил-2,3,5,6,7,9,11,12,13,15,16,17-додекагидро-1H-циклопента[a]фенантрен-3-ил]окси]-6-(гидроксиметил)оксан-3-ил]окси-6-(гидроксиметил)оксан-3,4,5-триол | С42В72О13 | 785.5 | 4.26 | 8.49 | [М+Ч]+ T | D | ||
| 9 | Трицин | С17В14О7 | 331.08 | 4.67 | 0.85 | [М+Ч]+ T | G | ||
| 10 | Гинзенозид Rg1 | С42В72О14 | 845.49 | 5.83 | 2.16 | [М+ФА]- T | D | ||
| 11 | (20R)-Гинзенозид Rh1 | С36В62О9 | 683.44 | 5.98 | 1.35 | [М+ФА]- T | D | ||
| 12 | Джуджубозид В | С52В84О21 | 1089.55 | 6.11 | 1.3 | [М+ФА]- T | F | ||
| 13 | Аукубин | C15H22O9 | 391.12 | 6.71 | 1.11 | [М+ФА]- T | A | ||
| 14 | Гинзенозид Rg3 | С42В72О13 | 807.48 | 8.1 | 5.3 | [М+На]+ T | D | ||
| 15 | бета-элемоновая кислота | C30В46O3 | 453.34 | 13.74 | 0.42 | [М-Х]- T | E | ||
Таблица 1: Компоненты, всасывающиеся в кровь после приема отвара XY. В таблице перечислены активные компоненты, обнаруженные в крови после приема XY отвара: А: Rehmannia glutinosa Libosch (Dihuang), В: Fritillaria thunbergii Miq. (Zhebeimu), C: Trichosanthes kirilowii Maxim. (Тяньхуафэнь), D: Panax ginseng C.A. Mey (Renshen), E: Boswellia carterii Birdw. (Ruxiang), F: Ziziphus jujuba Mill. var. spinosa (Bunge) (Suanzaoren), G: Phragmites communis Trin. (Люген).
Обсуждение
Заболеваемость раком ежегодно растет, привлекая значительный клинический и исследовательский интерес22,23. Недавние исследования продемонстрировали эффективность традиционной китайской медицины (ТКМ) в лечении рака легких 24,25,26. Например, было показано, что отвар маймендонга увеличивает количество и активность NK-клеток, тем самым подавляя метастазирование рака легких27. Аналогичным образом, отвар Махуан Фуцзы Сисинь достиг терапевтического эффекта при раке легких, воздействуя на множественные сигнальные пути28. В этом исследовании используется анализ LC-MS и эксперименты in vivo для прогнозирования возможных механизмов, с помощью которых отвар XY оказывает терапевтическое воздействие на аденокарциному легкого.
Анализ ЖХ-МС выявил 15 компонентов крови. Среди них было показано, что трицин и пикроподофиллотоксин подавляют лекарственную устойчивость и снижают уровни экспрессии p-PRKCA, SPHK1, SPHK2 и EGFR, тем самым подавляя активность клеток рака легкого29,30. Гинзенозид Rg1 и гинзенозид Rg3, компоненты женьшеня обыкновенного C.A. Meyer, могут блокировать митоз клеток, ингибировать передачу сигналов mTOR, оказывать антиангиогенное действие, усиливать иммунную функцию и, в конечном итоге, подавлять рост опухоли и метастазирование при одновременном снижении лекарственной устойчивости 31,32,33,34. Стахиоза может индуцировать апоптоз в клетках рака кишечника путем модуляции экспрессии проапоптотических белков35. Империалин, алкалоид с противовоспалительными и антипролиферативными свойствами, обладает потенциалом в качестве противоопухолевого агента на ранних стадиях36. Пеймин может останавливать клеточный цикл, вызывая апоптоз, ингибировать миграцию клеток через стресс эндоплазматического ретикулума и регулировать экспрессию белка, связанного с NF-κB путем, для подавления роста клеток рака молочной железы и желудка 37,38. Сообщалось, что аукубин и джуджубозид В способствуют аутофагии и апоптозу в опухолевых клетках, ингибируя ангиогенез, тем самым оказывая противоопухолевое действие 39,40,41.
Путь MAPK необходим для различных биологических процессов, включая активацию клеток, пролиферацию, аутофагию и апоптоз. Некоторые соединения, обнаруженные в входящих в кровь компонентах отвара XY, такие как гинзенозид Rg1, гинзенозид Rg3, пеймин и джуджубозид В, могут оказывать противоопухолевое действие через путь MAPK 42,43,44,45. Путь MAPK включает в себя сигнальные каскады ERK, JNK и P38 и широко изучается в исследованиях рака из-за его роли в регулировании физиологических процессов через активацию белкового каскада MAP3K-MAP2K-MAPK46,47.
Активация пути ERK стимулирует пролиферацию клеток и ингибирует апоптоз путем регуляции активности и экспрессии проапоптотических и антиапоптотических белков на транскрипционном и трансляционном уровнях 48,49. Белковые ингибиторы, нацеленные на путь ERK, были широко изучены и используются в лечении рака 50,51,52. Также было показано, что мономеры и составы традиционной китайской медицины (ТКМ) оказывают противоопухолевое действие, модулируя путь ERK. Например, формула QYHJ ингибирует пролиферацию и способствует апоптозу клеток протоковой аденокарциномы поджелудочной железы, регулируя экспрессию p-P38 и p-ERK1/253. Производные феруловой кислоты подавляют пролиферацию, останавливают клеточный цикл и индуцируют апоптоз в клеточной линии54 рака легких человека A549.
Путь JNK/P38 играет различные роли, регулируя различные нижестоящие эффекторные белки посредством фосфорилирования, тем самым влияя на клеточный цикл, пролиферацию клеток и апоптоз55,56. Исследования показали, что триптолид модулирует экспрессию p-P38 и p-JNK и ингибирует пролиферацию клеток A549, оказывая противоопухолевое действие57. Кроме того, байкалеин индуцирует апоптоз в клетках HeLa, влияя на экспрессию p-P38 и p-JNK58. Исследования in vivo и in vitro показали, что инъекция Aidi влияет на экспрессию p-JNK и p-P38 в клетках HepG2 и моделях мышей с гепатоцеллюлярной карциномой, тем самым ингибируя пролиферацию опухоли59.
Ki-67 и Каспаза 3 являются ключевыми индикаторами пролиферации и апоптоза опухолей. Ki-67 представляет собой ядерный белок, который высоко экспрессируется во время пролиферации клеток и отсутствует в покоящихся клетках (фаза G0)60. Поскольку развитие опухоли тесно связано с пролиферацией клеток, исследования корреляции между Ki-67 и онкогенезом привлекли значительное внимание. Экспрессия Ki-67 положительно коррелирует со злокачественностью опухоли, агрессивностью и прогнозом61,62, что делает его широко используемым биомаркером пролиферации рака63. Он был широко изучен в патогенезе и прогнозе рака желудочно-кишечного тракта, легких, молочной железы и шейки матки 64,65,66,67.
Семейство каспаз состоит из протеолитических ферментов, которые регулируют апоптоз и воспаление. Каспаза 3, в основном обнаруженная в цитоплазме, является ключевым эффектором апоптоза. Он способствует гибели клеток, расщепляя белки цитоскелета, инактивируя белки, ингибирующие апоптоз, и разрушая ферменты репарации ДНК 68,69,70. Изменения в экспрессии каспазы 3 могут влиять на чувствительность опухолевых клеток к химиотерапии, тем самым влияя на инвазию, метастазирование и прогрессирование различных видов рака 71,72,73,74.
Это исследование показало, что отвар XY ингибирует пролиферацию опухолей у мышей с опухолями LLC дозозависимым образом. Патологический анализ опухолевых тканей в группах лечения XY и DDP выявил более рыхлое расположение клеток по сравнению с М-группой, а также снижение патологического митоза. Кроме того, в опухолевых тканях групп лечения наблюдались некроз и кровоизлияния. Результаты иммуногистохимии (ИГХ) также подтвердили, что отвар XY ингибирует пролиферацию опухолевых клеток и способствует апоптозу дозозависимым образом. Вестерн-блоттинг опухолевых тканей показал значительные изменения в уровнях экспрессии ключевых белков в пути MAPK. В целом, патологические данные и данные ИГХ свидетельствуют о том, что отвар XY оказывает терапевтическое действие против аденокарциномы легкого, модулируя экспрессию белков в сигнальном пути MAPK.
Раскрытие информации
Авторам нечего раскрывать.
Благодарности
Эта работа была поддержана пунктом (YDZJ202301ZYTS459) Плана развития науки и технологий провинции Цзилинь.
Материалы
| Name | Company | Catalog Number | Comments |
| Acetonitrile | CNW Technologies | 5/8/1975 | |
| 2-Chloro-L phenylalanine | Shanghai Hengbo Biotechnology Co., Ltd. | 103616-89-3 | |
| Ammonium Hydroxide Solution | China National Pharmaceutical Group Chemical Reagent Co., Ltd. | #2028 | |
| Antibody-β-actin | Abcam | ab8228 | |
| Anti-Erk1 (pT202/pY204) + Erk2 (pT185/pY187) Antibody | Abcam | ab4819 | |
| Anti-ERK1/ERK2 Antibody | Abcam | ab184699 | |
| Anti-JNK1 (pY185) + JNK2 (pY185) + JNK3 (pY223) Antibody | Abcam | ab76572 | |
| Anti-JNK1/JNK2/JNK3 Antibody | Abcam | ab208035 | |
| Anti-Ki67 Antibody | Cell Signaling Technology | GB121141 | |
| Anti-p38 (phospho T180) Antibody | Abcam | ab178867 | |
| Anti-p38 alpha/MAPK14 Antibody | Abcam | ab170099 | |
| BCA protein concentration assay kit | Boster Biological Technology | 17E17B46 | |
| Bovine Serum Albumin (BSA) | DAKO | BIOFROXX | |
| Broad-spectrum phosphatase inhibitor (100x) | Boster Biological Technology | AR1183 | |
| C57bl/6 mice | Liaoning Changsheng Biotechnology Co., Ltd. | SCXK2021-0006 | |
| Chromatographic column | Waters | ACQUITY UPLC BEH C18 1.7 μm2.1*100 mm | |
| Cisplatin | China National Pharmaceutical Group Chemical Reagent Co., Ltd. | 232120 | |
| Citrate (pH 6.0) Antigen Retrieval Solution | Wuhan Baiqiandu Biotechnology Co., Ltd. | B2010 | |
| Cover Slip | Jiangsu Shitai Laboratory Equipment Co., Ltd. | 10212432C | |
| Cryogenic Stage | Wuhan Junjie Electronics Co., Ltd. | JB-L5 | |
| DAB Chromogenic Kit | Jiangsu Shitai Laboratory Equipment Co., Ltd. | 2005289 | |
| Decolorization shaker | Beijing Liu Yi Instrument Factory | WD-9405A | |
| Dehydrator | Wuhan Junjie Electronics Co., Ltd. | JJ-12J | |
| Drying Oven | Shanghai Huitai Instrument Manufacturing Co., Ltd. | DHG-9140A | |
| Dulbecco's modified eagle medium | Gibco | 8121587 | |
| EDTA (pH 8.0) Antigen Retrieval Solution | Wuhan Baiqiandu Biotechnology Co., Ltd. | B2001 | |
| EDTA (pH 9.0) Antigen Retrieval Solution | Wuhan Baiqiandu Biotechnology Co., Ltd. | B2002 | |
| Electrophoresis buffer | NCM Biotech | 20230801 | |
| Embedding machine | Wuhan Junjie Electronics Co., Ltd. | JB-P5 | |
| Eosin | China National Pharmaceutical Group Chemical Reagent Co., Ltd. | 212954 | |
| Ethanol | China National Pharmaceutical Group Chemical Reagent Co., Ltd. | 493511 | |
| Fetal bovine serum | Gibco | 2166090RP | |
| Formic acid | SIGMA | 64-18-6 | |
| GraphPad Prism software | GraphPad software, LLC | Version 9.0.0 | |
| Hematoxylin | China National Pharmaceutical Group Chemical Reagent Co., Ltd. | H3136 | |
| High performance liquid chromatography | Agilent | 1260 Infinity II Prime | |
| High speed refrigerated centrifuge | Thermo Fisher Scientific | Legend Micro 17R | |
| High-Resolution Mass Spectrometry | Thermo Fisher Scientific | Q Exactive Focus | |
| HRP-conjugated Goat Anti-Mouse | SeraCare | 5220-0341 | |
| HRP-conjugated Goat Anti-Rabbit | SeraCare | 5220-0336 | |
| HRP-conjugated Goat Anti-Rabbit/Mouse Universal Secondary Antibody | DAKO | K5007 | |
| HRP-conjugated Goat Anti-Rat | SeraCare | 5220-0364 | |
| HRP-conjugated Rabbit Anti-Goat | SeraCare | 5220-0362 | |
| Hydrochloric acid | China National Pharmaceutical Group Chemical Reagent Co., Ltd. | H9892 | |
| Hydrogen Peroxide | China National Pharmaceutical Group Chemical Reagent Co., Ltd. | B12555 | |
| Hypersensitive ECL chemiluminescence kit | NCM Biotech | P10300 | |
| ImageJ software | National Institutes of Health | v1.8.0 | |
| Imaging System | Nikon (Japan) | NIKON DS-U3 | |
| Lewis lung carcinoma cells | China National Pharmaceutical Group Chemical Reagent Co., Ltd. | 90020104 | |
| Mesh cloth | Baijie | 100110779650 | |
| Metal heating temperature control instrument | Baiwan Electronictechnology Co., Ltd. | HG221-X3 | |
| Methanol | Aladdin | M116118 | |
| Micropipette | Dlab Scientific Co., Ltd. | KE0003087/KA0056573 | |
| Microscope Slide | Jiangsu Shitai Laboratory Equipment Co., Ltd. | 10212432C | |
| Microtome | Shanghai Leica Instruments Co., Ltd. | RM2016 | |
| Microwave Oven | Galanz Microwave Electrical Appliances Co., Ltd. | P70D20TL-P4 | |
| Neutral Balsam | China National Pharmaceutical Group Chemical Reagent Co., Ltd. | 10004160 | |
| Optical microscope | Nikon (Japan) | Nikon Eclipse CI | |
| Oven | Shanghai Huitai Instrument Manufacturing Co., Ltd. | DHG-9140A | |
| PAGE gel rapid preparation kit | Biosharp | PL566B-5 | |
| Paraformaldehyde | China National Pharmaceutical Group Chemical Reagent Co., Ltd. | 8.18715 | |
| Phosphate buffered saline (1x) | Gibco | 8120485 | |
| Pre-stained color protein marker (10-180 kDa) | Cywin Innovation (Beijing) Biotechnology Co., Ltd. | SW176-02 | |
| Protein loading buffer (5X) | Boster Biological Technology | AR1112 | |
| pulverizer | Shangzhiqiao Co., Ltd. | DFT-100A | |
| PVDF (0.45 μm) | Cywin Innovation (Beijing) Biotechnology Co., Ltd. | SW120-01 | |
| Rapid membrane transfer solution | Cywin Innovation (Beijing) Biotechnology Co., Ltd. | SW171-02 | |
| RIPA lysate | Boster Biological Technology Co., Ltd. | AR0105 | |
| TBS buffer | NCM Biotech | 23HA0102 | |
| Tissue Flotation Workstation | Jinhua Kedi Instrument Equipment Co., Ltd., Zhejiang Province. | KD-P | |
| Transmembrane buffer | NCM Biotech | 23CA2000 | |
| Trypsin (0.25%, 1x) | HyClone | J210045 | |
| Ultrasonic cell disruption apparatus | Ningbo Xinyi ultrasonic equipment Co., Ltd. | JY92-IIDN | |
| Upright Optical Microscope | Nikon (Japan) | Nikon Eclipse CI | |
| vacuum lyophilizer | Lanjing Co., Ltd. | HD-LG20D | |
| Vortex mixer | Kylin-Bell | XW-80A | |
| Xylene | China National Pharmaceutical Group Chemical Reagent Co., Ltd. | 214736 |
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены