Method Article
Implante de válvula aórtica transfemoral transfemoral asistida por litotricia intravascular
En este artículo
Resumen
Se ha demostrado que el implante de válvula aórtica transcatéter (TAVI) genera los mejores resultados clínicos cuando se realiza mediante el abordaje transfemoral percutáneo. La litotricia intravascular (IVL) puede facilitar un proceso transfemoral en pacientes con enfermedad vascular iliofemoral calcificada y diámetros intraluminales limítrofes. El presente protocolo describe la TAVI transfemoral asistida por IVL.
Resumen
Durante la última década, el implante de válvula aórtica transcatéter (TAVI) ha evolucionado como una terapia bien establecida para los pacientes mayores que sufren de estenosis valvular aórtica grave sintomática. Esto también se refleja en las guías internacionales recientemente actualizadas sobre el manejo de pacientes con valvulopatías. Un enfoque TAVI transfemoral (TF) ha demostrado ser superior a las estrategias de acceso alternativas. Con la introducción de la litotricia intravascular (IVL), los pacientes con enfermedad vascular iliofemoral calcificada y diámetros intraluminales limítrofes también se han convertido en candidatos para TF-TAVI percutánea. Además, la IVL reduce el riesgo de complicaciones vasculares mayores al modificar el calcio vascular superficial y profundo, cambiando así la distensibilidad del vaso y controlando la expansión luminal. De esta manera, se ha demostrado que la IVL facilita de forma segura la administración de TF de dispositivos TAVI en pacientes con enfermedad arterial periférica calcificada. El presente artículo tiene como objetivo proporcionar una descripción detallada paso a paso sobre cómo realizar TF-TAVI asistido por IVL de manera segura y eficiente. Además, se incluye una revisión de la literatura sobre los resultados obtenidos con esta tecnología, junto con una discusión concisa sobre este enfoque único de TAVI.
Introducción
El implante valvular aórtico transcatéter (TAVI) ha demostrado ser un tratamiento valioso para los pacientes ancianos que padecen estenosis valvular aórtica (EA) grave sintomática en todas las categorías de riesgo quirúrgico 1,2. Los datos y los resultados son más convincentes para aquellos pacientes en los que el procedimiento de TAVI se puede realizar por abordaje transfemoral (TF). También se puede considerar la TAVI por acceso alternativo, como el acceso transsubclavio, transaxilar, transcarotídeo, transcaval y transapical. Sin embargo, las tasas de complicaciones reportadas para TAVI por acceso alternativo son mayores que TF-TAVI 3,4. Esto también se refleja en las guías más recientes de la UE y los Estados Unidos sobre el manejo de pacientes con valvulopatía5, en las que existe un papel destacado para el TF-TAVI como opción de tratamiento para los pacientes con EA grave sintomática.
A pesar de que existe consenso en que el TF-TAVI debe ser la estrategia predeterminada para los pacientes con acceso iliofemoral adecuado5, la enfermedad arterial periférica (EAP) no es infrecuente en los pacientes programados para TAVI, dada su edad avanzada y a menudo múltiples comorbilidades6. En los últimos años se ha producido una rápida evolución tecnológica en el campo de TAVI, lo que ha dado lugar a dispositivos TAVI con perfiles de inserción más bajos y sistemas de administración más flexibles. Además, el aumento de la experiencia del operador ha aumentado el uso de un enfoque TF-TAVI totalmente percutáneo. En la actualidad, más del 90% de los casos de TAVI se realizan de esta forma en los centros de TAVI más avanzados7.
Aun así, un grupo de pacientes (5%-10%) siguen siendo buenos candidatos para TAVI, pero sufren de EAP severamente calcificada. Para muchos de estos pacientes, la introducción de la litotricia intravascular periférica (IVL) ha abierto la posibilidad de ser tratados con TF-TAVI. Cuando se utiliza IVL, se generan ondas de presión sónicas utilizando emisores de litotriptores miniaturizados integrados dentro de un globo. Se crea una burbuja de vapor dentro del globo que se expande y colapsa rápidamente mediante la entrega de energía eléctrica. Esto genera ondas de presión sónicas, similares en su forma de onda a las utilizadas durante la litotricia extracorpórea de la nefrolitiasis. Estas ondas viajan a través del vaso con una presión máxima positiva de alrededor de 50 atm, agrietando y modificando el calcio vascular tanto superficial como profundo, cambiando en última instancia la distensibilidad del vaso y permitiendo una expansión luminal controlada 8,9,10 (Figura 1). De esta forma, se ha demostrado que la IVL facilita la administración de TF de dispositivos TAVI en pacientes con EAP calcificada de forma segura 11,10,13. Estos balones IVL están disponibles en diferentes diámetros que oscilan entre 3,5 mm y 7 mm con una longitud de 60 mm.
El presente artículo tiene como objetivo proporcionar una descripción detallada de la realización de TF-TAVI asistida por IVL de manera segura y eficiente. Además, se incluye una revisión bibliográfica sobre los resultados obtenidos con esta tecnología, junto con una discusión concisa sobre este nuevo enfoque TAVI.
Los pacientes (hombres/mujeres) con una anatomía iliofemoral enferma que corresponda a los siguientes criterios podrían ser adecuados para TF-TAVI asistida por IVL (Figura 2): (1) enfermedad vascular iliofemoral con una longitud de lesión de <20 mm y un arco de calcio de ±270°, con un diámetro de luz mínimo de >3,0 mm, (2) enfermedad vascular iliofemoral con una longitud de lesión de <20 mm y calcio de arco ±360°, con un diámetro mínimo de luz de >4,0 mm, (3) enfermedad vascular iliofemoral con una longitud de lesión de >20 mm y un arco de calcio de ±270°, con un diámetro de luz mínimo de >3,5 mm, y (4) enfermedad vascular iliofemoral con una longitud de lesión de >20 mm y calcio de arco ±360°, con un diámetro de luz mínimo de >4,5 mm. Estas recomendaciones se basan en la opinión de expertos y en la práctica local.
Protocolo
El protocolo está aprobado por el comité de ética de investigación en humanos del Hospital Universitario de Copenhague, y los estudios se realizan siguiendo las directrices de dicho comité de ética. Siguiendo las políticas locales, todos los pacientes dieron su consentimiento informado para el procedimiento TAVI, la tomografía computarizada cardíaca y los datos anónimos para la investigación.
1. Planificación previa al procedimiento
- Inspeccione los vasos aorta-iliofemorales que van desde la válvula aórtica, pasando por el arco aórtico, hasta la arteria femoral común (AFC) y la bifurcación femoral. Para una evaluación precisa, realice una angiografía por tomografía computarizada (TC)específica 14 y realice una reconstrucción tridimensional (3D) basada en angiografía utilizando un software específico15 (consulte la Tabla de materiales).
- Evaluar visualmente el grado de tortuosidad de los vasos.
- Evaluar visualmente el grado y la cantidad de calcificación de los vasos (arco, morfología, etc.)16. Preste especial atención a las manchas calcificadas con una circunferencia calcificada de >270°.
- Mida el diámetro luminal mínimo (MLD), el diámetro luminal máximo y el diámetro luminal medio en el sitio de las calcificaciones y estenosis más críticas16.
- Decidir sobre la factibilidad de un enfoque de TF para TAVI. Evaluar la necesidad y el beneficio de un abordaje de TF asistido por IVL. Tenga en cuenta las recomendaciones proporcionadas en la Figura 2.
- Determinar la región de interés para un posible tratamiento con IVL: bifurcación ilíaca, arteria ilíaca común y/o arteria ilíaca externa.
- Determinar el sitio preferido de acceso/punción del TAVI en referencia a la angiografía por TC previa al procedimiento; Esto se refiere a la bifurcación femoral y la cabeza del fémur.
- Decidir el diámetro y la longitud de los stents (des)cubiertos si es necesario en situaciones de rescate vascular.
2. Obtención de acceso vascular
- Aplique anestesia local inyectando ~ 10-20 mL de solución de xilocaína (10 mg / mL) en la piel y el tejido subcutáneo en el sitio de punción preferido para TAVI. Confirme el efecto de la anestesia evaluando la sensibilidad de la piel con una aguja.
- Realice una punción ecoguiada del CFA e inserte una guía de 0,035" (consulte la tabla de materiales).
NOTA: Evite una punción del CFA demasiado cerca de la bifurcación femoral, ya que esto puede complicar y comprometer la opción de colocación de un stent de rescate del CFA en caso de fallo del dispositivo de cierre vascular. Verificarlo mediante fluoroscopia. - Haga una incisión en la piel de 2-3 cm e inserte un dilatador 7 F-8 F (consulte la tabla de materiales) sobre el alambre.
- Mantenga la guía de 0.035" en la arteria y retire el dilatador 7 F-8 F. Decidir la estrategia de cierre vascular (p. ej., cierre con sutura, cierre con tapón, etc.) y realizar maniobras previas al cierre si es necesario.
- Inserte la funda 7 F-8 F (consulte la Tabla de materiales) sobre el cable.
- Administrar heparina intravenosa según el protocolo local (p. ej., 100 UI/kg).
3. Uso y posicionamiento de un cable de seguridad
- En una intervención percutánea en un sitio tratado con IVL, coloque un cable de seguridad a través del sitio de acceso principal y un cable en la aorta abdominal. Mantenga estrictamente este cable incluso después de la retracción del sistema TAVI y la vaina de inserción de gran diámetro.
NOTA: Si el sitio principal de acceso TAVI no está enfermo, no es absolutamente necesario colocar un cable de seguridad a través del sitio principal de la punción. - En caso de enfermedad vascular en el sitio de acceso TAVI, considere un cable de seguridad que cruce el sitio de punción principal, ya sea introducido por un acceso arterial secundario contralateral (p. ej., a través de una vaina de 6 F-8 F de largo), ipsilateral inferior o transradial. Utilice este alambre de seguridad para tratar las complicaciones vasculares en la punción y/o en los sitios tratados con IVL.
- Elija un alambre de seguridad de 0.018" (que sea lo suficientemente rígido, consulte la Tabla de materiales) para administrar balones vasculares y/o stents, si es necesario, pero con una punta flexible y no traumática. Mantenga este cable de seguridad en su lugar durante todo el procedimiento de TAVI hasta la confirmación de un buen cierre vascular.
4. Configuración del sistema IVL
- Introduzca una guía de 0.014", preferiblemente con características de soporte adicionales, en la funda 7F-8F en el sitio de acceso principal de TAVI. No empuje este alambre a través del arco aórtico.
- Encienda el generador IVL y conecte el cable conector (consulte la Tabla de materiales).
- Elija un catéter IVL de 110 cm de largo con una longitud de balón de 60 mm y diámetros que oscilan entre 3,5 y 8 mm en un sistema sobre el alambre (OTW) (consulte la Tabla de materiales).
NOTA: Hay tres puertos en el extremo distal del catéter: uno para conectar el conector IVL, otro para inflar y desinflar el balón y otro que se ajusta a la guía de 0.014". - Prepare el catéter/balón IVL siguiendo los pasos que se indican a continuación.
- Aspire 5 mL de una mezcla de contraste al 50% (ver Tabla de Materiales) y 50% de solución salina en una jeringa de 20 mL. Conéctelo al puerto de inflado/desinflado del catéter con balón.
- Tire de la jeringa para aspirar aire y reemplace este aire dentro del catéter con la mezcla de líquido en la jeringa. Repita al menos tres veces.
- Llene un dispositivo desinflador (consulte la Tabla de materiales) con un 50 % de solución salina y un 50 % de medio de contraste. Desconecte la jeringa de 20 mL y conecte el desinflador al puerto de inflado del catéter IVL con una llave de paso de tres vías en una posición intermedia, asegurándose de que no se introduzca aire en el sistema.
- Enjuague el orificio de salida de la guía en el extremo distal del catéter IVL con una solución salina.
- Envuelva el cable conector en una cubierta estéril.
- Conecte el catéter IVL de forma estéril al cable conector. Envuelva un poco de cinta adhesiva o una banda elástica alrededor de la conexión entre el catéter estéril y la cubierta estéril para evitar que se deslice.
- Presione el botón de terapia en el generador de IVL. La luz cambiará de naranja a verde.
NOTA: No presione el botón de terapia a menos que el balón esté lleno con un 50% de solución salina / 50% de medio de contraste (de lo contrario, corre el riesgo de dañar los emisores de litotricia). El sistema IVL ya está listo para su uso (Figura 1).
5. Tratamiento IVL
- Moje el balón y el eje del catéter IVL antes de insertarlo para activar el recubrimiento hidrofílico.
- Inserte el catéter IVL sobre el alambre (OTW) en la vaina 7 F-8 F (sitio de acceso principal).
- Utilice la fluoroscopia para colocar las bandas marcadoras en la región de interés.
- Infle el balón IVL a 4 atm. Documente la posición y el inflado correctos mediante fluoroscopia. Asegúrese de que no haya aire visible en el globo inflado.
- Mantenga presionado el botón de activación en el mango del conector. Mantener durante 10 s para aplicar un ciclo de 30 pulsos IVL. Los clics audibles y los destellos de luz confirmarán que la terapia se ha administrado.
- Al final de los 30 pulsos de IVL, aumente el inflado del balón IVL a 6 atm. Mantenga esta presión durante 4 s.
- Desinfle el globo y mantenga la presión negativa durante 30 segundos para asegurarse de que esté vacío. Repite esta acción dos veces más.
- Repita los pasos 5.3-5.7 durante un máximo de 10 ciclos con 30 pulsos IVL (300 pulsos en total).
- Confirme que el balón esté completamente desinflado antes de retirar el catéter IVL.
- Sustituya la guía de 0,014" por una guía de 0,018"-0,035", en función de la planificación posterior (pasos 5.11-5.12).
- Si es necesario, realice una angioplastia transluminal percutánea (ATP) adicional con un balón no distensible (p. ej., 6-8 mm).
- Asegúrese de que haya una guía rígida de 0.035" en su lugar antes de insertar la funda introductora TAVI de gran diámetro en el sitio de acceso principal.
- Continúe con el procedimiento TAVI, como de costumbre.
6. Cierre vascular después de TAVI
- Antes de retirar la funda de inserción, compruebe la posición del cable de seguridad. Tenga siempre en mente y listo en el laboratorio de cateterismo una opción de rescate para la intervención percutánea con balones y/o stents (des)cubiertos.
- Realizar el cierre vascular empleando un dispositivo de cierre vascular basado en sutura o tapón (ver Tabla de Materiales).
- Evalúa el cierre vascular con inyección de contraste, ya sea desde el sitio de acceso secundario o a través de una vaina de 6 F que reemplazó a la vaina de inserción de gran diámetro.
NOTA: Una angiografía por sustracción digital (DSA) puede ser útil para identificar mejor las posibles complicaciones vasculares17. Seleccione y use el modo DSA en su módulo y pídale al paciente que contenga la respiración mientras realiza la grabación. - Si se produce una complicación vascular, trátelo en consecuencia. Por ejemplo, colocar un stent cubierto en caso de extravasación significativa y un stent descubierto en una disección en espiral, etc.
Resultados
El tratamiento de la IVL (Figura 1) de la EAP calcificada se investigó por primera vez en el estudio europeo previo a la comercialización DISRUPT-PAD18. El estudio mostró un aumento agudo del diámetro de los vasos en 35 pacientes después del tratamiento con IVL periférica a costa de una lesión mínima de los vasos. El ensayo multicéntrico DISRUPT-PAD II19 confirmó estos hallazgos en 60 pacientes. DISRUPT PAD III20 fue diseñado como un estudio prospectivo y multicéntrico del mundo real en el que 306 pacientes fueron aleatorizados 1:1 para el tratamiento de IVL o PTA de enfermedad arterial femoropoplítea severamente calcificada. El éxito del procedimiento, definido como estenosis residual <30% sin disección limitante del flujo después de la dilatación con balón, fue mayor en el grupo de IVL que en el grupo de PTA clásico (65,8% vs. 50,4%; p = 0,01). Además, en el grupo de PTA (1,4% vs. 6,8%; p = 0,03), las disecciones limitantes del flujo ocurrieron con mayor frecuencia.
Teniendo en cuenta estos resultados prometedores, la IVL se utiliza cada vez más para permitir la administración de TF de dispositivos de gran calibre, según sea necesario en la TAVI y la reparación aórtica endovascular ((T)EVAR). En la Tabla 1 se presenta una visión general de los registros que informan sobre el uso de la IVL para facilitar el TF-TAVI 11,13,21,22. La entrega del dispositivo TAVI fue exitosa en todos los casos, con bajas tasas de complicaciones. El registro de Copenhague11 reportó la mayor serie de un solo centro hasta el momento, en la que se incluyeron y trataron 50 pacientes. La selección de los pacientes se basó en las recomendaciones de TC descritas en la Figura 2. Los 50 casos de TAVI se realizaron con éxito sin complicaciones vasculares mayores definidas por VARC-2 (Tabla 1). No se documentaron perforaciones ni roturas vasculares, y solo se produjo una disección, que se trató con un stent no cubierto. Hubo una tasa relativamente mayor de fracaso del dispositivo de cierre vascular (14%), lo que requirió el uso de un stent cubierto en 5 pacientes (10%)11. Esto subraya una vez más el grado de EAP en estos pacientes y la necesidad de una planificación previa diligente al procedimiento y el uso de medidas de seguridad durante el TAVI en esta población de pacientes.

Figura 1: Sistema IVL. (A) Los componentes del sistema IVL. (B,C) Análisis de micro-tomografía computarizada que muestra "microfisuras" en la pared vascular calcificada después del tratamiento con IVL. IVL: litotricia intravascular; OTW, over-the-wire; PTA: angioplastia transluminal percutánea. Haga clic aquí para ver una versión más grande de esta figura.
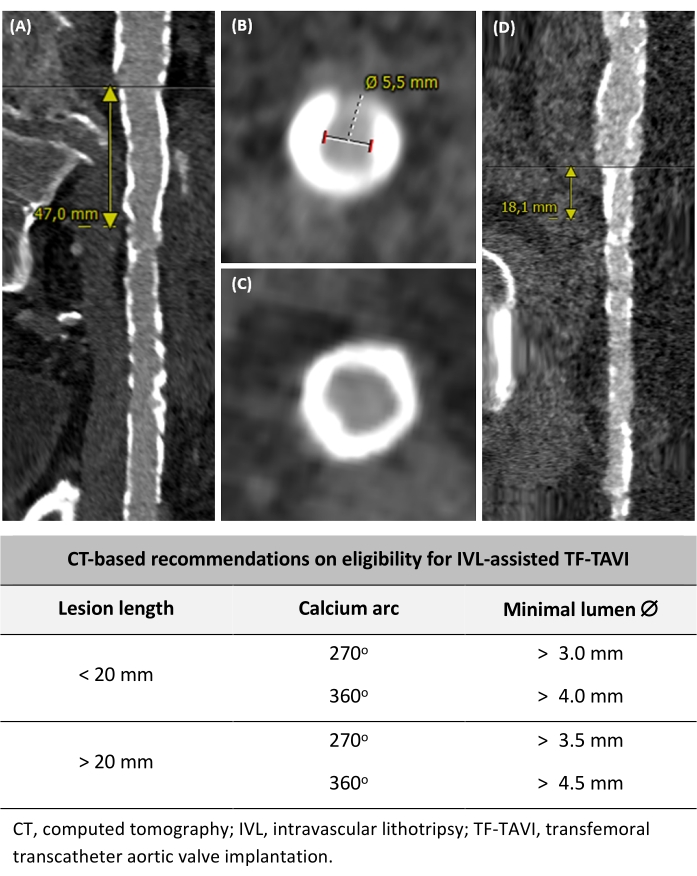
Figura 2: Determinación de la elegibilidad para TF-TAVI asistida por IVL. (A) Segmento de vaso calcificado largo >20 mm de longitud. (B) Arco de calcio de 270° y medición del diámetro mínimo del lumen. (C) Arco circunferencial de calcio de 360°. (D) Lesión severamente calcificada pero focal de <20 mm. Sobre la base de los criterios de la TC previa al procedimiento, también se incluyen recomendaciones sobre la elegibilidad para el TF-TAVI asistido por IVL. Haga clic aquí para ver una versión más grande de esta figura.
| Sawaya et al.11 | Nardi et al.22 | Armstrong et al.21 | Price et al.13 | |
| N = 50 | N = 108 | N = 17 | N = 9 | |
| Edad | 78,3 ± 6,7 | 80,5 ± 6,2 | 72,5 ± 8,3 | 79,3 ± 9,8 |
| Tipo de procedimiento | ||||
| TAVI | 50 (100%) | 108 (100%) | 4 (24%) | 4 (44%) |
| TEVAR | - | - | - | 1 (11%) |
| EVAR | - | - | 13 (76%) | 1 (11%) |
| EVAR fenestrado | - | - | - | 3 (33%) |
| Diámetro del recipiente de referencia, mm | 8,7 ± 2,2 | 9.1 (8.3-10.0) | 8,4 ± 2,5 | N/A |
| Estenosis del diámetro del vaso, % | 55 ± 13 | 50 ± 11 | 79 ± 19 | N/A |
| Longitud de la lesión diana, mm | 37 ± 16 | 20 (12-30) | 43 ± 22 | 42 ± 31 |
| Tamaño del catéter IVL | ||||
| 5,0 x 60 mm | - | 2 (1.8%) | N/A | 0 (0) |
| 6,0 x 60 mm | - | 8 (7.1%) | N/A | 4 (40%) |
| 6,5 x 60 mm | - | 6 (5.4%) | N/A | 0 (0) |
| 7,0 x 60 mm | 50 (100%) | 96 (85.7%) | N/A | 6 (60%) |
| # pulsos por lesión | N/A | 300 (270-300) | 234 ± 144 | N/A |
| Entrega exitosa de TF | 50 (100%) | 108 (100%) | 17 (100%) | 9 (100%) |
| Complicaciones | ||||
| Perforación | 0 (0) | 0 (0) | 0 (0) | 1 (11%) |
| Ruptura | 0 (0) | 1 (0.9%) | 0 (0) | 0 (0) |
| Disección: colocación de stents | 1 (2%) | 2 (1.8%) | 0 (0) | 2 (22%) |
Tabla 1: Estudios sobre el acceso transfemoral de gran diámetro asistido por IVL. Los valores son la media ± SD o N (%). N/A, no disponible; IVL: litotricia intravascular; EVAR: reparación aórtica endovascular; TAVI: implante de válvula aórtica transcatéter; TF: transfemoral; TEVAR: reparación aórtica endovascular torácica.
Ficha complementaria 1: ¿Por qué pretender maximizar el TAVI mediante el abordaje percutáneo de la TF? Posibles ventajas de los procedimientos TAVI por abordaje transfemoral percutáneo en comparación con abordajes alternativos. TAVI: implante de válvula aórtica transcatéter; TF: transfemoral. Haga clic aquí para descargar este archivo.
Discusión
Desde la introducción del TAVI como opción de tratamiento para los pacientes con EA sintomática grave, estudios y registros han demostrado que el abordaje del TAVI por TF genera un mejor éxito en el procedimiento y menores tasas de complicaciones 3,4,23. Como resultado, la mayoría de los centros hoy en día buscan realizar la mayoría de sus procedimientos de TAVI mediante abordaje percutáneode TF 23.
La introducción de la IVL como una nueva herramienta en el arsenal de TAVI ha dado lugar a un mayor número de pacientes aptos para TF-TAVI y ofrece a los operadores la posibilidad de realizar TF-TAVI de forma más segura y eficiente en caso de EAP calcificada. En el ejemplo de Copenhague, el uso de IVL ha aumentado el porcentaje de casos de TAVI que podrían tratarse con el abordaje de TF del 90% al 95%, sin aumentar el riesgo de complicaciones vasculares7.
Al considerar la TF-TAVI asistida por IVL, la selección adecuada del paciente es de suma importancia para realizar estos casos con éxito y sin complicaciones. El grupo de Copenhague11 ha propuesto un algoritmo basado en TC que también se ha implementado con éxito en otros países nórdicos y occidentales de la UE. También es esencial entender que la aposición de la pared del globo es importante para transmitir la energía a la pared del vaso10. En la práctica del mundo real, la mayoría de los balones IVL de 6 mm-7 mm se han utilizado en el contexto de 22, ya que el diámetro exterior de los actuales sistemas de administración de TAVR/vainas introductoras es de 16 F-22 F (es decir, 5,3-7,3 mm). Sobre la base de los datos disponibles en la literatura, ya se ha demostrado que la TF-TAVI asistida por IVL es fiable, lo que da como resultado una entrega de TF 100% exitosa de los sistemas TAVI22. Esto es alentador, especialmente si se tiene en cuenta que los partos transcatéter de válvulas cardíacas (THV) más difíciles con acceso alternativo a TAVI.
Por último, se debe enfatizar que se deben tomar medidas de seguridad diligentes cuando se participan en casos desafiantes de TF-TAVI con enfermedad vascular iliofemoral severamente calcificada. Incluso los ensayos recientes de última generación con TAVI todavía muestran una incidencia de 6%-8% de complicaciones vasculares mayores24. Este riesgo solo aumenta cuando se trata a pacientes con un acceso más hostil25,26. Sin embargo, con una buena planificación previa al procedimiento y las medidas de seguridad adecuadas durante la TAVI, las tasas significativas de complicaciones vasculares pueden mantenerse cerca de cero. Existen muchas estrategias de rescate7, que se basan principalmente en un sitio de acceso secundario. Un enfoque clásico consiste en realizar un cruce desde un sitio de acceso femoral contralateral y avanzar un cable de seguridad en el vaso de acceso principal, pasando por el sitio principal de punción. Además, se puede considerar un acceso ipsilateral distal o transradial para introducir un cable de seguridad. Si se produce una complicación vascular, ya sea en el sitio de punción tratado con IVL o en el sitio principal de la punción, se puede desplegar un balón de oclusión y/o un stent (des)cubierto de manera rápida y eficiente para salvar los problemas vasculares. El uso de estas estrategias de rescate proporciona seguridad en el tratamiento de estos casos desafiantes de TF-TAVI, lo cual es imprescindible en la práctica actual, ya que la deambulación temprana y el alta al día siguiente se han vuelto más rutinarios en muchos centros TAVI27,28.
El enfoque actual adolece de ciertas limitaciones. En la actualidad, no existen directrices o instrucciones bien definidas que indiquen qué pacientes son adecuados para la TF-TAVI asistida por IVL. A partir de la experiencia en grandes centros TAVI, se ha propuesto un algoritmo basado en TC11. Sin embargo, estos valores de corte pueden ser diferentes dependiendo de la experiencia del equipo de intervención. Es esencial verificar que el equipo intervencionista tenga las habilidades y la experiencia para realizar intervenciones vasculares periféricas percutáneas y que todas las herramientas/materiales estén presentes en el laboratorio de cateterismo cuando se participe en estos casos. El tratamiento con LIV también añade un coste económico específico al procedimiento TAVI; sin embargo, se espera que el hecho de evitar la anestesia general, la necesidad de monitorización en cuidados intensivos, una herida quirúrgica y la posibilidad de una deambulación precoz29 y alta27,28 compensen (en gran medida) este costo adicional para el tratamiento de la LIV. Además, el acceso transfemoral se asocia con una menor exposición a la radiación del operador30 (Archivo Suplementario 1).
Si se considera que un paciente no es apto para TF-TAVI después de un cuidadoso análisis de angiotomografía computarizada previo al procedimiento, generalmente se considera TAVI por acceso alternativo. Sin embargo, estas estrategias son más invasivas, requieren experiencia específica, a menudo están ausentes en los centros de TAVI de menor volumen y se asocian con mayores tasas de complicaciones perioperatorias 3,4. El PTA clásico con balón también podría considerarse en pacientes con acceso iliofemoral aceptable en el límite para TF-TAVI. Esta estrategia es menos costosa y más eficiente en el tiempo, pero también podría asociarse con una menor ganancia luminal y un mayor riesgo de complicaciones vasculares mayores16 como se informó en el DISRUPT PAD III trail20 para intervenciones por debajo de la rodilla. Se necesita más investigación sobre este tema.
Otra estrategia alternativa es utilizar la llamada técnica de "pavimentación y grieta", en la que se implantan múltiples stents cubiertos en el eje iliofemoral como una especie de "endoconductos" que provocan la ruptura controlada de los vasos de acceso y la dilatación a diámetros mayores31. La ventaja de esta técnica es que protege contra la perforación vascular extensa, la ruptura y la disección. Por otro lado, esta técnica también tiene múltiples desventajas: alto costo, riesgo de reestenosis y carácter más invasivo.
Divulgaciones
El Prof. Dr. De Backer recibió honorarios de orador de Shockwave Medical Inc. Todos los demás autores no informan de conflictos de intereses relevantes.
Agradecimientos
Los autores no tienen nada que reconocer.
Materiales
| Name | Company | Catalog Number | Comments |
| 0.014” guidewire | Floppy II Extra Support Guide Wire, Abbott, USA | 22299M | |
| 0.035’’ stiff guidewire | Amplatz superstiff j-tip 7 cm floppy, Boston Scientific, USA | M001465020 | |
| 20 mL syringe | |||
| 6 F or 8 F femoral sheat | Radifocus Introducer II, Terumo | RS*B70N10MRD and RS*B80N10MRD | |
| 6-8 F Arrow sheat 35 cm- if contralateral access | Teleflex | CL07635 and CL07835 | |
| Arterial puncture needle | Percutaneous entry thinwall needle, Cook Medical | SDN18-18-7.0 | |
| Contrast solution | Visipaque 350, GE Healthcare | ||
| CT angiography-based 3D reconstruction dedicated software | 3mensio, Pie Medical, The Netherlands | ||
| Diagnostic catheter | 6F IMA diagnostic catheter, Cordis | 534-6605 | |
| Echo probe sterile cover | CIV-flex transducer cover, CIVCO | 610-1212 | |
| Indeflator device (20 mL) | Everest 30, Medtronic | AC3200 | |
| IVL Connector Cable | Shockwave medical | IVLCC | |
| IVL generator | Shockwave medical | IVLGCC | |
| Local anesthetic | Xylocain 10 mg/mL, Aspen | ||
| Non-compliant balloon | Z-MED II balloon 6 to 8 mm, Numed Canada inc. | PDZ622 | |
| Safety wire | 0.018’’ Platinum Plus guidewire, Boston Scientific, USA | M0014666050 | |
| Shockwave M5/M5+ catheter (7 mm-8 mm diameter) | Shockwave medical | M5IVL7060 - M5PIVL7060 - M5PIVL8060 | |
| Standard J-wire | angiodyn guide wire j-tip, B. Braun | 5050200 | |
| Sterile cover for shockwave connector cable | camera drape, Mönlycke health care | ||
| Three-way stopcock | |||
| Unfractionated heparin | 10 mL vials of 1000 IE/mL, Amgros I/S | ||
| Vascular closure device | Perclose Prostyle device, Abbott, USA | 12773-02 | |
| Vascular echo probe | |||
| Manta VCD, Essential Medical, USA | 2156NE, 2115NE |
Referencias
- Mack, M. J., et al. Transcatheter aortic-valve replacement with a balloon-expandable valve in low-risk patients. The New England Journal of Medicine. 380 (18), 1695-1705 (2019).
- Popma, J. J., et al. Transcatheter aortic-valve replacement with a self-expanding valve in low-risk patients. New England Journal of Medicine. 380 (18), 1706-1715 (2019).
- Blackstone, E. H., et al. Propensity-matched comparisons of clinical outcomes after transapical or transfemoral transcatheter aortic valve replacement. A placement of aortic transcatheter valves (PARTNER)-I trial substudy. Circulation. 131 (22), 1989-1999 (2015).
- Siontis, G. C. M., et al. Transcatheter aortic valve implantation vs. surgical aortic valve replacement for treatment of severe aortic stenosis: a meta-analysis of randomized trials. European Heart Journal. 37 (47), 3503-3512 (2016).
- Vahanian, A., et al. 2021 ESC/EACTS Guidelines for the management of valvular heart disease. European Heart Journal. 43 (7), 561-632 (2021).
- Ueshima, D., et al. The impact of pre-existing peripheral artery disease on transcatheter aortic valve implantation outcomes: A systematic review and meta-analysis. Catheterization and Cardiovascular Interventions. 95 (5), 993-1000 (2020).
- Costa, G., Bieliauskas, G., Fukutomi, M., Ihlemann, N., Søndergaard, L., De Backer, O. Feasibility and safety of a fully percutaneous transcatheter aortic valve replacement program. Catheterization and Cardiovascular Interventions. 97 (3), 418-424 (2021).
- Cleveland, R. O., McAteer, J. A. Chapter 38, The physics of shock wave lithotripsy. Smith's Textbook on Endourology. 1, 529-558 (2007).
- Dini, C. S., et al. Intravascular lithotripsy for calcific coronary and peripheral artery stenoses. EuroIntervention. 15 (8), 714-721 (2019).
- Kereiakes, D. J., et al. Principles of intravascular lithotripsy for calcific plaque modification. JACC: Cardiovascular Interventions. 14 (12), 1275-1292 (2021).
- Sawaya, F. J., et al. Intravascular lithotripsy-assisted transfemoral TAVI: The Copenhagen experience and literature review. Frontiers in Cardiovascular Medicine. 8, 1-7 (2021).
- Nardi, G., et al. Peripheral intravascular lithotripsy to facilitate transfemoral TAVR: a multicentric prospective registry. European Heart Journal. 42, 1-11 (2021).
- Price, L. Z., Safir, S. R., Faries, P. L., McKinsey, J. F., Tang, G. H. L., Tadros, R. O. Shockwave lithotripsy facilitates large-bore vascular access through calcified arteries. Journal of Vascular Surgery Cases and Innovative Techniques. 7 (1), 164-170 (2021).
- Blanke, P., et al. Computed Tomography Imaging in the context of Transcatheter Aortic Valve Implantation (TAVI)/Transcatheter Aortic Valve Replacement (TAVR): An expert consensus document of the Society of Cardiovascular Computed Tomography. JACC: Cardiovascular Imaging. 12 (1), 1-24 (2019).
- Okuyama, K., et al. Transfemoral access assessment for transcatheter aortic valve replacement: evidence-based application of computed tomography over invasive angiography. Circulation Cardiovascular Imaging. 8 (1), 001995(2015).
- Staniloae, C. S., et al. Systematic transfemoral transarterial transcatheter aortic valve replacement in hostile vascular access. Structural Heart. 3 (1), 34-40 (2019).
- El-Mawardy, M., et al. Impact of femoral artery puncture using digital subtraction angiography and road mapping on vascular and bleeding complications after transfemoral transcatheter aortic valve implantation. EuroIntervention. 12 (13), 1667-1673 (2017).
- Marianne, B., et al. Safety and performance of lithoplasty for treatment of calcified peripheral artery lesions. Journal of the American College of Cardiology. 70 (7), 908-910 (2017).
- Brodmann, M., et al. Primary outcomes and mechanism of action of intravascular lithotripsy in calcified, femoropopliteal lesions: Results of Disrupt PAD II. Catheterization and cardiovascular interventions Official journal of the Society for Cardiac Angiography & Interventions. 93 (2), 335-342 (2019).
- Tepe, G., et al. Intravascular lithotripsy for peripheral artery calcification: 30-day outcomes from the randomized Disrupt PAD III Trial. JACC: Cardiovascular Interventions. 14 (12), 1352-1361 (2021).
- Armstrong, E. J., et al. Intravascular lithotripsy for treatment of calcified, stenotic iliac arteries: a cohort analysis from the Disrupt PAD III Study. Cardiovascular revascularization medicine including molecular interventions. 21 (10), 1262-1268 (2020).
- Nardi, G., et al. Peripheral intravascular lithotripsy of iliofemoral arteries to facilitate transfemoral TAVI: a multicentre prospective registry. EuroIntervention. , (2021).
- Carroll, J. D., et al. STS-ACC TVT Registry of transcatheter aortic valve replacement. Journal of the American College of Cardiology. 76 (21), 2492-2516 (2020).
- Scarsini, R., et al. Impact of complications during transfemoral transcatheter aortic valve replacement: How can they be avoided and managed. Journal of the American Heart Association. 8 (18), 013801(2019).
- Hayashida, K., et al. Transfemoral aortic valve implantation new criteria to predict vascular complications. JACC. Cardiovascular interventions. 4 (8), 851-858 (2011).
- Stefan, T., et al. Percutaneous aortic valve replacement. Journal of the American College of Cardiology. 59 (2), 113-118 (2012).
- Barbanti, M., et al. Optimising patient discharge management after transfemoral transcatheter aortic valve implantation: the multicentre European FAST-TAVI trial. EuroIntervention. 15 (2), 147-154 (2019).
- Wood, D. A., et al. The vancouver 3M (multidisciplinary, multimodality, but minimalist) clinical pathway facilitates safe next-day discharge home at low-, medium-, and high-volume transfemoral transcatheter aortic valve replacement centers. JACC: Cardiovascular Interventions. 12 (5), 459-469 (2019).
- Vendrik, J., et al. Early mobilisation after transfemoral transcatheter aortic valve implantation: results of the MobiTAVI trial. Netherlands Heart Journal: Monthly journal of the Netherlands Society of Cardiology and the Netherlands Heart Foundation. 28 (5), 240-248 (2020).
- Aquino, A., et al. Radiation exposure during transcatheter valve replacement: what cardiac surgeons need to know. The Annals of Thoracic Surgery. 109 (1), 118-122 (2020).
- Asciutto, G., Aronici, M., Resch, T., Sonesson, B., Kristmundsson, T., Dias, N. V. Endoconduits with "Pave and Crack" technique avoid open ilio-femoral conduits with sustainable mid-term results. European Journal of Vascular and Endovascular Surgery. 54 (4), 472-479 (2017).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoExplorar más artículos
This article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados