Method Article
تحسين الجراحة بمساعدة المنظار الصدري لعلاج أورام العمود الفقري الصدري النقيلي
In This Article
Summary
هنا ، نقدم بروتوكولا لإثبات الجراحة المحسنة بمساعدة المنظار الصدري لعلاج أورام العمود الفقري الصدرية النقيلية.
Abstract
أدى التقدم الكبير المحرز في تشخيص الأورام الخبيثة وعلاجها إلى تحسين معدلات بقاء المرضى. ومع ذلك ، فإن الانتشار النقيلي لهذه الأورام إلى الفقرات الصدرية لا يزال يمثل تحديا كبيرا ، وغالبا ما يؤدي إلى أحداث ضارة متعلقة بالعظام ، مثل الكسور المرضية والمضاعفات الشديدة. لمعالجة هذه المشكلة ، تم استكشاف نهج متعدد التخصصات ، والذي يستخدم تقنيات تنظير الصدر لاستئصال الورم والتدخلات الشوكية. توفر تقنيات تنظير الصدر بديلا طفيفا التوغل للطرق الجراحية التقليدية المفتوحة ، بهدف تقليل الصدمة الإجمالية التي يعاني منها المرضى. من خلال الاستفادة من مزايا تنظير الصدر ، يمكن للأطباء استئصال الأورام النقيلية بشكل فعال داخل الفقرات الصدرية مع تقليل التأثير على الأنسجة والهياكل المحيطة. هذا النهج ، جنبا إلى جنب مع التدخلات الشوكية المستهدفة ، لديه القدرة على تحسين نتائج المرضى ونوعية حياتهم من خلال التخفيف من الآثار المنهكة للكسور المرضية والمضاعفات الأخرى المرتبطة بأمراض العظام النقيلية. يمثل تنفيذ هذه الاستراتيجية متعددة التخصصات ، التي تتضمن استئصال الورم بالمنظار الصدري وتدخلات العمود الفقري ، وسيلة واعدة لإدارة الأورام النقيلية داخل الفقرات الصدرية. من الضروري إجراء مزيد من البحث والتقييم السريري لتوضيح الفوائد طويلة الأجل بشكل كامل ووضع بروتوكولات العلاج المثلى لهذه المجموعة من المرضى ، مما يعزز في النهاية الرعاية والنتائج للأفراد المصابين بهذه الحالة الصعبة.
Introduction
مع استمرار التقدم في تشخيص وعلاج الأورام الخبيثة ، زادت معدلات البقاء على قيد الحياة للمرضى الذين يعانون من الأورام الخبيثة بشكل كبير1. ومع ذلك ، فقد لوحظ ارتفاع مصاحب في حدوث الأحداث الضائرة المرتبطة بالعظام الناجمة عن الأورام الخبيثة ، وخاصة النقائل إلى الفقرات الصدرية2. يعاني العديد من المرضى الذين يعانون من نقائل عظمية واسعة النطاق ، وخاصة أولئك الذين يعانون من إصابة الفقرات الصدرية ، بكسور مرضية تؤدي إلى ألم شديد وحتى شلل3.
تتطلب الإجراءات المفتوحة شقوقا جلدية كبيرة وتشريحا واسعا للعضلات ، مما يؤدي إلى صدمة جراحية كبيرة وأوقات تعافي طويلة للمريض. ترتبط هذه العمليات المفتوحة أيضا بفقدان الدم بشكل أكبر ، لأنها تنطوي على تلف الأوعية الدموية الرئيسية ، مما يزيد من المخاطر الجراحيةالإجمالية 4. بالإضافة إلى ذلك ، فإن الصدمات الواسعة التي تحدث أثناء العمليات الجراحية المفتوحة ترفع من معدلات مضاعفات ما بعد الجراحة ، مثل مشاكل الرئة وتجلط الأوردة العميقة. تؤدي فترة التعافي المطولة بعد الإجراءات المفتوحة أيضا إلى إطالة مدة الإقامة في المستشفى ، مما يفرض عبئا كبيرا على كل من المرضى ومقدمي الرعاية لهم. علاوة على ذلك ، فإن المجال البصري المحدود الذي توفره العمليات الجراحية المفتوحة يجعل من الصعب تحديد المناطق المريضة واستئصالها بدقة ، مما يزيد من الصعوبة الفنية للعملية5.
في عام 1993 ، أبلغ الطبيب الألماني ماك لأول مرة عن جراحة العمود الفقري بالمنظار الصدري ، تلاه روزنتال من الولايات المتحدة في عام 1994 ، الذي أبلغ عن استئصال القرص الفقري الصدري بالمنظار6. يستخدم هذا النهج تقنيات تنظير الصدر الراسخة لإنشاء قناة ، مما يتيح استئصال الورم ، وتخفيف ضغط الحبل الشوكي ، وزرع الجسم الفقري الاصطناعي ، والتثبيت باستخدام مسامير العمود الفقري الصدري. تتميز هذه التقنية بالحد الأدنى من الصدمات وتقليل النزيف وتقليل الألم بعد الجراحة. تشمل جراحة العمود الفقري بمساعدة المنظار العديد من الإجراءات ، بما في ذلك إطلاق العمود الفقري المحدب الجانبي ، واستئصال القرص الفقري ، وخزعة الجسم الفقري ، وتصريف خراج القرص الفقري ، وجراحة الاندماج الأمامي7. أبلغ بعض الباحثين عن استخدام المناظير الجراحية المجهرية لإعادة بناء العمود الفقري الأمامي للصدر والصدر القطني والإفراج الأمامي والاندماج في علاج الأورام النقيلية والكسور والتشوهات8.
ينبع الأساس المنطقي وراء تطوير واستخدام هذه التقنية من زيادة حدوث الأحداث الضائرة المتعلقة بالعظام ، وخاصة الكسور المرضية ، الناجمة عن الانتشار النقيلي للأورام الخبيثة إلى الفقرات الصدرية8. يمكن أن تؤدي هذه المضاعفات إلى ألم شديد وشلل وانخفاض كبير في نوعية حياة المرضى المصابين. بالمقارنة مع الطرق الجراحية التقليدية المفتوحة ، يوفر نهج تنظير الصدر العديد من المزايا ، بما في ذلك الحد الأدنى من الصدمات ، وتقليل النزيف ، وتقليل الألم بعدالجراحة 9. تم الإبلاغ عن هذه التقنية ، التي تتضمن إنشاء قناة لاستئصال الورم ، وتخفيف ضغط الحبل الشوكي ، وزرع الجسم الفقري الاصطناعي ، والتثبيت بمسامير العمود الفقري الصدري ، لتكون فعالة في علاج أمراض العمود الفقري المختلفة ، مثل الأورام النقيلية والكسور والتشوهات10.
يقع استخدام تقنيات تنظير الصدر لإدارة الأورام النقيلية في الفقرات الصدرية في السياق الأوسع للتقدم في تشخيص وعلاج الأورام الخبيثة ، مما أدى إلى تحسين معدلات بقاء المريضعلى قيد الحياة 1. ومع ذلك ، فإن التحدي المستمر لمرض العظام النقيلي ، لا سيما في العمود الفقري الصدري ، استلزم استكشاف مناهج مبتكرة طفيفة التوغل لمعالجة هذه المشكلة السريرية. تقدم هذه المقالة سلسلة حالات من 40 مريضا خضعوا لجراحة بالمنظار الصدري للأورام النقيلية في الفقرات الصدرية ، مما يوفر للأطباء رؤى قيمة حول فعالية هذه التقنية وقابليتها للتطبيق المحتمل. الهدف العام من هذه الدراسة هو استكشاف استخدام نهج متعدد التخصصات ، يتضمن تقنيات تنظير الصدر لاستئصال الورم والتدخلات الشوكية ، في إدارة الأورام النقيلية داخل الفقرات الصدرية
Protocol
تم الحصول على موافقة خطية مستنيرة من المرضى للنشر. يلتزم هذا البروتوكول الجراحي بالمعايير الأخلاقية التي وضعتها لجنة الأخلاقيات في المستشفى الأول التابع ، كلية الطب بجامعة تشجيانغ (رقم المنحة: IIT20240869A).
1. تقييم ما قبل الجراحة
- استخدم معايير التضمين التالية: المشاركون الذين تبلغ أعمارهم 18 عاما فما فوق. التشخيص المؤكد للأورام الفقرية الصدرية النقيلية باستخدام التصوير (التصوير بالرنين المغناطيسي ، التصوير المقطعي المحوسب) والخزعة. يجب أن يكون الورم موجودا داخل الفقرات الصدرية ، T1-T12 ؛ يجب أن يكون لدى المشاركين حالة أداء تشير إلى أنهم لائقون للجراحة ؛ يجب على المشاركين تقديم موافقة مستنيرة للخضوع لعملية جراحية كجزء من الدراسة.
- استخدم معايير الاستبعاد التالية: المشاركون الذين يعانون من ورم خبيث واسع الانتشار خارج المنطقة الإقليمية للفقرات الصدرية ؛ الحالات الطبية المتزامنة الشديدة مثل مرض السكري غير المنضبط واضطرابات القلب والأوعية الدموية والفشل الكلوي أو الكبدي ، مما قد يزيد من خطر الجراحة ؛ بسبب المخاطر المحتملة على الجنين ، سيتم استبعاد النساء الحوامل. المشاركون السابقون في جراحة العمود الفقري الذين خضعوا سابقا لعملية جراحية في نفس موقع الورم الفقري الصدري الحالي ؛ الالتهابات الجهازية النشطة أو الالتهابات الموضعية في موقع الجراحة ، لأنها قد تعقد النتائج الجراحية ؛ قد يتم استبعاد المرضى الذين يقل متوسط العمر المتوقع لديهم عن 3 أشهر ، بناء على تقييم الطبيب ؛ المشاركون الذين خضعوا لعلاجات سابقة مثل العلاج الإشعاعي أو العلاج الكيميائي. الحساسية أو ردود الفعل السلبية للمواد أو الأدوية المستخدمة أثناء الإقامة في المستشفى. المرضى الذين خضعوا لعمليات جراحية سابقة في الصدر أو صدمات أو معدية قد تسببت في التصاقات جنبية.
- قم بإجراء تصوير قياسي للعمود الفقري جنبا إلى جنب مع الصور الشعاعية الأمامية والخلفية والجانبية للصدر لتقييم أي مشكلة محتملة في الجنبة.
- عرض العمود الفقري الأمامي الخلفي (AP): اطلب من المريض الوقوف في مواجهة جهاز الأشعة السينية ، مع وضع الذراعين بشكل طبيعي على الجانبين. ارفع الذقن قليلا لتمديد العمود الفقري العنقي. قم بمحاذاة خط الوسط مع نقطة منتصف القص. اطلب من المريض أن يحبس أنفاسه في نهاية الإلهام.
- منظر الصدر الجانبي: اطلب من المريض الاستلقاء مع توجيه الجانب الأيسر لجهاز الأشعة السينية ورفع الذراعين فوق الرأس. تأكد من بقاء الجسم في وضع مستقيم والكتفين مسترخيين. محاذاة خط الوسط على مستوى الفقرة الصدرية 4. اطلب من المريض أن يحبس أنفاسه في نهاية الإلهام
- بدء العلاج بالستيرويد للمرضى الذين يعانون من انضغاط الحبل الشوكي المصحوبة بأعراض: جرعة البداية النموذجية هي 10-16 مجم. بعد الجرعة الأولية ، قم بتوفير جرعة صيانة 4-6 مجم كل 4-6 ساعات. قم بتقليل الجرعة تدريجيا على مدى عدة أيام إلى أسابيع ، اعتمادا على استجابة المريض.
- تقييم المرضى الذين لديهم درجات توكوهاشي عالية ودرجات توميتا منخفضة ولكن دون تدخل جذور القوس الفقري والزوائد.
ملاحظة: درجة توكوهاشي هي نظام تسجيل تنبؤي مصمم للتنبؤ بالبقاء على قيد الحياة لدى المرضى الذين يعانون من أورام العمود الفقري النقيلية. تصنف درجة توكوهاشي المنقحة المرضى إلى ثلاث مجموعات تنبؤية: أولئك الذين حصلوا على درجات 0-8 (أقل من 6 أشهر من البقاء على قيد الحياة) ، و 9-11 (6-12 شهرا من البقاء على قيد الحياة) ، و 12-15 (أكثر من 12 شهرا من البقاء على قيد الحياة) 11. درجة توميتا هي أداة تنبؤية تستخدم لتقييم المرضى الذين يعانون من نقائل العمود الفقري ، مما يساعد في اختيار الاستراتيجيات الجراحية المناسبة. يعين الدرجات بناء على عوامل مثل معدل نمو الورم الأولي ، ووجود النقائل الحشوية وقابليتها للاستئصال ، وعدد النقائل العظمية. تساعد النتيجة الإجمالية الأطباء على تصنيف المرضى إلى مجموعات تنبؤية مختلفة ، وتوجيه القرارات بشأن ما إذا كانوا سيتابعون الجراحة الجذرية أو الجراحة التلطيفية أو العلاجالمحافظ 12. - ضع في اعتبارك الانصمام قبل الجراحة للمرضى الذين يعانون من أورام شديدة الأوعية الدموية. تحديد المرضى الذين خضعوا لعمليات جراحية سابقة في الصدر أو الصدمات أو المعدية التي قد تكون تسببت في التصاقات جنبية.
- استبعاد جراحة تنظير الصدر في المرضى الذين يعانون من حالات رئوية شديدة ، مثل مرض الانسداد الرئوي المزمن أو الربو ، والتي قد تعقد التهوية أحادية الرئة.
2. تخدير المريض ووضعه
- ابدأ تحريض التخدير عن طريق الوصول إلى الوريد وإعطاء الأكسجين عالي التركيز من خلال قناع الوجه لزيادة احتياطيات الأكسجين. بعد ذلك ، قم بحقن عوامل التخدير عن طريق الوريد (مثل البروبوفول 20 مجم / مل) ، والمسكنات (مثل الفنتانيل 50 ميكروغرام / مل) ، ومرخيات العضلات (مثل الروكورونيوم 10 مجم / مل).
- بمجرد أن يفقد المريض وعيه ، اختر الحجم والجانب المناسبين (اليسار أو اليمين) لأنبوب القصبة الهوائية مزدوج التجويف (DLT) بناء على الإجراء. إجراء تنظير الحنجرة المباشر أو تنظير الحنجرة بالفيديو لتصور الأحبال الصوتية. أدخل DLT من خلال الحبال الصوتية مع تجويف الشعب الهوائية متجها للأمام تقدم الأنبوب حتى تشعر بمقاومة طفيفة ، عادة عند 28-30 سم عند الأسنان. تضخيم الكفة القصبية.
- ضع المريض بشكل جانبي وقم بتثبيته بأشرطة تثبيت على طاولة العمليات ، مما يضمن أمان مجرى الهواء للمريض. ادعم رأس المريض ورقبته برفق. اقلب جسم المريض ببطء إلى الجانب ، بدءا من الكتفين ثم الوركين. حافظ على وضع الاستلقاء الجانبي مع تعرض الصدر وثني الساقين والأطراف العلوية الممتدة للأمام (الشكل 1).
- حافظ على محاذاة العمود الفقري وتجنب أي حركات التواء. ضع وسادة بين الركبتين والذراعين للحصول على الدعم. تحقق من العناصر الحيوية للمريض ومستوى الراحة لتجنب الضغط أو المحاذاة غير المبررة. قم بتوصيل أحزمة التثبيت حول كتفي المريض وفخذيه لمنع الحركة.
- استخدم التنظير الفلوري للذراع C لتأكيد محاذاة العمود الفقري: ضع التنظير الفلوري للذراع C للحصول على AP والمناظر الجانبية للعمود الفقري. تأكد من محاذاة العمود الفقري عن طريق التحقق من توسيط العمليات الشائكة بين العنقيق في طريقة عرض AP.
3. الوصول الجراحي والرؤية
- قم بإعداد سكين العظام بالموجات فوق الصوتية والأدوات الجراحية الأخرى لاستخدامها لاحقا.
- تحديد مواقع الموانئ الاستراتيجية حول الموقع المتأثر لضمان معالجة الأجهزة وسحبها على النحو الأمثل. يتم إجراء شق الأدوات الجراحية في المساحاتالوربية 3و 5 و 7 على طول الخط الإبطي الأمامي ، وكذلك فيالفضاء الوربي 7 على طول الخط الأوسط الإبطي (الشكل 2).
- جهز جدار الصدر لتبديل محتمل لفتح بضع الصدر. بعد التأكد من الحاجة إلى التحول إلى نهج مفتوح ، قم بنقل المريض بعناية إلى وضع الاستلقاء الجانبي إذا كان الوصول إلى العمود الفقري الصدري الجانبي أو الأمامي مطلوبا. إذا كانت هناك حاجة إلى الوصول الخلفي ، فحافظ على وضعية الانبطاح ولكن تأكد من محاذاة المريض بشكل صحيح. إذا لزم الأمر ، تابع بحذر عند إنشاء البوابات لمنع الإصابة.
4. الإجراء الجراحي
- إنشاء منافذ وصول: قم بعمل شق صغير بمشرط (1-2 سم) لمنفذ الكاميرا في المساحة الوربية 7 والخط الأوسط الإبطي. أدخل منظار الصدر من خلال هذا المنفذ وتأكد من رؤية واضحة للتجويف الصدري. قم بإنشاء منافذ عمل إضافية ، عادة اثنان أو ثلاثة ، في المساحات الوربية 3 و 5. اضبط المواضع الدقيقة بناء على موقع الورم والتشريح.
- تفريغ الرئة: قم بتفجير الرئة على الجانب الجراحي باستخدام تهوية الرئة المفردة لتوفير مجال جراحي واضح. تأكد من انكماش الرئة الكافي من خلال الفحص البصري من خلال منظار الصدر.
- كشف الورم: قم بتشريح غشاء الجنب الجداري الذي يغطي الأجسام الفقرية والورم بعناية باستخدام مقص ومقبض بالمنظار. تحديد وحماية الهياكل التشريحية المهمة مثل الشريان الأورطي والمريء والسلسلة الودي والأوعية المقطعية.
- استئصال الورم: قم بتشريح الورم من الأنسجة المحيطة باستخدام مزيج من تقنيات التشريح الحادة والحادة. إذا كان الورم ملتصقا بالأم الجافية أو الحبل الشوكي ، فاستخدم أدوات دقيقة وحساسة لتحريره بعناية. كن حذرا من إتلاف الحبل الشوكي أو الهياكل العصبية المحيطة.
- إزالة الورم: أمسك الورم وإزالته في أجزاء (الشكل 3). افحص هوامش الاستئصال باستمرار لضمان الإزالة الكاملة للورم. الحصول على عينات لعلم الأمراض أثناء الجراحة.
- تحضير مساحة القرص: استخدم المكشطات ، والرونجور ، والشفط لتنظيف وإزالة الفراغ الفقري ، وإزالة أي أنسجة ورم متبقية أو مادة نخرية أو بقايا قرص. جهز الصفائح النهائية للفقرات لوضع جسم فقري اصطناعي. تأكد من أن سطح الألواح الطرفية أملس وخالي من المخالفات. الهدف هو إنشاء سطح موحد ومستو لتعزيز الاتصال الأمثل بجسم العمود الفقري الاصطناعي. احرص على عدم إتلاف العظم تحت الغضروف.
- ضع الجسم الفقري الاصطناعي: اختر جسما فقريا اصطناعيا بحجم مناسب يتناسب مع أبعاد الجسم الفقري المقطوع. أدخل الجسم الفقري الاصطناعي في مساحة القرص المعدة. تأكد من ملاءمته بشكل آمن واستعادة ارتفاع ومحاذاة العمود الفقري.
- تأمين الغرسة: تأكد من الموضع الصحيح ومحاذاة الجسم الفقري الاصطناعي باستخدام التصوير التنظيري الفلوري.
- ضع أجهزة دمج العمود الفقري وتأمينها: أدخل مسامير وقضبان عنيق أعلى وأسفل موقع الاستئصال والزرع. قم بتأمين هذه الأجهزة لتثبيت العمود الفقري ، والتحقق يدويا من أي حركة أو عدم استقرار في البناء. تأكد من المحاذاة والتثبيت المناسبين باستخدام التصوير الفلوري ، مع التأكد من أن مسامير وقضبان العنق في مكانها بشكل آمن واستقرار العمود الفقري.
- تحقيق الإرقاء: السيطرة على أي نزيف من فراش الورم أو الفضاء الفقري أو الأنسجة المحيطة باستخدام الكي ثنائي القطب أو عوامل مرقئ أو الغرز. تأكد من خلو المجال الجراحي من النزيف المفرط قبل الشروع في الإغلاق.
- أعد نفخ الرئة وأغلقها: أعد نفخ الرئة ببطء أثناء التحقق من تسرب الهواء عبر منظار الصدر. ضع أنبوب صدر عبر أحد مواقع المنفذ للسماح بالتصريف بعد الجراحة وإعادة تمدد الرئة. قم بإزالة منظار الصدر والأدوات الأخرى وأغلق مواقع المنفذ بخيوط أو دبابيس بحجم 4-0.
5. إدارة ما بعد الجراحة
- المراقبة: نقل المريض إلى غرفة الإنعاش أو وحدة العناية المركزة (ICU) لمراقبة العلامات الحيوية ووظيفة الجهاز التنفسي والحالة العصبية عن كثب. راقب المضاعفات مثل النزيف أو العدوى أو ضيق التنفس.
- إدارة الألم: ابدأ بروتوكول إدارة الألم ، والذي يتضمن المواد الأفيونية عن طريق الوريد والمسكنات غير الأفيونية والمسكنات التي يتحكم فيها المريض (PCA).
- إدارة أنبوب الصدر: مراقبة إخراج أنبوب الصدر ، والانتقال إلى ختم الماء عند انتفاخ الرئة المستقر ، والاستعداد للإزالة عندما ينخفض الإنتاج إلى أقل من 100 مل / يوم ، عادة بحلول اليومالثاني بعد الجراحة. احصل على AP وعرض الصدر الجانبي قبل وبعد إزالة أنبوب الصدر للتحقق من إعادة تمدد الرئة واستبعاد استرواح الصدر.
- التنقل وإعادة التأهيل: تشجيع التعبئة المبكرة عندما يكون المريض مستقرا من الناحية الديناميكية الدموية ، مع وجود علامات حيوية ضمن الحدود الطبيعية. يمكن أن يساعد ذلك في منع المضاعفات مثل تجلط الأوردة العميقة (DVT) والانسداد الرئوي (PE). اعمل مع أخصائيي العلاج الطبيعي لتصميم خطة إعادة تأهيل مصممة خصيصا تتضمن تمارين لطيفة لتحسين الحركة والقوة.
- التغذية: تعزيز نظام غذائي متوازن غني بالبروتينات والفيتامينات والمعادن لدعم الشفاء واندماج العظام. شجع على الترطيب واتباع نظام غذائي غني بالألياف لمنع الإمساك ، خاصة إذا كان المريض يتناول مسكنات الألم الأفيونية.
- النشاط ونمط الحياة: ينصح المريض بتجنب رفع الأشياء الثقيلة أو الانحناء أو حركات الالتواء التي يمكن أن تجهد العمود الفقري. شجع التمارين المنتظمة واللطيفة مثل المشي أو السباحة أو التمارين الرياضية منخفضة التأثير للحفاظ على الصحة العامة ودعم تعافي العمود الفقري.
النتائج
تتضمن بيانات المريض درجة توكوهاشي قبل الجراحة ، ودرجة توميتا قبل الجراحة ، ودرجة مقياس التناظر البصري (VAS) قبل الجراحة ، ودرجة VAS بعد الجراحة. ويبين الجدول 1 التحليل الإحصائي. تم تحليل درجات VAS بعد الجراحة وVAS قبل الجراحة باستخدام اختبارات t المقترنة. تشير نتائج البيانات إلى أن الأفراد الذين يخضعون لإجراء محسن بمساعدة تنظير الصدر يظهرون انخفاضا كبيرا في درجة VAS الخاصة بهم (الشكل 4). يجب تقييم حالة استئصال ورم العمود الفقري وإعادة بنائه من خلال متابعة ما بعد الجراحة (الشكل 5).
شملت الدراسة مجموعة من 40 مريضا تتراوح أعمارهم بين 63 و 78 عاما. أظهرت درجة توكوهاشي قبل الجراحة ، ودرجة توميتا قبل الجراحة ، ودرجة VAS قبل الجراحة ، ودرجة VAS بعد الجراحة نطاقا يتراوح بين 11.5 ± 2.8 و 5.5 ± 1.2 و 6.0 ± 1.4 و 1.5 ± 1.2 في درجات تقييم المرضى. تظهر درجة VAS تباينا ذا دلالة إحصائية بين تقييمات ما قبل الجراحة وبعدها.
أشارت درجة توكوهاشي ، بمتوسط 11.5 ± 2.8 ، إلى أن معظم المرضى كانوا بصحة جيدة إلى جيدة ، حيث تم تصنيف 40٪ على أنهم يتمتعون بصحة جيدة و 60٪ على أنهم عادلون. كانت السيطرة على الورم جزئية في الغالب ، حيث حقق 50٪ تحكما جزئيا و 30٪ حققوا السيطرة الكاملة. كان استقرار العمود الفقري شائعا ، حيث كان 80٪ من المرضى لديهم أشواك مستقرة. كان لدى جميع المرضى موقع نقيلي واحد بسبب طبيعة الجزء الواحد للأورام ، وكان لدى 70٪ أنواع سرطان أولية مواتية. أظهرت نقاط توميتا ، بمتوسط 5.5 ± 1.2 ، انقساما متساويا في حالة الأداء ، حيث تم تصنيف 50٪ على أنها جيدة و 50٪ على أنها سيئة. من الناحية النسيجية ، كان لدى 65٪ من المرضى أنواع مواتية. تعكس هذه النتائج مجموعة من المرضى مع ظروف مواتية بشكل عام للتدخل الجراحي ، بما في ذلك المرض الذي يمكن التحكم فيه والصحة الجيدة بشكل عام.

الشكل 1: وضع المرضى الذين يخضعون للجراحة. صورة توضح الوضع الصحيح للمريض لجراحة تنظير الصدر ، عادة في وضع الاستلقاء الجانبي ، مع حشوة ودعامات مناسبة لتأمين المريض. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.

الشكل 2: شقوق للأدوات الجراحية. يتم إجراء شق الأدوات الجراحية في الفراغات الوربية الثالثة والخامسة والسابعة على طول الخط الإبطي الأمامي ، وكذلك في الفضاء الوربي السابع على طول الخط الأوسط الإبطي. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
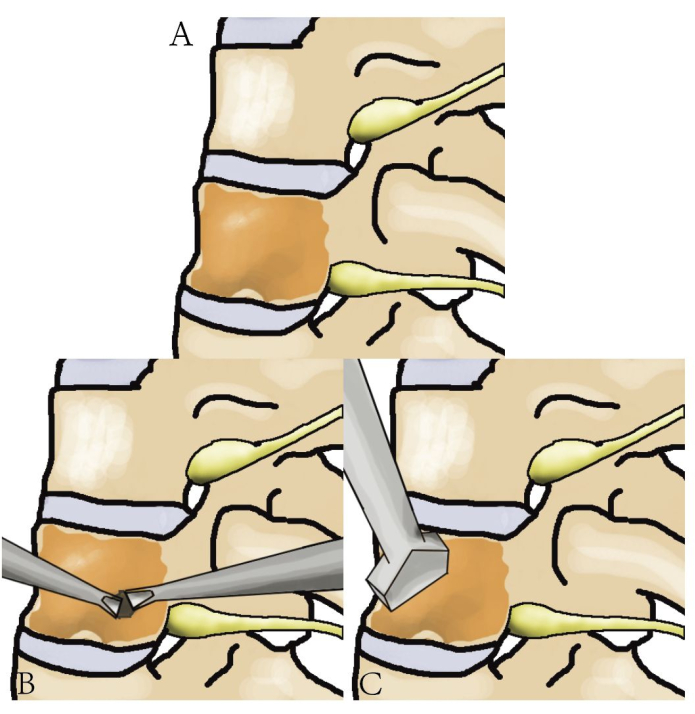
الشكل 3: رسم تخطيطي لاستئصال ورم العمود الفقري الصدري. رسم تخطيطي مفصل يوضح العمود الفقري الصدري والورم والخطوات المتبعة في استئصال الورم. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
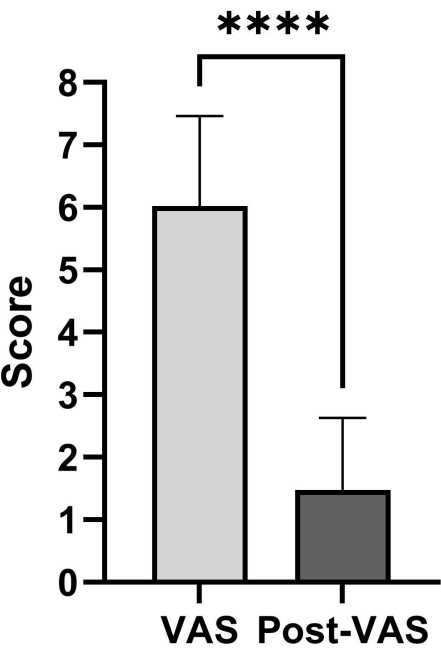
الشكل 4: مقارنة بين درجات VAS بعد الجراحة وما قبل الجراحة. هناك تفاوت يعتد به إحصائيا بين تقييمات VAS قبل الجراحة وبعدها. تقدم البيانات متوسط ± الانحراف المعياري. تم تحليل الدرجات باستخدام اختبارات t المقترنة. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
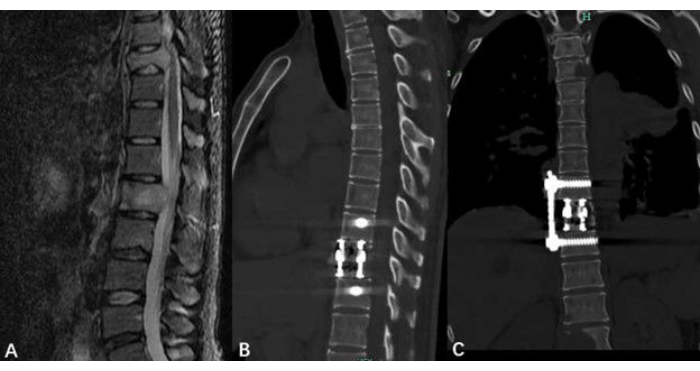
الشكل 5: تصوير أورام العمود الفقري الصدري. (أ) أشار التصوير بالرنين المغناطيسي قبل الجراحة إلى ورم العمود الفقري الصدري. (ب ، ج) صور لفحص التصوير المقطعي المحوسب بعد الجراحة تظهر العمود الفقري الصدري بعد استئصال الورم وأي أجهزة مزروعة. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
| مجموعة | درجة توكوهاشي | نتيجة توميتا | درجة VAS قبل الجراحة | درجة VAS بعد الجراحة | العمر (سنوات) |
| TAS (ن = 40) | 11.5 ± 2.8 | 5.5 ± 1.2 | 6.0 ± 1.4 | 1.5 ± 1.2 | 70.8 ± 4.7 |
الجدول 1: درجات تقييم المريض. وعرضت البيانات العددية كمتوسط ± انحراف معياري (متوسط ± SD). اختصار: TAS = الجراحة بمساعدة المنظار.
Discussion
تشمل عيوب الجراحة المفتوحة شقوق أكبر وندبات أطول ، مما يؤدي إلى اضطراب أكبر في الأنسجة وزيادة ألم ما بعدالجراحة 13. غالبا ما يؤدي هذا النهج إلى زيادة فقدان الدم أثناء الإجراء ويزيد من خطر الإصابة بالعدوى والمضاعفات بسبب التعرض الأوسع نطاقا. يعاني المرضى من أوقات تعافي أطول ، وإقامة طويلة في المستشفى ، وتأخر العودة إلى الأنشطة العادية. بالإضافة إلى ذلك ، فإن الجراحة المفتوحة لها تأثير أكبر على وظائف الرئة ، مما يزيد من خطر حدوث مضاعفات تنفسية بعد الجراحة. بشكل عام ، بينما توفر الجراحة المفتوحة رؤية ممتازة ومساحة عمل ، إلا أنها تأتي مع أعباء أعلى من الصدمات والتعافي14.
تمثل الجراحة المعززة بمساعدة المنظار الصدري لإدارة أورام العمود الفقري الصدري النقيلي تقدما كبيرا في مجال العمليات الجراحية طفيفة التوغل.
تشمل مزاياه التصور الممتاز للهياكل التشريحية الحرجة ، والحد الأدنى من الصدمات للأنسجة الطبيعية ، وتقليل آلام ما بعد الجراحة ، والإقامة في المستشفى لفترة أقصر ، وانخفاض حدوث المضاعفات. ومع ذلك ، فإن هذه التقنية لها قيود معينة يجب الاعتراف بها. يتطلب مستوى عال من الكفاءة الفنية ، مما يتطلب من الجراحين امتلاك مهارات متقدمة في كل من جراحة الصدر وإجراءات العمود الفقري. بالإضافة إلى ذلك ، بالمقارنة مع الجراحة المفتوحة ، قد يحد النهج بمساعدة المنظار الصدري من الرؤية المباشرة والجس للورم ، مما قد يؤثر على تأكيد الاستئصال الكامل15. علاوة على ذلك ، فإن قابلية تطبيق هذه الطريقة مقيدة بحجم الورم وموقعه. قد لا تكون الأورام الكبيرة بشكل استثنائي أو تلك التي تمتد إلى ما وراء الحدود التشريحية المحددة قابلة لهذه التقنية.
أحد العناصر الحاسمة في البروتوكول الجراحي بمساعدة المنظار الصدري هو التخطيط الدقيق قبل الجراحة ، بما في ذلك استخدام تقنيات التصوير لتحديد موقع الورم ومداه بدقة. يعد تحقيق الوضع الأمثل للمريض لضمان أقصى قدر من الوصول إلى الفقرات الصدرية أمرا بالغ الأهمية لنجاح الجراحة. علاوة على ذلك ، فإن التشريح الدقيق والحفاظ على الهياكل الحيوية المحيطة مع ضمان الاستئصال الكامل للورم هو توازن دقيق يتطلب مهارات جراحية متخصصة.
خلال تنفيذ هذا البروتوكول ، قد يواجه الجراحون تحديات مختلفة تستلزم تعديل التقنية. على سبيل المثال ، في الحالات التي تنطوي على تورط واسع النطاق في الأوعية الدموية ، قد تكون هناك حاجة إلى دعم إضافي داخل الأوعية الدموية لإدارة النزيف المحتمل. يمكن أن يتضمن استكشاف الأخطاء وإصلاحها أثناء الجراحة استخدام أدوات متخصصة أو ضبط زاوية الدخول لتعزيز المجال البصري. تمكن القدرة على التكيف المتأصلة في هذا البروتوكول الجراحين من تصميم مناهجهم للحالات الفردية ، وبالتالي تحسين نتائج المرضى.
يمثل تطبيق الجراحة المعززة بمساعدة المنظار الصدري تقدما كبيرا على العمليات الجراحية المفتوحة التقليدية والتقنيات السابقة طفيفة التوغل. بالمقارنة مع بضع الصدر المفتوح ، فإن نهجنا يوفر تقليل المراضة ، وتقليل آلام ما بعد الجراحة ، وتقصير أوقات الشفاء. حتى عند مقارنتها بالأساليب الأخرى طفيفة التوغل ، فإن الطريقة الموضحة في هذه الدراسة توفر ظروفا مريحة فائقة للجراحين ودقة أعلى محتملة بسبب التصور المحسن الذي يسهله التكبير بالمنظارالصدري 15.
تحمل التقنية الجراحية المعززة بمساعدة المنظار الصدري أهمية كبيرة في مجال أبحاث الأورام ، لا سيما بالنسبة للتحقيقات التي تركز على جراحة الأورام وإدارة ورم خبيث في العمودالفقري 16. من خلال تمكين الإزالة طفيفة التوغل لأورام العمود الفقري الصدرية النقيلية ، يوفر هذا البروتوكول منصة لاستكشاف العلاجات المساعدة مثل العلاج الكيميائي أثناء الجراحة أو العلاج الإشعاعي. بالإضافة إلى ذلك ، فإنه يسهل التحقيق في نتائج المرضى المتعلقة بنوعية حياة ما بعد الجراحة ، مع الأخذ في الاعتبار تقليل الصدمات وربما استئناف الأنشطة اليومية بشكل أسرع. هذه التقنية لديها القدرة على تعزيز مناهج الطب الشخصي من خلال السماح بتعديل الخطة الجراحية بناء على التشريح الخاص بالمريض وخصائص الورم المستمدة من طرق التصوير المتقدمة.
Disclosures
ويعلن أصحاب البلاغ عدم وجود تضارب في المصالح.
Acknowledgements
لا ينطبق.
Materials
| Name | Company | Catalog Number | Comments |
| Absorbable sutures | ETHICON | VCP739D | Johnson & Johnson 2-0 Absorbable Suture for suturing incisions |
| anesthesia drug | Anlibang Pharmaceuticals | propofol injectable emulsion | Sedation used in anesthesia procedures |
| anterior fixation system | Medtronic | VANTAGE | Medtronic's Vertebral Lateral Fixation System can be used to fixate the adjacent vertebral bodies to the implanted artificial vertebral body from the lateral side of the vertebrae, creating a stable overall structure. |
| Artificial vertebral body | Stryker | VLIFT | Stryker Artificial Vertebral Body is used for implanting an artificial vertebral body prosthesis after the removal of a diseased vertebra to support the spine. |
| C-arm | GE | OEC One CFD | Used for intraoperative fluoroscopic confirmation of the proper positioning of metal implants. |
| Thoracoscope System | stryker | Precision Ideal Eyes HD | Used for imaging of visceral organs within the thoracic cavity to facilitate the surgical manipulation of pathological structures. |
| Ultrasonic bone knife | SMTP | XD860A | Used for intraoperative cutting of bone tissue. |
References
- Rosmini, S., et al. Cardiac computed tomography in cardio-oncology: an update on recent clinical applications. Eur Heart J Cardiovas Imaging. 22 (4), 397-405 (2021).
- Li, Y., et al. Distinct metabolism of bone marrow adipocytes and their role in bone metastasis. Front Endocrinol. 13, 902033 (2022).
- Bianchi, G., Ghobrial, I. M. Does my patient with a serum monoclonal spike have multiple myeloma. Hematol/Oncol Clinics North Am. 26 (2), 383-393 (2012).
- Choi, J. Y., Park, S. M., Kim, H. J., Yeom, J. S. Recent updates on minimally invasive spine surgery: Techniques, technologies, and indications. Asian Spine J. 16 (6), 1013-1021 (2022).
- Zhu, X., et al. A comparative study between minimally invasive spine surgery and traditional open surgery for patients with spinal metastasis. Spine. 46 (1), 62-68 (2021).
- Kuklo, T. R., Lenke, L. G. Thoracoscopic spine surgery: current indications and techniques. Ortho Nurs. 19 (6), 15-22 (2000).
- Roque, D., Cabral, D., Rodrigues, C., Simas, N. Extradural thoracic nerve root hemangioblastoma approached by a combined posterior thoracic spine and video-assisted thoracoscopic surgery: A case report. Surg Neurol Int. 13 (10), (2022).
- Hanna, G., Kim, T. T., Uddin, S. A., Ross, L., Johnson, J. P. Video-assisted thoracoscopic image-guided spine surgery: evolution of 19 years of experience, from endoscopy to fully integrated 3D navigation. Neurosurg Focus. 50 (1), E8 (2021).
- Johnson, J. P., Drazin, D., King, W. A., Kim, T. T. Image-guided navigation and video-assisted thoracoscopic spine surgery: the second generation. Neurosurg Focus. 36 (3), E8 (2014).
- Ragel, B. T., Amini, A., Schmidt, M. H. Thoracoscopic vertebral body replacement with an expandable cage after ventral spinal canal decompression. Neurosurg. 61 (5 Suppl 2), 317-322 (2007).
- Tokuhashi, Y., Uei, H., Oshima, M., Ajiro, Y. Scoring system for prediction of metastatic spine tumor prognosis. World J Ortho. 5 (3), 262-271 (2014).
- Mezei, T., et al. A novel prognostication system for spinal metastasis patients based on network science and correlation analysis. Clin Oncol. 35 (1), e20-e29 (2023).
- Zhu, X., et al. A comparative study between minimally invasive spine surgery and traditional open surgery for patients with spinal metastasis. Spine. 46 (1), 62-68 (2021).
- Qiu, J., et al. Novel technique for endoscopic-assisted nipple-sparing mastectomy and immediate breast reconstruction with endoscopic-assisted latissimus dorsi muscle flap harvest through a single axillary incision: a retrospective cohort study of comparing endoscopic and open surgery. Gland Surg. 11 (8), 1383-1394 (2022).
- Haoran, E., et al. Perioperative outcomes comparison of robotic and video-assisted thoracoscopic thymectomy for thymic epithelial tumor: a single-center experience. Updates Surg. , (2023).
- Maki, R., et al. Minimally invasive robot-assisted thoracoscopic surgery for mediastinal tumor. Kyobu geka. Japan J Thoracic Surg. 76 (7), 506-509 (2023).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved