Method Article
Comparação do desempenho preditivo de três sistemas de estadiamento linfonodal no carcinoma colorretal de células do anel de sinete com base no modelo de aprendizado de máquina
* Estes autores contribuíram igualmente
Neste Artigo
Resumo
Este estudo avalia sistemas prognósticos para pacientes com carcinoma de células em anel de sinete colorretal usando modelos de aprendizado de máquina e análises de risco concorrentes. Ele identifica as chances logarítmicas de linfonodos positivos como um preditor superior em comparação com o estadiamento pN, demonstrando forte desempenho preditivo e auxiliando na tomada de decisões clínicas por meio de ferramentas robustas de previsão de sobrevida.
Resumo
O status dos linfonodos é um preditor prognóstico crítico para os pacientes; no entanto, o prognóstico do carcinoma colorretal de células em anel de sinete (SRCC) tem recebido atenção limitada. Este estudo investiga a capacidade preditiva prognóstica das chances logarítmicas de linfonodos positivos (LODDS), razão linfonodal (LNR) e estadiamento pN em pacientes com SRCC usando modelos de aprendizado de máquina (Random Forest, XGBoost e Neural Network) juntamente com modelos de risco concorrentes. Os dados relevantes foram extraídos do banco de dados Surveillance, Epidemiology, and End Results (SEER). Para os modelos de aprendizado de máquina, os fatores prognósticos para a sobrevida específica do câncer (CSS) foram identificados por meio de análises de regressão de Cox univariadas e multivariadas, seguidas pela aplicação de três métodos de aprendizado de máquina - XGBoost, RF e NN - para determinar o sistema ideal de estadiamento linfonodal. No modelo de risco competitivo, análises de risco competitivas univariadas e multivariadas foram empregadas para identificar fatores prognósticos, e um nomograma foi construído para prever o prognóstico de pacientes com CCRE. A área sob a curva característica de operação do receptor (AUC-ROC) e as curvas de calibração foram utilizadas para avaliar o desempenho do modelo. Um total de 2.409 pacientes com CEC foram incluídos neste estudo. Para validar a eficácia do modelo, uma coorte adicional de 15.122 pacientes com câncer colorretal, excluindo casos de SRCC, foi incluída para validação externa. Tanto os modelos de aprendizado de máquina quanto o nomograma de risco concorrente exibiram forte desempenho na previsão de resultados de sobrevida. Em comparação com o estadiamento pN, os sistemas de estadiamento LODDS demonstraram capacidade prognóstica superior. Após a avaliação, os modelos de aprendizado de máquina e os modelos de risco concorrentes alcançaram excelente desempenho preditivo caracterizado por boa discriminação, calibração e interpretabilidade. Nossos achados podem ajudar a informar a tomada de decisão clínica para os pacientes.
Introdução
O câncer colorretal (CCR) é o terceiro tumor maligno mais prevalente globalmente 1,2,3. O carcinoma de células em anel de sinete (CEC), um subtipo raro de CCR, compreende aproximadamente 1% dos casos e é caracterizado por mucina intracelular abundante deslocando o núcleo celular 1,2,4. O CEC é frequentemente associado a pacientes mais jovens, tem maior prevalência em mulheres e tem estágios tumorais avançados no momento do diagnóstico. Em comparação com o adenocarcinoma colorretal, o CEC apresenta menor diferenciação, maior risco de metástase à distância e sobrevida em 5 anos de apenas 12%-20%5,6. O desenvolvimento de um modelo prognóstico preciso e eficaz para o SRCC é crucial para otimizar as estratégias de tratamento e melhorar os resultados clínicos.
Este estudo tem como objetivo construir um modelo prognóstico robusto para pacientes com SRCC usando abordagens estatísticas avançadas, incluindo aprendizado de máquina (ML) e modelos de risco concorrentes. Essas metodologias podem acomodar relacionamentos complexos em dados clínicos, oferecendo avaliações de risco individualizadas e superando os métodos tradicionais em precisão preditiva. Modelos de aprendizado de máquina, como Random Forest, XGBoost e Neural Networks, se destacam no processamento de dados de alta dimensão e na identificação de padrões intrincados. Estudos mostraram que os modelos de IA preveem efetivamente os resultados de sobrevida no câncer colorretal, enfatizando o potencial do ML em aplicações clínicas 7,8. Complementando o ML, os modelos de risco concorrentes abordam vários tipos de eventos, como mortalidade específica por câncer versus outras causas de morte, para refinar a análise de sobrevida. Ao contrário dos métodos tradicionais, como o estimador de Kaplan-Meier, os modelos de risco competitivo estimam com precisão a probabilidade marginal de eventos na presença de riscos concorrentes, fornecendo avaliações de sobrevida mais precisas8. A integração de ML e análise de risco competitivo melhora o desempenho preditivo, oferecendo uma estrutura poderosa para ferramentas de prognóstico personalizadas no SRCC 9,10,11.
A metástase linfonodal influencia significativamente o prognóstico e a recorrência em pacientes com CCR. Embora a avaliação em estágio N na classificação TNM seja crítica, o exame inadequado dos linfonodos - relatado em 48% a 63% dos casos - pode levar à subestimação da doença. Para resolver isso, foram introduzidas abordagens alternativas, como a razão de linfonodos (LNR) e as chances logarítmicas de linfonodos positivos (LODDS). O LNR, a razão entre linfonodos positivos (PLNs) e linfonodos totais (TLNs), é menos afetado pela contagem de TLN e serve como um fator prognóstico no CCR. LODDS, a razão logarítmica de PLNs para linfonodos negativos (NLNs), mostrou capacidade preditiva superior tanto no SRCC gástrico quanto no câncer colorretal10,11. O aprendizado de máquina tem sido cada vez mais aplicado em oncologia, com modelos que melhoram a estratificação de risco e as previsões prognósticas em vários tipos de câncer, incluindo câncer de mama, próstata e pulmão 12,13,14. No entanto, sua aplicação no CEC colorretal permanece limitada.
Este estudo procura preencher essa lacuna integrando LODDS com ML e modelos de risco concorrentes para criar uma ferramenta de prognóstico abrangente. Ao avaliar o valor prognóstico do LODDS e alavancar técnicas preditivas avançadas, esta pesquisa visa melhorar a tomada de decisões clínicas e melhorar os resultados para pacientes com SRCC.
Protocolo
Este estudo não se refere à aprovação ética e consentimento para participar. Os dados utilizados neste estudo foram obtidos de bancos de dados. Incluímos pacientes diagnosticados com carcinoma colorretal de células em anel de sinete de 2004 a 2015, bem como outros tipos de câncer colorretal. Os critérios de exclusão incluíram pacientes com tempo de sobrevida inferior a um mês, aqueles com informações clínico-patológicas incompletas e casos em que a causa da morte não era clara ou não especificada.
1. Aquisição de dados
- Baixar SEER. Obtenha o software de estatísticas 8.4.3 no site do banco de dados SEER (http://seer.cancer.gov/about/overview.html). Depois de fazer login no software, clique em Sessão de lista de casos > Dados e selecione o banco de dados Incidence SEER Research Plus Data, 17 Registries, Nov 2021 Sub (2000-2019).
- Clique em Seleção > Editar e escolha {Raça, Sexo, Ano Dx. Ano do diagnóstico} = '2004', '2005', '2006', '2007', '2008', '2009', '2010', '2011', '2012', '2013', '2014', '2015' E {Local e Morfologia. Recodificação do site CID-O-3/OMS 2008} = '8490/3'.
- Em seguida, clique em Tabela e, na interface de variáveis disponíveis, selecione Recodificação de idade com idades únicas e 100+, Sexo, Conjugal, Recodificação de local CID-O-3/OMS 2008, Tamanho do tumor CS, Regional nodes_examined (1988+), Regional nodes_positive (1988+), Grupo de estágios AJCC derivado, 6ª ed (2004-2015), AJCC derivado T, 6ª ed (2004-2015), AJCC derivado N, 6ª ed (2004-2015), AJCC M derivado, 6ª ed (2004-2015), CEA, Recodificação de radiação, Recodificação de quimioterapia (sim, não/desconhecido), Classificação de morte específica por causa SEER, Recodificação do estado vital (corte de estudo usado), Meses de sobrevida, Ano do diagnóstico.
- Por fim, clique em Saída, nomeie os dados e clique em Executar para gerar e salvar os dados. O processo de inclusão detalhado é mostrado na Figura 1.
- Baixe dados de pacientes com câncer colorretal, excluindo casos de SRCC, para validação externa subsequente. Clique em Seleção > Editar e escolha {Raça, Sexo, Ano Dx. Ano do diagnóstico} = '2004', '2005', '2006', '2007', '2008', '2009', '2010', '2011', '2012', '2013', '2014', '2015' E {Local Primário - rotulado} = 'C18-C20'. Repita as etapas 1.3 e 1.4 para obter informações clínico-patológicas e excluir amostras com {Site e Morfologia. Recodificação do site CID-O-3/OMS 2008} = '8490/3' do arquivo baixado.
- Para fins comparativos, processe várias variáveis. Classifique o status dos linfonodos usando a razão dos linfonodos (LNR) e o logaritmo das chances de linfonodos positivos (LODDS).
- Defina LNR como a proporção de linfonodos positivos (PLNs) para linfonodos totais (TLNs). Calcule o valor LODDS usando a fórmula:
loge(número de PLNs + 0,5) / (número de linfonodos negativos (NLNs) + 0,5)
onde 0,5 foi adicionado para evitar um resultado infinito. Os valores de corte para LNR, LODDS e tamanho do tumor foram determinados usando o software X-tile (versão 3.6.1) com base no método do valor mínimo de P.
- Defina LNR como a proporção de linfonodos positivos (PLNs) para linfonodos totais (TLNs). Calcule o valor LODDS usando a fórmula:
- Abra o software X-tile, clique em Arquivo > Abrir e selecione o arquivo de dados para importá-lo para o software. Depois que os dados forem carregados, mapeie as variáveis: Censor corresponde ao status de sobrevivência, Tempo de sobrevivência corresponde ao tempo de sobrevivência e Marker1 é a variável a ser analisada, garantindo que os dados correspondam corretamente.
- Em seguida, clique em Do > Kaplan-Meier > Marker1 para realizar a análise de sobrevida de Kaplan-Meier e gerar a curva de sobrevida. Com base na separação das curvas de sobrevida de Kaplan-Meier, significância estatística (por exemplo, valor de p) e relevância clínica, determine o valor de corte ideal e, finalmente, registre ou exporte os resultados da análise.
- Divida o LNR em três grupos: LNR 1 (≤0,16), LNR 2 (0,16 - 0,78) e LNR 3 (≥ 0,78). Categorize os pacientes em três grupos com base no LODDS: LODDS 1 (≤ -1,44), LODDS 2 (-1,44 - 0,86) e LODDS 3 (≥ 0,86).
- Classifique o tamanho do tumor em três categorias: ≤ 3,5 cm, 3,5 - 5,5 cm e ≥ 5,5 cm. Converta a idade de uma variável contínua para uma variável categórica. Categorize a idade dos pacientes no momento do diagnóstico inicial em ≥60 anos e <60 anos. Classifique a localização do tumor com base na distribuição dos tumores de carcinoma de células em anel de sinete (SRCC) como cólon direito, cólon esquerdo e reto. O cólon direito inclui o ceco, o cólon ascendente, a flexura hepática e o cólon transverso, enquanto o cólon esquerdo inclui a flexura esplênica, o cólon descendente, o cólon sigmóide e a junção retossigmoide.
- Para este estudo, atribua aleatoriamente um total de 2409 dados de pacientes elegíveis com SRCC a uma coorte de treinamento (N = 1686) e uma coorte de validação (N = 723) em uma proporção de 7:3. Use o código a seguir para divisão aleatória e data.csv de origem do banco de dados SEER. Os arquivos gerados após a divisão aleatória serão usados para análise posterior.
biblioteca (acento circunflexo)
Dados <- read.csv("data.csv")
set.seed(123)
train_indices <- createDataPartition(dados$variável, p = 0,7, lista = FALSO)
train_data <- dados[train_indices, ]
test_data <- dados[-train_indices, ]
write.csv(train_data, "traindata.csv", row.names = FALSE)
write.csv(test_data, "testdata.csv", row.names = FALSE)
2. Desenvolvimento e verificação de modelos de ML
- Baixe o RStudio (2024.04.2+764) e o software R (4.4.1). Abra o RStudio para executar o software R. Clique em Novo Arquivo e selecione Script R para criar uma nova interface de programação R. Insira o código relevante no editor de código e clique em Executar para executar o código.
- Use o código a seguir para filtrar as variáveis incluídas nos modelos de ML pela análise de regressão de Cox. Além disso, explore o impacto do estadiamento LODDS, LNR e pN na sobrevida específica do câncer (CSS) em pacientes com SRCC. O traindata.csv são dados obtidos do banco de dados SEER.
biblioteca ("sobrevivência")
biblioteca("survminer")
biblioteca("rms")
biblioteca("dplyr")
Dados <- read.csv("traindata.csv")
dados$tempo=as.numeric(dados$tempo)
dados$status=as.numeric(dados$status)
variáveis <- c("Sexo", "Idade", "Raça", "Conjugal", "Estágio", "T", "N", "M","Tumor_size", "LNR", "LODDS", "CEA","Radiação", "Quimioterapia", "Local")
dados <- dados %>%
mutate(across(all_of(variáveis), as.factor))
cox=coxph(Surv(tempo, status) ~ dados$T, dados = dados)
cox$coeficientes
pval=anova(cox)$Pr[2]
clean_data=dados[,c(1:12, 14:18)]
get_coxVariable=função(your_data;índice){cox_list=c() k=1
for (i em 1:index) {mod=coxph(Surv(time, status) ~ your_data[,i],data=your_data) pval=anova(mod)$Pr[2] print(pval) print(colnames(your_data)[i]) if (pval<0.05) {cox_list[k]=colnames(your_data)[i] k=k+1}}return(cox_list)}
variable_select=get_coxVariable(clean_data,15)
for(i em 1:15){print(variable_select[i])}
for (var em variable_select) {formula <- as.formula(paste("Surv(time, status) ~", var))cox_model <- coxph(formula, data = data) print(summary(cox_model))
ggforest(cox)
variáveis <- c("Sexo", "Idade", "Raça", "Conjugal", "Estágio", "T", "N", "M", "Tumor_size", "LNR", "LODDS", "Quimioterapia")
dados <- dados %>%
mutate(across(all_of(variáveis), as.factor))
cox=coxph(Surv(tempo, status) ~ Sexo+Idade+Raça+Conjugal+T+N+M+Tumor_size+LNR+
LODDS+Quimioterapia, dados = dados)
ggforest(cox,data = data)
ggplot_forest <- ggforest(cox, dados = dados) - Use o código a seguir para comparar as habilidades de previsão prognóstica de três sistemas LN (LODDS, LNR e pN staging) nas coortes de treinamento, validação e validação externa.
Biblioteca (RMS)
biblioteca (sobrevivência)
Biblioteca (Survminer)
library(riskRegression)
biblioteca(gt)
train_data <- read.csv("train_data123.csv")
validation_data <- read.csv("test_data123.csv")
DD <- distDados(train_data)
opções(distDados(DistDados= "DD")
model_LNR <- cph(Surv(tempo, status) ~ LNR, dados = train_data, x = VERDADEIRO, y = VERDADEIRO)
model_LODDS <- cph(Surv(tempo, status) ~ LODDS, dados = train_data, x = VERDADEIRO, y = VERDADEIRO)
model_pN <- cph(Surv(tempo, status) ~ N, dados = train_data, x = VERDADEIRO, y = VERDADEIRO)
calculate_performance <- function(model, data) {pred <- predict(model, newdata = data) c_index_result <- concordance(Surv(data$time, data$status) ~ pred) c_index <- c_index_result$concordance aic <- AIC(model) bic <- BIC(model) return(c(C_index = round(c_index, 3), AIC = round(aic, 2), BIC = round(bic, 2)))}
calculate_performance <- function(model, data) {pred <- predict(model, newdata = data, type = "lp") concordance_result <- concordancefit(Surv(data$time, data$status), x = pred) c_index <- concordance_result$concordance ci_lower <- c_index - 1.96 * sqrt(concordance_result$var) ci_upper <- c_index + 1.96 * sqrt(concordance_result$var) aic <- AIC(modelo) bic <- BIC(modelo) return(c(C_Index = round(c_index, 3), CI_Lower = round(ci_lower, 3), CI_Upper = round(ci_upper, 3), AIC = round(aic, 2), BIC = round(bic, 2)))}
train_LNR <- calculate_performance(model_LNR, train_data)
train_LODDS <- calculate_performance(model_LODDS, train_data)
train_pN <- calculate_performance(model_pN, train_data)
model_LNR_val <- cph(Surv(tempo, status) ~ LNR, dados = validation_data, x = VERDADEIRO, y = VERDADEIRO)
model_LODDS_val <- cph(Surv(tempo, status) ~ LODDS, dados = validation_data, x = VERDADEIRO, y = VERDADEIRO)
model_pN_val <- cph(Surv(tempo, status) ~ N, dados = validation_data, x = VERDADEIRO, y = VERDADEIRO)
val_LNR <- calculate_performance(model_LNR_val, validation_data)
val_LODDS <- calculate_performance(model_LODDS_val, validation_data)
val_pN <- calculate_performance(model_pN_val, validation_data)
resultados <- data.frame(Variável = c("LNR", "LODDS", "pN"), Training_C_Index = c(paste(train_LNR["C_Index"], "(", train_LNR["CI_Lower"], ", ", train_LNR["CI_Upper"], ")", sep = ""), paste(train_LODDS["C_Index"], "(", train_LODDS["CI_Lower"], ", ", train_LODDS["CI_Upper"], ")", sep = ""), paste(train_pN["C_Index"], "(", train_pN["CI_Lower"], ", ", train_pN["CI_Upper"], ")", sep = "")Training_AIC = c(train_LNR["AIC"], train_LODDS["AIC"], train_pN["AIC"]), Training_BIC = c(train_LNR["BIC"], train_LODDS["BIC"], train_pN["BIC"]), Validation_C_Index = c(paste(val_LNR["C_Index"], "(", val_LNR["CI_Lower"], ", ", ", val_LNR["CI_Upper"], ")", sep = ""), paste(val_LODDS["C_Index"], "(", val_LODDS["CI_Lower"], ", ", val_LODDS["CI_Upper"], ")", sep = ""), paste(val_pN["C_Index"], "(", val_pN["CI_Lower"], ", ", val_pN["CI_Upper"], ")", sep = "")), Validation_AIC = c(val_LNR["AIC"], val_LODDS["AIC"], val_pN["AIC"]), Validation_BIC = c(val_LNR["BIC"], val_LODDS["BIC"], val_pN["BIC"]))
results_table <- gt(resultados) %>%
tab_header(title = "Desempenho de previsão dos três sistemas de estadiamento linfonodal") %>%
cols_label(Variável = "Variável",Training_C_Index = "Índice C (IC 95%) (Treinamento)", Training_AIC = "AIC (Treinamento)", Training_BIC = "BIC (Treinamento)", Validation_C_Index = "Índice C (IC 95%) (Validação)", Validation_AIC = "AIC (Validação)", Validation_BIC = "BIC (Validação)")
write.csv(resultados, "prediction_performance.csv", row.names = FALSE) - Use o código a seguir para criar um modelo XGBoost e gerar gráficos de barras da importância relativa das variáveis, para comparar a importância dos três sistemas LN. Da mesma forma, gere curvas ROC e curvas de calibração. Os dados são obtidos do banco de dados SEER.
Biblioteca(xgboost)
biblioteca (acento circunflexo)
biblioteca (pROC)
train_data <- read.csv("train_data.csv")
test_data <- read.csv("test_data.csv")
train_matrix <- XGB. DMatrix(dados = as.matrix(train_data[, c('Idade', 'T', 'N', 'M', 'LODDS', 'Quimioterapia')]), rótulo = train_data$status)
test_matrix <- XGB. DMatrix(dados = as.matrix(test_data[, c('Idade', 'T', 'N', 'M', 'LODDS', 'Quimioterapia')]), rótulo = test_data$status)
params <- list(booster = "gbtree", objective = "binary:logistic", eval_metric = "auc", eta = 0,1, max_depth = 6, subsample = 0,8, colsample_bytree = 0,8)
xgb_model <- xgb.train(params = params, dados = train_matrix, nrounds = 100, watchlist= list(train = train_matrix), verbose = 1)
pred_probs <- prever(xgb_model, newdata = test_matrix)
pred_labels <- senão(pred_probs > 0,5, 1, 0)
conf_matrix <- confusionMatrix(as.factor(pred_labels), as.factor(test_data$status))
roc_curve <- roc(test_data$status, pred_probs)
auc_value <- AUC(roc_curve)
ci_auc <- ci.auc(roc_curve)
sensibilidade <- conf_matrix$byClass["Sensibilidade"]
especificidade <- conf_matrix$byClass["Especificidade"]
precisão <- conf_matrix$overall["Precisão"]
ppv <- conf_matrix$byClass["Valor Pos Pred"]
npv <- conf_matrix$byClass["Neg Pred Value"]
result_table <- data.frame(Model = "XGBoost", AUC = sprintf("%.3f (%.3f-%.3f)", auc_value, ci_auc[1], ci_auc[3]), Sensibilidade = sprintf("%.3f", sensibilidade), Especificidade = sprintf("%.3f", especificidade), Precisão = sprintf("%.3f", precisão), PPV = sprintf("%.3f", ppv), NPV = sprintf("%.3f", npv))
write.csv(result_table, "xgboost_model_performance.csv", row.names = FALSE)
roc_df <- data.frame(FPR = 1 - roc_curve$especificidades, TPR = roc_curve$sensibilidades)
roc_plot <- ggplot(roc_df, aes(x = FPR, y = TPR)) +geom_line(color = "steelblue", size = 1.2) + geom_abline(intercept = 0, slope = 1, linetype = "tracejado", color = "gray") + annotate("text", x = 0.9, y = 0.2, label = paste("AUC =", round(auc_value, 3)), size = 5, color = "black") + labs(title = "Curva ROC para o modelo XGBoost", x = "Taxa de falsos positivos", y = "Taxa de verdadeiros positivos") + theme_minimal() + theme(panel.border = element_rect(color = "black", fill = NA, tamanho = 1))
calibration_data <- data.frame(Status = as.factor(test_data$status), pred_probs = pred_probs)
calib_model <- calibração(Status ~ pred_probs, dados = calibration_data, classe = "1", cortes = 5)
ggplot(calib_model$data, aes(x = ponto médio, y = Porcentagem)) + geom_line(cor = "steelblue", tamanho = 1) + geom_point(cor = "vermelho", tamanho = 2) + geom_abline(interceptação = 0, inclinação = 1, tipo de linha = "tracejado", cor = "preto") +labs(title = "Curva de calibração para o modelo XGBoost", x = "Probabilidade prevista", y = "Proporção observada") + theme_minimal() + theme(panel.border = element_rect(cor = "preto", preenchimento = NA, tamanho = 0,5)) - Use o código a seguir para construir um modelo de RF e gerar gráficos de barras da importância relativa das variáveis, comparando assim a importância dos três sistemas LN. Da mesma forma, gere curvas ROC e curvas de calibração. Os dados são obtidos do banco de dados SEER.library(randomForest)
biblioteca (dplyr)
biblioteca(ggplot2)
biblioteca (pROC)
biblioteca (acento circunflexo)
Biblioteca (RMS)
Composição <- read.csv("train_data.csv")
Testado <- read.csv("test_data.csv")
trainset$status=factor(trainset$status)
variáveis1 <- c("Idade", "T", "N", "M", "LODDS", "Quimioterapia")
Trem < - Trem %>%
mutate(across(all_of(variables1), as.numeric))
testado$status=fator(testado$status)
Testado < - Testado %>%
mutate(across(all_of(variables1), as.numeric))
RF=randomForest(trainset$status ~ Idade + T + N + M + LODDS + Quimioterapia, data=trainset,ntree=100,importance=TRUE,proximity=TRUE)
imp=importância(RF)
varImpPlot(RF)
impvar=rownames(imp)[order(imp[,4],decrescente = TRUE)]
importance_df <- as.data.frame(imp)
importance_df$Variáveis <- rownames(importance_df)
importance_plot <- ggplot(importance_df, aes(x = reorder(Variables, MeanDecreaseAccuracy), y = MeanDecreaseAccuracy)) +geom_bar(stat = "identity", fill = "steelblue") +coord_flip() + labs(title = "Variable Importance", x = "Variables", y = "Mean Decrease Accuracy") + theme_minimal()
pred_probs <- predict(RF, conjunto de testes, tipo = "prob")[,2]
roc_obj <- roc(testset$status, pred_probs)
auc_value <- AUC(roc_obj)
roc_plot <- ggplot() +geom_line(aes(x = 1 - roc_obj$especificidades, y = roc_obj$sensibilidades), cor = "steelblue", tamanho = 1,2) +geom_abline(interceptação = 0, inclinação = 1, tipo de linha = "tracejado", cor = "cinza") + anotar("texto", x = 0,8, y = 0,2, rótulo = colar("AUC =", redondo(auc_value, 3)), cor = "preto", tamanho = 5, hjust = 0) + labs(título = "Curva ROC para Modelo de Floresta Aleatória", x = "Taxa de falsos positivos", y = "Taxa de verdadeiros positivos") +theme_minimal() + theme(panel.border = element_rect(color = "black", fill = NA, size = 1))
calibration_data <- data.frame(pred_probs = pred_probs, status = testado$status)
calib_model <- calibração(status ~ pred_probs, dados = calibration_data, classe = "1", cortes = 5)
calib_df <- as.data.frame(calib_model[["data"]])
calib_df$mid <- calib_df$midpoint
calib_df $ por cento < - calib_df $ por cento
calibration_plot <- ggplot(calib_df, aes(x = mid, y = Percent)) + geom_line(color = "steelblue", size = 1.2) + geom_point(color = "steelblue", size = 3) + geom_abline(intercept = 0, slope = 1, linetype = "tracejado", color = "black", size = 0.8) + labs(title = "Curva de calibração para floresta aleatória", x = "Probabilidade prevista", y = "Probabilidade real") + theme_minimal() + theme(panel.border = element_rect(color = "preto", fill = NA, tamanho = 1), plot.title = element_text(hjust = -0,05, vjust = -1,5, face = "negrito", tamanho = 12))
rf_probs <- predict(RF, newdata=tested, type="prob")[, 2]
rf_auc <- roc(testado$status, rf_probs)
auc_value <- AUC(rf_auc)
ci_auc <- ci.auc(rf_auc)
rf_predictions <- predict(RF, newdata=testado)
conf_matrix <- confusionMatrix(rf_predictions, testado$status)
sensibilidade <- conf_matrix$byClass["Sensibilidade"]
especificidade <- conf_matrix$byClass["Especificidade"]
precisão <- conf_matrix$overall["Precisão"]
ppv <- conf_matrix$byClass["Valor Pos Pred"]
npv <- conf_matrix$byClass["Neg Pred Value"]
result_table <- data.frame(Model = "RF", AUC = sprintf("%.3f (%.3f-%.3f)", auc_value, ci_auc[1], ci_auc[3]), Sensibilidade = sprintf("%.3f", sensibilidade), Especificidade = sprintf("%.3f", especificidade), Precisão = sprintf("%.3f", precisão), PPV = sprintf("%.3f", ppv), NPV = sprintf("%.3f", npv))
write.csv(result_table, "RF_model_performance.csv", row.names = FALSE) - Use o código a seguir para criar um modelo NN e gerar gráficos de barras da importância relativa das variáveis, comparando assim a importância dos três sistemas LN. Da mesma forma, gere curvas ROC e curvas de calibração. Os dados são obtidos do banco de dados SEER.library(nnet)
biblioteca (acento circunflexo)
biblioteca (pROC)
biblioteca(ggplot2)
train_data <- read.csv("train_data.csv")
test_data <- read.csv("test_data.csv")
train_data$status <- as.factor(train_data$status)
test_data$status <- as.factor(test_data$status)
características <- c("Idade", "T", "N", "M", "LODDS", "Quimioterapia")
x_train <- train_data[, recursos]
y_train <- train_data$status
x_test <- test_data[, recursos]
y_test <- test_data$status
nn_model <- nnet(status ~ Idade + T + N + M + LODDS + Quimioterapia, dados = train_data, tamanho = 5, decaimento = 0,01, maxit = 200)
pred_probs <- predict(nn_model, newdata = x_test, type = "raw")
pred_labels <- senão(pred_probs > 0,5, 1, 0)
roc_curve <- roc(as.numeric(y_test), pred_probs)
auc_value <- AUC(roc_curve)
auc_ci <- ci.auc(roc_curve)
auc_text <- colar0(rodada(auc_value, 3), " (", rodada(auc_ci[1], 3), "-", rodada(auc_ci[3], 3), ")")
conf_matrix <- confusionMatrix(as.factor(pred_labels), y_test)
precisão <- conf_matrix$overall["Precisão"]
sensibilidade <- conf_matrix$byClass["Sensibilidade"]
especificidade <- conf_matrix$byClass["Especificidade"]
ppv <- conf_matrix$byClass["Valor Pos Pred"]
npv <- conf_matrix$byClass["Neg Pred Value"]
performance_table <- data.frame(Métrica = c("AUC (IC 95%)", "Precisão", "Sensibilidade", "Especificidade", "PPV", "VPN"),Valor = c(auc_text, redondo(precisão, 3), redondo(sensibilidade, 3), redondo(especificidade, 3), redondo(ppv, 3), redondo(npv, 3)))
write.csv(performance_table, "NN_performance_table.csv", row.names = FALSE)
roc_curve <- roc(y_test, pred_probs)
auc_value <- AUC(roc_curve)
roc_plot <- ggplot() + geom_line(aes(x = 1 - roc_curve$especificidades, y = roc_curve$sensibilidades), cor = "steelblue", tamanho = 1,2) +geom_abline(interceptação = 0, inclinação = 1, tipo de linha = "tracejado", cor = "cinza") + anotação("texto", x = 0,8, y = 0,2, rótulo = colar("AUC =", redondo(auc_value, 3)), cor = "preto", tamanho = 5, hjust = 0) + labs(título = "Curva ROC para Modelo de Rede Neural", x = "Taxa de falsos positivos", y = "Taxa de verdadeiros positivos") + theme_minimal() + theme(panel.border = element_rect(color = "black", fill = NA, size = 1))
calibration_data <- data.frame(pred_probs = pred_probs, status = as.numeric(y_test) - 1)
calibration_data$pred_probs <- as.numeric(calibration_data$pred_probs)
calibration_data$calibration_bin <- cut(calibration_data$pred_probs, breaks = seq(0, 1, by = 0.2), include.lowest = TRUE)
calibration_summary <- aggregate(status ~ calibration_bin, dados = calibration_data, FUN = média)
calibration_summary$pred_mean <- aggregate(pred_probs ~ calibration_bin, data = calibration_data, FUN = mean)$pred_probs
calibration_plot <- ggplot(calibration_summary, aes(x = pred_mean, y = status)) + geom_line(color = "steelblue", size = 1.2) + geom_point(color = "red", size = 3) + geom_abline(intercept = 0, slope = 1, linetype = "tracejado", color = "black", size = 0.8) + labs(title = "Curva de calibração para rede neural", x = "Probabilidade prevista", y = "Probabilidade real") + theme_minimal() + theme(panel.border = element_rect(color = "preto", fill = NA, tamanho = 1))
nn_var_importance <- varImp(nn_model)
importance_df <- data.frame(Recurso = rownames(nn_var_importance), Importância = nn_var_importance$Geral )
importance_plot <- ggplot(importance_df, aes(x = reorder(Feature, Importance), y = Importance)) + geom_bar(stat = "identity", fill = "steelblue") + coord_flip() + labs(title = "Importância Variável para Rede Neural", x = "Features", y = "Importância") + theme_minimal()
3. Desenvolvimento e verificação de modelos de risco concorrentes
- Use o código a seguir para executar a análise univariada e plotar a curva da função de incidência cumulativa (CIF). O data.csv são os dados obtidos do banco de dados SEER. O método para salvar imagens subsequentes será o mesmo desta etapa. Substitua Site no código um por um por outros fatores para executar a análise univariada para todos os fatores.
biblioteca(tidycmprsk)
Biblioteca(gtResumo)
biblioteca(ggplot2)
biblioteca(ggsurvfit)
Biblioteca (ggprism)
AA <- read.csv("data.csv")
cif2 <- tidycmprsk::cuminc(Surv(time, Status1) ~Site, data = aa)
arrumado(CIF2,vezes = C(12,24,36,48,60))
tbl_cuminc(cif2, times =c(12,24,36,48,60), outcomes = c("CSS", "OSS"),estimate_fun = NULL, label_header = "**{time/12}-year cuminc**") %>%
add_p() %>%
add_n(localização = "nível")
cuminc_plot <- ggcuminc(cif2, resultado = c("CSS", "OSS"), tamanho = 1,5) + labs(x = "tempo") +add_quantile(y_value = 0,20, tamanho = 1) + scale_x_continuous(breaks = seq(0, 84, by = 12), limites = c(0, 84)) +scale_y_continuous(label = scales::p ercent, breaks = seq(0, 1, by = 0,2), limits = c(0, 1)) + theme_prism() + theme(legend.position = c(0,2, 0.8), panel.grid = element_blank(),panel.grid.major.y = element_line(cor = "grey80")) + tema(legenda.espaçamento.x = unidade(0.1, "cm"), legenda.espaçamento.y = unidade(0.01, "cm")) + tema(axis.ticks.comprimento.x = unidade(-0.2, "cm"), axis.ticks.x = element_line(cor = "preto", tamanho = 1, lineend = 1)) + tema(axis.ticks.comprimento.y = unidade(-0.2, "cm"), axis.ticks.y = element_line(cor = "preto", tamanho = 1, lineend = 1)) - Use o código a seguir para executar análise e visualização multivariadas. O data1.csv vem dos resultados do código anterior. Depois de executar o código, clique em Exportar, clique em Salvar como PDF e, finalmente, clique em Salvar para salvar a imagem.
biblioteca(tidycmprsk)
Biblioteca(gtResumo)
AA <-read.csv('data1.csv')
for (i em nomes(aa)[c(1:16, 19)]){aa[,i] <- as.factor(aa[,i])}
mul1Tabela2 <- MUL1 %>%
gtsummary::tbl_regression(exponentiate = TRUE) %>%
add_n(localização = "nível"); Tabela 2
table_df <- as_tibble(Tabela 2)
guia <- tabela2$table_body
tab1 <- tab[,c(12,19,20,22:29)] - Use o código a seguir para plotar o nomograma, a curva ROC e a curva de calibração. Depois de treinar o modelo usando dados da coorte de treinamento, use os dados de coortes de validação e validação externa para validar o model.library(QHScrnomo). Os dados da coorte externa consistem em amostras de câncer colorretal que não sejam carcinoma de células em anel, que foram selecionadas na etapa 1.4.
Biblioteca (RMS)
biblioteca(timeROC)
biblioteca (sobrevivência)
AA <-read.csv('data3.csv')
for (i em nomes(aa)[c(1:16, 19)]){aa[,i] <- as.factor(aa[,i])}
DD <- distDados(AA)
opções(distDados(DistDados= "DD")
mul <- cph(Surv(tempo, Status1 == 1) ~ T + N + M + LODDS + Site, dados = aa, x = VERDADEIRO, y = VERDADEIRO, surv = VERDADEIRO)
m3 <- crr.fit(mul, failcode = 1, cencode = 0)
nomo <-Newlabels(fit = m3, labels =c(T="T", N= "N", M = "M", LODDS = "LODDS", Site = "Site"))
nomoc("N0","N1","N2"),M=c("M0","M1"),LODDS=c
("LODDS1","LODDS2","LODDS3"),Site=
c("RSC","LSC","Reto")))
nomogram.crr(fit =nomo , lp = F, xfrac = 0.3, fun.at =seq(from=0, to=1, by= 0.1) , failtime =c(12,36,60), funlabel = c("Incidência Cumulativa de CSS de 1 ano","Incidência Cumulativa de CSS de 3 anos","Incidência Cumulativa de CSS de 5 anos"))
time_points <- c(12, 36, 60)
pred_risks_list <- lapply(time_points, function(time_point) {predict(m3, newdata = aa, type = "risk", time = time_point)})
pred_risks_df <- data.frame(do.call(cbind, pred_risks_list))
colnames(pred_risks_df) <- paste("risk_at", time_points, "meses", sep = "_")
roc_1year <- timeROC(T = aa$time, delta = ifelse(aa$Status1 == "CSS", 1, 0), marker = pred_risks_df$risk_at_12_months, cause = 1, times = 12, iid = TRUE)
roc_3year <- timeROC(T = aa$time, delta = ifelse(aa$Status1 == "CSS", 1, 0), marker = pred_risks_df$risk_at_36_months, cause = 1, times = 36, iid = TRUE)
roc_5year <- timeROC(T = aa$time, delta = ifelse(aa$Status1 == "CSS", 1, 0), marker = pred_risks_df$risk_at_60_months, cause = 1,times = 60, iid = TRUE)
legend("canto inferior direito",legenda = c("CSS de 1 ano", "CSS de 3 anos", "CSS de 5 anos"), col = c("#BF1D2D", "#262626", "#397FC7"), lwd = 2)
sas.cmprsk(m3,tempo = 36)
set.seed(123)
aa$pro <- tenf.crr(m3,tempo = 36)
cindex(prob = aa$pro, fstatus = aa$Status1, ftime = aa$time, type = "crr", failcode = 1, cencode = 0, tol = 1e-20)
groupci(x=aa$pro, ftime = aa$time, fstatus = aa$Status1, failcode = 1, cencode = 0, ci = TRUE, g = 5, m = 1000, u = 36, xlab = "Probabilidade prevista", ylab = "Probabilidade real", lty=1, lwd=2, col="#262626",xlim=c(0,1.0), ylim=c(0,1.0), add =TRUE)
Resultados
Características dos pacientes
Este estudo se concentrou em pacientes diagnosticados com CEC colorretal, usando dados do banco de dados SEER de 2004 a 2015. Os critérios de exclusão incluíram pacientes com tempo de sobrevida inferior a um mês, aqueles com informações clínico-patológicas incompletas e casos em que a causa da morte não era clara ou não especificada. Um total de 2409 pacientes com SRCC colorretal que atenderam aos critérios de inclusão foram divididos aleatoriamente em uma coorte de treinamento (N = 1686) e uma coorte de validação (N = 723). Os parâmetros demográficos e clínicos das coortes de treinamento e validação foram analisados por meio do software R, conforme apresentado na Tabela 1. Do total de pacientes incluídos, a maioria tinha mais de 60 anos, com número semelhante de pacientes do sexo masculino e feminino. A maioria dos pacientes era branca. Mais da metade dos pacientes (56%) eram casados. A maioria dos tumores foi classificada como III-IV (76%). A maioria dos pacientes (82%) apresentava tumores maiores que 3,5 centímetros, e a maioria dos pacientes pertencia ao grupo LODDS1 (42%). Em toda a coorte, uma alta proporção de pacientes (53%) recebeu quimioterapia. Os tumores primários localizavam-se principalmente no cólon direito (67%). Após a randomização, não houve diferenças significativas nas características basais entre os dois grupos estatisticamente.
Identificação dos fatores clínicos prognósticos incluídos nos modelos de ML
Primeiro, selecionamos variáveis significativas para inclusão no modelo de aprendizado de máquina usando a análise de regressão de Cox. Os resultados da regressão univariada de Cox mostraram que o tempo de sobrevida foi significativamente correlacionado com certas variáveis clínicas, incluindo sexo, idade, raça, estado civil, estadiamento AJCC, estadiamento pT, estadiamento pN, estadiamento pM, tamanho do tumor, nível de CEA, classificação LNR, classificação LODDS e se o paciente recebeu radioterapia ou quimioterapia (Tabela 2). Notavelmente, LNR, LODDS e estadiamento pN exibiram taxas de risco (HR) estatisticamente significativas, indicando que esses três sistemas de estadiamento LN estão associados ao prognóstico. A análise de regressão de Cox multivariada subsequente foi conduzida para determinar ainda mais a associação entre estadiamento pN, LODDS, LNR e CSS em pacientes com SRCC. Os resultados indicaram que LODDS, LNR e status pN afetaram significativamente o CSS de pacientes com SRCC (Figura 2).
Comparação de sistemas LN
As habilidades prognósticas preditivas dos três sistemas LN foram semelhantes nas coortes de treinamento, validação e validação externa (amostras de câncer colorretal diferente do carcinoma de células em anel, que foram selecionadas na etapa 1.4.; Tabela 3). Na coorte de treinamento, os índices C para LNR, LODDS e pN foram de 0,309, 0,308 e 0,337, respectivamente, enquanto na coorte de validação, os índices C foram de 0,288, 0,279 e 0,319, respectivamente. Na coorte de validação externa, os índices C para LNR, LODDS e pN foram 0,419, 0,420 e 0,424, respectivamente. Além disso, os valores de AIC para cada sistema na coorte de treinamento foram 12667,56, 12670,57 e 12731,89, e na coorte de validação, foram 4575,36, 4559,13 e 4613,20, respectivamente. Na coorte de validação externa, os valores de AIC para cada sistema foram os seguintes: 106554,68 para LODDS, 106581,85 para LNR e 106915,45 para estadiamento pN. Esses achados indicam que existem diferenças mínimas na qualidade discriminatória entre os três sistemas. Portanto, utilizamos métodos de aprendizado de máquina - RF, XGBoost e NN - para determinar ainda mais o sistema LN ideal em termos de capacidade preditiva. Essa análise incluiu variáveis significativas na regressão de Cox univariada e pelo menos um modelo multivariado (pN, LODDS ou LNR) para a construção dos modelos de aprendizado de máquina, incluindo pN, pT, pM, idade, raça, classificação LNR, classificação LODDS e se o paciente recebeu radioterapia ou quimioterapia.
Construímos modelos de RF, XGBoost e NN usando o conjunto de dados de treinamento. Os valores de importância para cada variável são mostrados na Figura 3. Em RF e XGBoost, o LNR exibiu a maior importância, enquanto o LODDS também demonstrou considerável importância. No entanto, no modelo NN, o LODDS apresentou melhor capacidade preditiva em comparação com pN e LNR. Considerando os resultados combinados das três abordagens de aprendizado de máquina, concluímos que o sistema LODDS pode ser o melhor sistema para avaliar o status de NL em pacientes com SRCC.
Desempenho dos modelos de ML
Conforme mostrado na Tabela 4 e na Figura 4A-C, todos os três modelos foram capazes de prever o prognóstico de forma eficaz, e as AUCs dos três modelos variaram de 0,777 a 0,851 no conjunto de dados de teste (XGBoost: AUC = 0,820, IC 95% = 0,789-0,851; FR: AUC = 0,819, IC 95% = 0,788-0,850; NN: AUC = 0,809, IC 95% = 0,777-0,841). Os modelos XGBoost, RF e NN mostraram grande especificidade (0,82, 0,825, 0,815) e acurácia (0,762, 0,763, 0,757). As curvas de calibração são mostradas na Figura 5D-F.
Construção e validação de modelo de risco competitivo
Dado que os modelos de ML não levaram em conta a influência de fatores de risco concorrentes, construímos um modelo de risco competitivo para identificar melhor o sistema LN que teve melhor desempenho em termos de capacidade preditiva. A sobrevida específica do câncer (CSS) representa a morte por câncer, enquanto a sobrevida global (OSS) é responsável pelas mortes por outras causas, servindo como eventos de risco concorrentes. Usamos modelos de risco competitivos univariados e multivariados para analisar os fatores preditivos para CSS na coorte de treinamento. O modelo de risco competitivo univariado indicou que os fatores preditivos para CSS incluíram sexo, idade, raça, estado civil, estadiamento AJCC, estadiamento TNM, tamanho do tumor, classificação LNR, classificação LODDS, nível de CEA, se o paciente recebeu radioterapia ou quimioterapia e a localização do tumor primário. Finalmente, a análise de risco competitivo multivariado, o estadiamento T, o estadiamento N, o estadiamento M, a classificação LODDS e a localização do tumor primário foram identificados como cinco marcadores prognósticos independentes para pacientes com CEC colorretal. Os resultados das análises de risco competitivo univariadas e multivariadas são apresentados na Tabela 5, e as curvas de função de incidência cumulativa (CIF) correspondentes para os fatores de risco independentes são apresentadas na Figura 5. Com base nas cinco variáveis significativas (estadiamento T, estadiamento N, estadiamento M, classificação LODDS e localização do tumor primário), desenvolvemos um nomograma prognóstico (Figura 6A). Verificou-se que, em comparação com o pN, o LODDS apresentou maior peso. Esse achado se alinha com os resultados anteriores, sugerindo que o sistema LODDS é o melhor sistema para avaliar o status de NL em pacientes com SRCC.
Para avaliar a acurácia do modelo, foram construídas curvas de calibração (Figuras 6B-D). Os resultados indicaram que o modelo teve um bom desempenho na previsão da sobrevida total dos pacientes em 1, 3 e 5 anos. O ajuste das curvas à linha de 45° demonstra uma forte consistência do modelo. Os resultados da avaliação da curva ROC para o nomograma (Figuras 5E-G) mostraram que a área sob a curva (AUC) para predições em 1, 3 e 5 anos foi maior que 0,75. Esses resultados sugerem que as curvas de predição para 3 e 5 anos demonstraram benefícios significativos, indicando que o nomograma tem aplicações clínicas valiosas e valor de referência.

Figura 1: Fluxograma apresentando o processo de triagem no banco de dados SEER. Por meio de nossos critérios de inclusão e exclusão, selecionamos com sucesso pacientes com câncer colorretal do banco de dados SEER para uma série subsequente de análises baseadas em R. Clique aqui para ver uma versão maior desta figura.

Figura 2: Associação de LNR, LODDS e estadiamento pN com CSS na coorte de treinamento. Esta figura ilustra os resultados da análise de regressão de Cox multivariada para (A) LNR, (B) LODDS e (C) estadiamento pN, avaliados juntamente com outros fatores prognósticos independentes. A análise inclui Hazard Ratios (HR) e intervalos de confiança (IC) de 95%. Os resultados demonstram que LNR, LODDS e status pN são fatores prognósticos significativos para a sobrevida específica do câncer em pacientes com SRCC, com todos os valores de FC mostrando significância estatística (p < 0,05). *p < 0,05, **p < 0,01, ***p < 0,001. As barras de erro representam IC de 95%. Clique aqui para ver uma versão maior desta figura.

Figura 3: Importância relativa das variáveis. (A) Modelo XGBoost, (B) Modelo RF e (C) Modelo NN. Esta figura avalia a importância relativa das variáveis. Nos modelos XGBoost e RF, o LNR exibiu a maior importância, com o LODDS também mostrando considerável significância. Por outro lado, no modelo NN, o LODDS demonstrou capacidade preditiva superior em comparação com pN e LNR. Com base nos resultados combinados dos três modelos, sugere-se que o sistema LODDS seja o mais eficaz para avaliar o status de NL em pacientes com SRCC. Clique aqui para ver uma versão maior desta figura.

Figura 4: Curvas ROC e curvas de calibração dos modelos ML, XGBoost e aumento de gradiente eXtreme. (A, D) a coorte de treinamento, (B, E) a coorte de validação e (C, F) a coorte de validação externa. O valor da área sob a curva (AUC) mais próximo de 1 indica melhor desempenho de classificação do modelo. As barras de erro representam o intervalo de confiança de 95% para a probabilidade prevista da ocorrência do evento real. Clique aqui para ver uma versão maior desta figura.
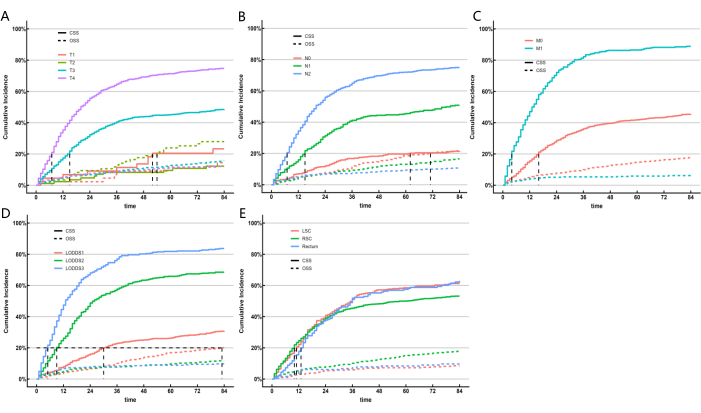
Figura 5: Estimativas de incidência cumulativa de óbito de acordo com as características dos pacientes no SRCC colorretal. CIF de subgrupos. O teste de Gray foi aplicado. Clique aqui para ver uma versão maior desta figura.
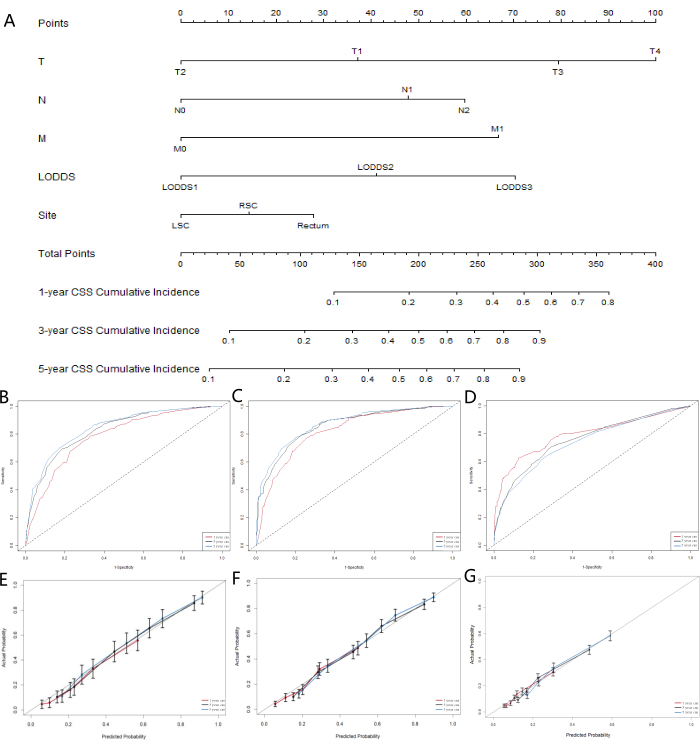
Figura 6: Desenvolvimento e validação de nomograma para CSS em pacientes com SRCC colorretal. (A) Um nomograma de risco concorrente prevendo probabilidade de sobrevida específica para câncer de 1 ano, 3 anos e 5 anos de pacientes com SRCC colorretal. As curvas de calibração dos nomogramas para prever a sobrevida específica do câncer de 1, 3 e 5 anos na coorte de treinamento (B), (C) coorte de validação e (D) coorte de validação externa. Curvas características operacionais do receptor para prever a sobrevida específica do câncer de 1, 3 e 5 anos na coorte de treinamento (E), coorte de validação (F) e coorte de validação externa (G). Clique aqui para ver uma versão maior desta figura.
Tabela 1: Características clínicas dos pacientes com CEC colorretal. Clique aqui para baixar esta tabela.
Tabela 2: Análise de regressão univariada de Cox de CSS na coorte de treinamento. Clique aqui para baixar esta tabela.
Tabela 3: Desempenho de predição dos três sistemas de estadiamento linfonodal. Clique aqui para baixar esta tabela.
Tabela 4: Desempenho preditivo dos modelos na coorte de validação e coortes de validação externa. Clique aqui para baixar esta tabela.
Tabela 5: Análise de risco competitivo univariado e multivariado para mortalidade específica por câncer de SRCC colorretal na coorte de treinamento. Clique aqui para baixar esta tabela.
Discussão
Câncer colorretal (CRC) O CCR é um subtipo raro e especial de câncer colorretal com prognóstico ruim. Portanto, maior atenção precisa ser dada ao prognóstico dos pacientes com CEC. A previsão precisa da sobrevida para pacientes com SRCC é crucial para determinar seu prognóstico e tomar decisões de tratamento individualizadas. Neste estudo, exploramos a relação entre as características clínicas e o prognóstico em pacientes com SRCC e identificamos o sistema de estadiamento ideal de LN para pacientes com SRCC a partir do banco de dados SEER. Até onde sabemos, este é o primeiro estudo a determinar o sistema LN adequado para pacientes com SRCC colorretal por meio de um uso abrangente de aprendizado de máquina e métodos de análise de risco concorrentes e a construir um nomograma para previsão prognóstica.
O número de linfonodos metastáticos em pacientes com CCR é um importante indicador de prognóstico e recorrência. O estadiamento preciso da NL desempenha um papel fundamental na determinação das estratégias de tratamento e prognóstico para pacientes com CEC. LNR e LODDS são métodos alternativos usados para avaliar o envolvimento da NL no GC, melhorar os sistemas de estadiamento e fornecer informações prognósticas mais precisas10,13. Revelamos a correlação entre LODDS, LNR e estadiamento pN com CSS em pacientes com SRCC usando o banco de dados SEER. As habilidades preditivas desses três sistemas LN (LNR, LODDS e pN) foram comparadas usando AUCs, AICs, BICs e índices C. No entanto, as diferenças entre eles eram mínimas. Portanto, usamos três métodos de aprendizado de máquina - Xgboost, RF e NN - para selecionar os recursos mais importantes como o sistema LN ideal. Com base nos resultados combinados dos três métodos, definimos LODDS como o sistema LN apropriado.
No entanto, a OSS é um evento de risco competitivo que afeta o prognóstico dos pacientes com SCS. O processo de triagem de variáveis para inclusão no modelo de aprendizado de máquina usando o método de regressão de Cox não considerou o impacto do OSS, o que pode levar a uma avaliação imprecisa das razões de risco12. Portanto, para determinar ainda mais o sistema de avaliação de LN ideal para pacientes com SRCC, construímos um modelo de risco competitivo. Os resultados confirmaram mais uma vez que o sistema de estadiamento LODDS fornece informações prognósticas mais precisas em comparação com o sistema pN. Durante o acompanhamento, entre 2409 pacientes, 1339 (56%) morreram de CSS e 464 (19%) morreram de OSS. Além disso, também desenvolvemos um gráfico de risco competitivo para prever as taxas de mortalidade específicas por câncer em 1 ano, 3 anos e 5 anos. Acreditamos que este modelo tem implicações significativas para a pesquisa clínica envolvendo pacientes com SRCC colorretal. Embora o American Joint Committee on Cancer recomende o sistema TNM como o sistema de estadiamento para todos os tipos histológicos de câncer colorretal, ele é usado principalmente para estadiamento do adenocarcinoma colorretal. O estágio AJCC N é limitado pelo TLN, enquanto o LNR não considera o impacto do NLN 13,14,15,16. Os relatórios indicam que o LODDS é menos afetado pelo TLN e considera o número de NLN10,17. Scarinci e col. demonstraram que o LODDS prediz a SG em pacientes com CCR melhor do que o estadiamento LNR e pN e sugeriram que pesquisas futuras deveriam validar seu papel em diferentes subtipos de CCR18. Neste estudo, descobrimos que o LODDS tem um efeito preditivo prognóstico significativo sobre a CSS no SRCC colorretal. Portanto, o LODDS pode ser uma ferramenta valiosa para avaliar a dissecção e o prognóstico dos linfonodos em pacientes com CEC colorretal. Embora ainda não tenha sido estabelecido um limite ideal para o LODDS, ele provou ser o sistema de estadiamento de LN mais confiável. Com o aumento da atenção ao LODDS, acredita-se geralmente que ele ganhará amplo reconhecimento em ambientes clínicos em um futuro próximo.
Nosso estudo constatou que a localização do tumor primário é um importante fator preditivo para CSS, com um prognóstico significativamente pior para o CEC retal, o que é consistente com estudos anteriores 12,19,20. O CEC retal pode ter características clínicas, patológicas e moleculares únicas21,22, justificando uma investigação mais aprofundada. Os gráficos derivados dos modelos preditivos são ferramentas fundamentais e eficazes para a tomada de decisões clínicas e aconselhamento ao paciente. Até onde sabemos, este estudo é o primeiro a integrar modelos de ML e modelos de risco concorrentes para explorar o sistema de estadiamento ideal de LN para pacientes com SRCC. Desenvolvemos e validamos três modelos de ML para prever o prognóstico de pacientes com SRCC. No conjunto de dados de teste, os modelos XGBoost, RF e NN mostraram bom desempenho preditivo prognóstico com base nos valores de AUC e métricas correspondentes. Assim, os modelos de ML podem auxiliar nas decisões de tratamento para pacientes com SRCC, prevendo o prognóstico. Além disso, geramos gráficos de risco concorrentes com base em modelos de risco proporcional para analisar fatores preditivos para SRCC colorretal e avaliar o papel do LODDS dentro dele. Utilizamos o índice C e as curvas de calibração para avaliar o desempenho preditivo do nomograma. O gráfico exibiu variáveis clínicas comuns, como sítio primário do tumor e agrupamento LODDS. Além disso, o nomograma que construímos é um método eficaz para prever o CSS de 1 ano, 3 anos e 5 anos em pacientes com SRCC colorretal. Essa ferramenta pode ajudar os médicos a realizar avaliações prognósticas precisas, completas e oportunas para cada paciente com CEC colorretal, permitindo que eles formulem planos de tratamento personalizados23.
Finalmente, este estudo tem várias limitações. Primeiro, os pacientes do estudo foram diagnosticados entre 2004 e 2015, levando a um período de acompanhamento relativamente curto. Prevemos que um período de acompanhamento mais longo ajudaria a melhorar a precisão das previsões do modelo. Em segundo lugar, o desenho do estudo usado aqui é retrospectivo e se baseia em dados obtidos do banco de dados SEER, o que pode introduzir alguns vieses inerentes. Algumas informações, como a localização dos LNs metastáticos, não foram registradas. Por fim, a maioria dos pacientes neste estudo era branca, necessitando de estudos mais amplos envolvendo diversas populações para confirmar e reforçar esses achados.
Conclusão
O estudo constatou que o LODDS exibe forte capacidade preditiva prognóstica para SRCC colorretal. Com base nessa base, desenvolvemos um nomograma baseado em um modelo de risco concorrente para prever as taxas de sobrevida global em intervalos de 1 ano, 3 anos e 5 anos para pacientes com SRCC colorretal. Após uma série de avaliações e validações internas, o nomograma demonstrou aplicabilidade e valor clínico significativos, fornecendo orientação para os médicos na tomada de decisões sobre o tratamento. Além disso, construímos três modelos de ML. Essas abordagens de ML têm o potencial de melhorar as capacidades preditivas prognósticas para SRCC e ajudar os médicos a entender como o ML pode ser utilizado para otimizar o tratamento e as estratégias de acompanhamento.
Divulgações
Os autores não têm conflitos de interesse financeiros a divulgar.
Agradecimentos
Nenhum
Materiais
| Name | Company | Catalog Number | Comments |
| SEER database | National Cancer institiute at NIH | ||
| X-tile software | Yale school of medicine | ||
| R-studio | Posit |
Referências
- Siegel, R. L., Giaquinto, A. N., Jemal, A. Cancer statistics, 2024. CA Cancer J Clin. 74 (1), 12-49 (2024).
- Korphaisarn, K., et al. Signet ring cell colorectal cancer: Genomic insights into a rare subpopulation of colorectal adenocarcinoma. Br J Cancer. 121 (6), 505-510 (2019).
- Willauer, A. N., et al. Clinical and molecular characterization of early-onset colorectal cancer. Cancer. 125 (12), 2002-2010 (2019).
- Watanabe, A., et al. A case of primary colonic signet ring cell carcinoma in a young man which preoperatively mimicked Phlebosclerotic colitis. Acta Med Okayama. 73 (4), 361-365 (2019).
- Kim, H., Kim, B. H., Lee, D., Shin, E. Genomic alterations in signet ring and mucinous patterned colorectal carcinoma. Pathol Res Pract. 215 (10), 152566(2019).
- Deng, X., et al. Neoadjuvant radiotherapy versus surgery alone for stage II/III mid-low rectal cancer with or without high-risk factors: A prospective multicenter stratified randomized trial. Ann Surg. 272 (6), 1060-1069 (2020).
- Buk Cardoso, L., et al. Machine learning for predicting survival of colorectal cancer patients. Sci Rep. 13 (1), 8874(2023).
- Monterrubio-Gómez, K., Constantine-Cooke, N., Vallejos, C. A. A review on statistical and machine learning competing risks methods. Biom J. 66 (2), e2300060(2024).
- Kim, H. J., Choi, G. S. Clinical implications of lymph node metastasis in colorectal cancer: Current status and future perspectives. Ann Coloproctol. 35 (3), 109-117 (2019).
- Xu, T., et al. Log odds of positive lymph nodes is an excellent prognostic factor for patients with rectal cancer after neoadjuvant chemoradiotherapy. Ann Transl Med. 9 (8), 637(2021).
- Chen, Y. R., et al. Prognostic performance of different lymph node classification systems in young gastric cancer. J Gastrointest Oncol. 12 (4), 285-1300 (2021).
- Bouvier, A. M., et al. How many nodes must be examined to accurately stage gastric carcinomas? Results from a population based study. Cancer. 94 (11), 2862-2866 (2002).
- Coburn, N. G., Swallow, C. J., Kiss, A., Law, C. Significant regional variation in adequacy of lymph node assessment and survival in gastric cancer. Cancer. 107 (9), 2143-2151 (2006).
- Li Destri, G., Di Carlo, I., Scilletta, R., Scilletta, B., Puleo, S. Colorectal cancer and lymph nodes: the obsession with the number 12. World J Gastroenterol. 20 (8), 1951-1960 (2014).
- Dinaux, A. M., et al. Outcomes of persistent lymph node involvement after neoadjuvant therapy for stage III rectal cancer. Surgery. 163 (4), 784-788 (2018).
- Sun, Y., Zhang, Y., Huang, Z., Chi, P. Prognostic implication of negative lymph node count in ypN+ rectal cancer after neoadjuvant chemoradiotherapy and construction of a prediction nomogram. J Gastrointest Surg. 23 (5), 1006-1014 (2019).
- Xu, Z., Jing, J., Ma, G. Development and validation of prognostic nomogram based on log odds of positive lymph nodes for patients with gastric signet ring cell carcinoma. Chin J Cancer Res. 32 (6), 778-793 (2020).
- Scarinci, A., et al. The impact of log odds of positive lymph nodes (LODDS) in colon and rectal cancer patient stratification: a single-center analysis of 323 patients. Updates Surg. 70 (1), 23-31 (2018).
- Nitsche, U., et al. Prognosis of mucinous and signet-ring cell colorectal cancer in a population-based cohort. J Cancer Res Clin Oncol. 142 (11), 2357-2366 (2016).
- Kang, H., O'Connell, J. B., Maggard, M. A., Sack, J., Ko, C. Y. A 10-year outcomes evaluation of mucinous and signet-ring cell carcinoma of the colon and rectum. Dis Colon Rectum. 48 (6), 1161-1168 (2005).
- Sung, C. O., et al. Clinical significance of signet ring cells in colorectal mucinous adenocarcinoma. Mod Pathol. 21 (12), 1533-1541 (2008).
- Alvi, M. A., et al. Molecular profiling of signet ring cell colorectal cancer provides a strong rationale for genomic targeted and immune checkpoint inhibitor therapies. Br J Cancer. 117 (2), 203-209 (2017).
- Brownlee, S., et al. Evidence for overuse of medical services around the world. Lancet. 390 (10090), 156-168 (2017).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados