Method Article
Discectomia cervicale anteriore assistita da endoscopio e fusione per il trattamento della mielopatia spondilotica cervicale
In questo articolo
Riepilogo
Descriviamo una chirurgia minimamente invasiva utilizzando la discectomia cervicale anteriore assistita da endoscopio e la fusione per la mielopatia spondilotica cervicale.
Abstract
La mielopatia spondilotica cervicale (CSM) è una causa comune di malattia del midollo spinale cervicale. L'endoscopia spinale offre vantaggi chirurgici come una vista ingrandita e un campo chirurgico chiaro mediato dall'acqua. Questo studio descrive una procedura di discectomia e fusione cervicale anteriore assistita da endoscopio (ACDF). L'aggiunta dell'endoscopia spinale alla chirurgia ACDF tradizionale ingrandisce il campo chirurgico e consente operazioni più precise, migliorando così la sicurezza chirurgica. Dopo l'intervento, i pazienti hanno sperimentato miglioramenti significativi della funzione neurologica, senza complicazioni come disfagia, ematoma o lesione del midollo spinale. L'imaging postoperatorio ha rivelato che la compressione del midollo spinale è stata completamente alleviata, con una sufficiente decompressione del midollo spinale e un posizionamento ottimale della gabbia di fusione. Il campo visivo chiaro fornito dall'endoscopia spinale migliora l'identificazione delle strutture anatomiche cervicali durante l'intervento chirurgico, riducendo efficacemente il rischio di lesioni al midollo spinale e ai nervi. L'ACDF assistita da endoscopio ha dimostrato eccellenti risultati clinici e radiologici nel trattamento del CSM.
Introduzione
La mielopatia spondilotica cervicale (CSM) è una delle forme più gravi di spondilosi cervicale. Il CSM è un gruppo di sindromi causate da alterazioni degenerative del rachide cervicale, che portano alla degenerazione delle strutture circostanti come i dischi intervertebrali e i legamenti. Queste strutture successivamente comprimono il midollo spinale, provocando disfunzioni degli arti o addirittura paralisi. La diagnosi precoce e l'intervento tempestivo sono fondamentali per migliorare la prognosi del paziente. L'intervento chirurgico è spesso necessario quando i trattamenti conservativi falliscono o la disfunzione del midollo spinale peggiora 1,2.
Sono disponibili diverse opzioni chirurgiche per il trattamento della mielopatia spondilotica cervicale (CSM), tra cui la tradizionale discectomia e fusione cervicale anteriore (ACDF), la corpectomia e fusione cervicale anteriore (ACCF), la sostituzione del disco cervicale (CDR) e la chirurgia ibrida (HS), che combina ACDF e CDR3. La discectomia e fusione cervicale anteriore tradizionale (ACDF) è un approccio terapeutico comune per il CSM che allevia efficacemente i sintomi decomprimendo direttamente il midollo spinale e le radici nervose. Tuttavia, questa chirurgia tradizionale ha dei limiti, tra cui un campo chirurgico ristretto e sfide con l'emostasi intraoperatoria. Questi problemi sono particolarmente pronunciati nei pazienti con ossificazione del legamento longitudinale posteriore (OPLL), che impedisce la rimozione completa del materiale compressivo durante l'intervento chirurgico e aumenta sostanzialmente il rischio di lesioni del midollo spinale 4,5,6. Nel 1983 Bollati ha denunciato 57 interventi chirurgici alla cervice uterina anteriore eseguiti con l'ausilio di un microscopio; Questi pazienti hanno dimostrato una sostanziale riduzione delle complicanze postoperatorie e un aumento della sicurezza e dell'efficacia7. Rispetto all'ACDF tradizionale, le tecniche microchirurgiche offrono alcuni vantaggi; Tuttavia, sono ancora presenti sfide come l'insufficiente precisione, la scarsa coordinazione occhio-mano e i punti ciechi in campo chirurgico, limitando l'applicazione clinica di queste tecniche8.
Le tecniche chirurgiche endoscopiche spinali, caratterizzate da una maggiore chiarezza visiva, un'eccellente identificazione dei tessuti e flessibilità operativa, sono state ampiamente applicate negli interventi chirurgici della colonna lombare e hanno ottenuto esiti clinici favorevoli 9,10,11. Pertanto, abbiamo integrato le tecniche endoscopiche spinali con l'ACDF tradizionale per rimuovere completamente l'ossificazione o il tessuto del nucleo polposo libero situato anteriormente al midollo spinale sotto il campo chirurgico chiaro fornito dall'endoscopio spinale. Questo approccio elimina i punti ciechi associati agli interventi chirurgici tradizionali e riduce sostanzialmente il rischio di lesioni intraoperatorie del midollo spinale. Questo articolo ha lo scopo di introdurre gli aspetti tecnici chiave dell'ACDF assistita da endoscopio. Poiché la chirurgia tradizionale dell'ACDF è stata ampiamente descritta in studi precedenti12, non sarà ribadita in questo articolo.
Protocollo
Questo studio è stato approvato dal Comitato Etico dell'Hebei General Hospital. Il consenso informato è stato ottenuto da tutti i singoli partecipanti.
1. Preparazione preoperatoria
- Prima dell'intervento, posizionare il paziente in posizione supina sul letto d'ospedale, con cuscini morbidi sotto entrambe le spalle e un cuscino cilindrico sotto l'occipite per mantenere il rachide cervicale in posizione iperestesa.
NOTA: Questo passaggio ha due scopi: (1) consentire al paziente di adattarsi alla posizione chirurgica e (2) valutare, mentre il paziente era sveglio, se l'iperestensione aggrava i sintomi neurologici. - Pianificazione dell'operazione sull'immagine: acquisire la tomografia computerizzata (TC) preoperatoria con ricostruzioni sagittali e coronali per rilevare l'ossificazione del legamento longitudinale posteriore (OPLL). Eseguire la risonanza magnetica (MRI) per valutare la compressione preoperatoria del midollo spinale.
NOTA: La distanza di ossificazione sulle immagini TC sagittali può aiutare a determinare gli intervalli superiore e inferiore della finestra.
2. Marcatura cutanea e anestesia
- Posizionare il paziente in posizione supina sul tavolo operatorio e tracciare dei segni cutanei sul segmento chirurgico.
- Disinfettare il sito chirurgico applicando iodio applicato due volte e seguito da una singola applicazione di alcol al 75%, utilizzando un movimento circolare dal sito di incisione verso l'esterno. Pianificare l'incisione come un'incisione trasversale sul collo anteriore destro.
- La gamma di disinfezione chirurgica copre principalmente la parte anteriore del collo e la parte superiore del torace. Assicurarsi che, verticalmente, si estenda dal bordo inferiore della mandibola al bordo superiore dello sterno e della clavicola e, orizzontalmente, raggiunga i bordi laterali dei muscoli sternocleidomastoidei su entrambi i lati.
- Somministrare la preossigenazione utilizzando una maschera facciale di ossigeno puro da 5 L/min per almeno 3 minuti per mantenere una saturazione di ossigeno del polso del 100% prima di iniziare l'induzione dell'anestesia generale. Chiedere a un singolo anestesista di somministrare per via endovenosa l'iniezione di sufentanil citrato (0,3-0,5 μg/kg), il cisatracurio besilato per iniezione (0,15-0,20 mg/kg) e l'iniezione di etomidato (0,2-0,4 mg/kg), monitorando continuamente l'elettrocardiogramma (ECG), la pressione sanguigna e la saturazione di ossigeno per garantire la sicurezza intraoperatoria.
3. Esposizione del segmento interessato
- Praticare un'incisione trasversale di circa 3 cm di lunghezza sul collo anteriore destro (Figura 1).
- Utilizzando l'approccio di Smith-Robinson, esporre l'aspetto anteriore del corpo vertebrale cervicale e del disco intervertebrale12. Utilizzare la fluoroscopia intraoperatoria con arco a C per confermare lo spazio del disco target.
- Incidere l'anulus fibroso del segmento interessato e rimuovere gradualmente il disco intervertebrale e le placche terminali della cartilagine fino a raggiungere il margine posteriore del corpo vertebrale.
- Installare un divaricatore Caspar e inserire il sistema endoscopico spinale nello spazio intervertebrale (Figura 2).
4. Procedure endoscopiche per il rachide cervicale
- Nella visualizzazione endoscopica spinale, indirizzare gli speroni ossei al margine posteriore del corpo vertebrale cervicale e allargare lo spazio intervertebrale. Utilizzare una fresa per rimuovere gli speroni ossei superiore e inferiore, nonché i punti di attacco dell'anulus fibrosus.
- La gamma di rimozione ossea su entrambi i lati si estende alle articolazioni non covertebrali; determinare l'entità dell'escissione cranica e caudale sulla base della posizione e delle dimensioni dell'ossificazione osservate all'imaging preoperatorio, garantendo un'escissione sufficiente ad entrambe le estremità.
- Asportare l'anulus fibroso profondo. Utilizzare alternativamente una pinza per nucleo polposo, punzoni Kerrison e altri strumenti per decomprimere il canale spinale, estendendo progressivamente la decompressione verso il midollo spinale (Figura 3).
NOTA: Durante il processo di sbavatura, le tecniche di rettifica laterale e di trazione verso l'alto sono state prioritarie per evitare un'eccessiva rimozione dell'osso superficiale, proteggendo così la placca terminale ossea. L'uso di un endoscopio spinale con angolo di 30°, capacità di inclinazione e fresa multidirezionale ha ulteriormente ampliato l'intervallo di decompressione e ha garantito una maggiore precisione chirurgica.
- Incidere il legamento longitudinale posteriore (PLL) morbido per esporre il midollo spinale. Dopo che l'anulus fibroso e lo strato superficiale del PLL sono stati incisi, utilizzare un punzone Kerrison e un coltello a uncino per tagliare il PLL morbido e separare lo spazio tra il PLL e il midollo spinale (Figura 4).
NOTA: Una volta separato lo spazio tra il midollo spinale e il PLL, la successiva decompressione diventa significativamente più facile. La rimozione del PLL e l'esposizione del midollo spinale sono passaggi fondamentali in questa procedura. - Per i pazienti con OPLL, iniziare la procedura con la rimozione del PLL molle e l'esposizione del midollo spinale. Utilizzare un dissettore della radice nervosa per valutare lo spazio tra l'ossificazione e il midollo spinale per confermare se c'è adesione tra l'ossificazione e la dura madre. Utilizzare una pinza per nucleo polposo a 45° o un punzone Kerrison per rimuovere gradualmente il legamento ossificato fino a quando la dura madre non è completamente esposta. Eseguire la visualizzazione endoscopica per verificare se la pulsazione della dura madre è soddisfacente (Figura 5).
NOTA: Durante questo processo, sono stati utilizzati alternativamente una fresa, un dissettore della radice nervosa, una pinza per nucleo polposo o un punzone Kerrison per aumentare la flessibilità operativa e la sicurezza. - Utilizzare sonde di elettrocoagulazione bipolare per l'emostasi e applicare gelatina fluida per aiutare a controllare il sanguinamento. Una volta confermato che il campo chirurgico è privo di sanguinamento attivo, estrarre lentamente l'endoscopio spinale (Figura 6).
NOTA: Evitare la rimozione rapida dell'endoscopio spinale per prevenire l'ernia durale causata dalla pressione negativa. - Riempire una gabbia in rete di titanio di dimensioni adeguate con osso autologo e inserirla nello spazio intervertebrale. Selezionare una placca in titanio abbastanza lunga da coprire il segmento chirurgico e impiantare sei viti nelle vertebre per fissare la placca in titanio, seguendo la procedura standard del tradizionale ACDF12 per garantire la stabilità postoperatoria e la riuscita della fusione.
5. Cure postoperatorie
- Eseguire il monitoraggio ECG continuo e somministrare l'inalazione e la nebulizzazione intermittente di ossigeno; Incoraggia il paziente a tossire ed espettorare.
- Valutare l'intensità del dolore del paziente mediante indagine e somministrare prontamente analgesici non steroidei secondo necessità.
- Monitorare attentamente i cambiamenti nella forza muscolare degli arti e nella funzione sensoriale.
- Rimuovere il tubo di drenaggio quando il volume di drenaggio è inferiore a 30 ml entro 24 ore dopo l'intervento.
Risultati
Questo studio ha incluso 20 pazienti sottoposti a chirurgia ACDF assistita da endoscopio da gennaio 2024 a novembre 2024. L'età media era di 62,2 anni e il campione dello studio comprendeva 9 femmine e 11 maschi. Il tempo operatorio medio è stato di 125,5 minuti e il volume medio di perdita di sangue è stato di 59,0 ml (Tabella 1 e Tabella 2). Tutti i pazienti hanno ottenuto un sollievo efficace dai sintomi del midollo spinale, con punteggi VAS (Visual Analog Scale) postoperatori più bassi rispetto ai punteggi preoperatori e punteggi JOA postoperatori significativamente migliorati. Il tasso medio di miglioramento del punteggio JOA è stato del 60,7%. Non si sono verificate complicanze, come disfagia, ematoma o lesione del midollo spinale (Tabella 1 e Tabella 2). L'imaging postoperatorio ha confermato la rimozione completa del materiale compressivo, una sufficiente decompressione del midollo spinale e il corretto posizionamento della gabbia di fusione (Figura 7 e Figura 8).
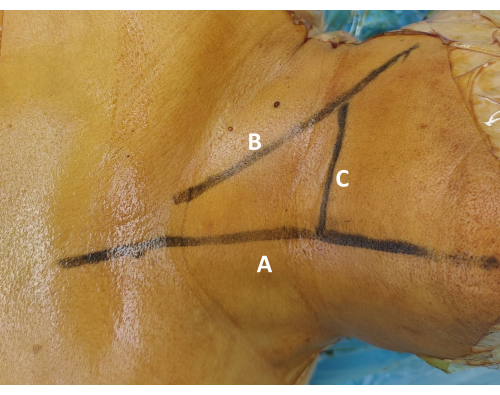
Figura 1: Marcatura superficiale del segmento chirurgico. (A) Tracciare la marcatura della linea mediana lungo la linea mediana tracheale per garantire la simmetria chirurgica. (B) Tracciare la linea di localizzazione trasversale lungo il bordo superiore della clavicola. Palpare il muscolo sternocleidomastoideo e la cartilagine cricoidea per guidare questa marcatura. (C) Confermare la marcatura del livello target utilizzando la guida fluoroscopica e contrassegnare la corrispondente proiezione cutanea del disco intervertebrale previsto. Fare clic qui per visualizzare una versione più grande di questa figura.

Figura 2: Procedure preoperatorie per endoscopia spinale. (A) Posizionamento intraoperatorio della fluoroscopia con arco a C. (B) Installazione del divaricatore Caspar. (C) Endoscopia spinale. Clicca qui per visualizzare una versione più grande di questa figura.
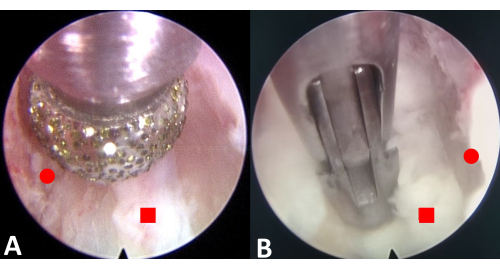
Figura 3: Escissione endoscopica degli osteofiti e dell'anulus fibrosus. (A) Sbavare gli osteofiti superiori e inferiori. (B) Resecare l'anulus fibrosus. Il cerchio rosso rappresenta l'osteofita e il quadrato rosso rappresenta l'anulus fibrosus. Clicca qui per visualizzare una versione più grande di questa figura.
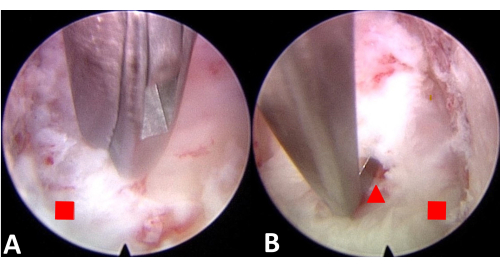
Figura 4: Incisione endoscopica del PLL e separazione del PLL dal midollo spinale per creare spazio. (A) Incidere il PLL. (B) Separare il PLL dal midollo spinale. Il quadrato rosso rappresenta il legamento longitudinale posteriore e il triangolo rosso rappresenta il midollo spinale. Clicca qui per visualizzare una versione più grande di questa figura.

Figura 5: Escissione endoscopica dell'ossificazione. (A) Valutare lo spazio tra il tessuto ossificato e il midollo spinale. (B) Asportare il legamento ossificato. Il triangolo rosso rappresenta il midollo spinale e la freccia rossa indica l'ossificazione del legamento longitudinale posteriore. Clicca qui per visualizzare una versione più grande di questa figura.

Figura 6: Emostasi. (A) Punto di sanguinamento. (B) Emostasi in visualizzazione endoscopica. L'asterisco rappresenta il punto di sanguinamento. Clicca qui per visualizzare una versione più grande di questa figura.
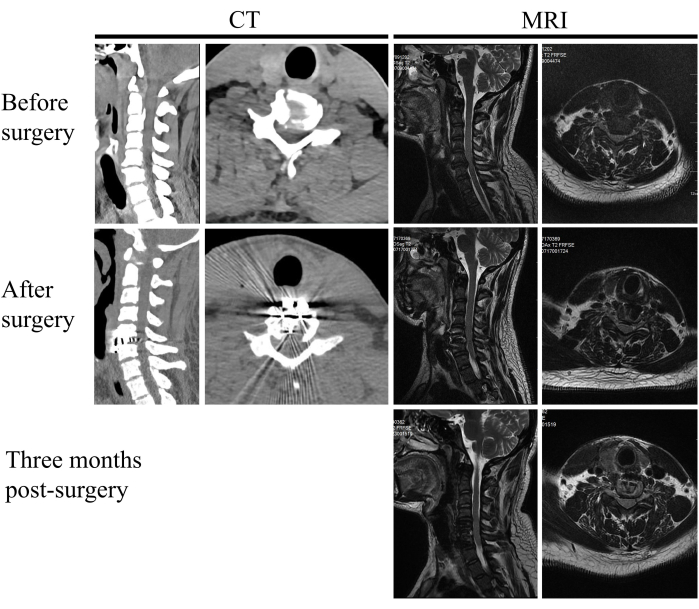
Figura 7: Imaging pre e postoperatorio. Un paziente con mielopatia spondilotica cervicale prima dell'intervento chirurgico, dopo l'intervento chirurgico e 3 mesi dopo l'intervento. Clicca qui per visualizzare una versione più grande di questa figura.
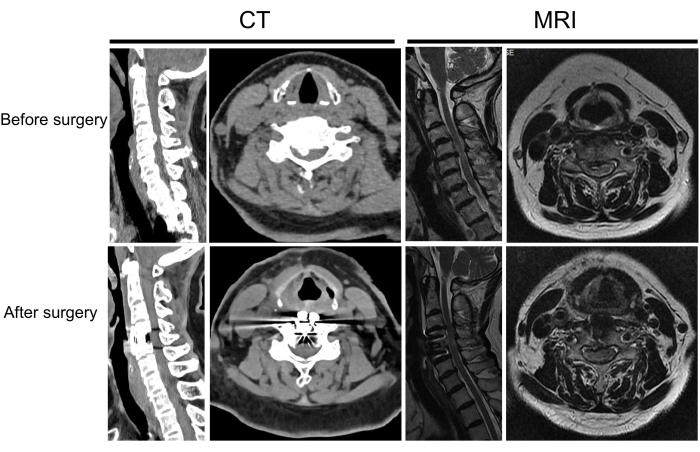
Figura 8: Imaging pre e postoperatorio di un altro paziente. Un paziente con mielopatia spondilotica cervicale prima e dopo l'intervento chirurgico. Clicca qui per visualizzare una versione più grande di questa figura.
Tabella 1: Informazioni per il paziente. Clicca qui per scaricare questa tabella.
Tabella 2: Caratteristiche chirurgiche ed esiti postoperatori. Clicca qui per scaricare questa tabella.
Discussione
La discectomia e fusione cervicale anteriore (ACDF) è un metodo chirurgico comune per il trattamento della mielopatia spondilotica cervicale (CSM) e ha esiti clinici soddisfacenti13,14. Tuttavia, la chirurgia tradizionale deve affrontare sfide come un campo chirurgico limitato e difficoltà con l'emostasi. Questi problemi sono particolarmente accentuati nei casi di ossificazione del legamento longitudinale posteriore (OPLL) o di ernia del disco a distanza; In questi casi, il materiale compressivo non può essere completamente rimosso intraoperatoriamente e il rischio di lesioni del midollo spinale rimane elevato15.
Con i progressi nelle tecniche di chirurgia spinale minimamente invasiva, l'applicazione dell'endoscopia microscopica nell'ACDF è gradualmente aumentata, ampliando il campo chirurgico e migliorando la precisione operativa. Tuttavia, la procedura assistita dal microscopio presenta ancora dei limiti, come la scarsa coordinazione occhio-mano e i punti ciechi nel campo visivo8. La discectomia cervicale anteriore endoscopica completa (FACD) è una procedura minimamente invasiva. Rispetto alla chirurgia convenzionale, la FACD riduce significativamente il danno ai tessuti molli, il tempo operatorio e le complicanze. Il processo di recupero è rapido, senza la necessità di ulteriori interventi chirurgici16.
Tuttavia, l'ACDF assistita da endoscopio offre diversi vantaggi rispetto alla decompressione cervicale anteriore completamente endoscopica, in particolare in termini di stabilità postoperatoria, indicazioni più ampie e facilità di esecuzione chirurgica. Incorporando la fusione intersomatica con una gabbia in titanio e una piastra di fissaggio, migliora la stabilità segmentale e riduce al minimo il rischio di perdita o recidiva postoperatoria dell'altezza del disco, che è un problema con le tecniche endoscopiche complete non di fusione. Inoltre, l'ACDF assistita da endoscopio è più adatta per la malattia multilivello, la grave degenerazione del disco e i casi di ossificazione del legamento longitudinale posteriore (OPLL), dove la decompressione endoscopica completa può essere insufficiente. Questa tecnica fornisce anche un campo chirurgico più ampio, consentendo una decompressione neurale più completa e riducendo il rischio di compressione residua. Inoltre, segue la procedura ACDF standard, rendendola più facile da adottare per i chirurghi rispetto all'approccio endoscopico completo tecnicamente impegnativo.
Mentre la decompressione anteriore endoscopica completa è vantaggiosa per casi selezionati con ernia del disco molle a livello singolo, l'ACDF assistita da endoscopio rimane un'opzione più versatile e riproducibile per una gamma più ampia di patologie del rachide cervicale. L'ACDF assistita da endoscopio ha ottenuto eccellenti risultati clinici e radiologici, dimostrando un'efficacia affidabile e un'elevata sicurezza chirurgica. Wu et al.17. ha scoperto che l'ACDF assistita da endoscopio offre vantaggi significativi rispetto all'ACDF tradizionale, tra cui un campo chirurgico più chiaro, una minore perdita di sangue intraoperatoria e un minor rischio di lesioni nervose. Tuttavia, hanno anche riportato un tempo operatorio più lungo a causa della complessità delle tecniche endoscopiche. I nostri risultati sono coerenti con i loro risultati, poiché il nostro studio ha anche dimostrato un tempo chirurgico leggermente prolungato con ACDF assistito da endoscopio. Tuttavia, la durata prolungata non influisce in modo significativo sui risultati clinici e i vantaggi di una migliore visualizzazione e di una riduzione del trauma superano questa limitazione, rendendo l'ACDF assistita da endoscopio una valida alternativa alla tradizionale ACDF.As un nuovo strumento di ingrandimento per l'ACDF, l'endoscopia spinale offre una visualizzazione più chiara e una maggiore flessibilità operativa, affrontando efficacemente questi problemi.
I vantaggi delle operazioni endoscopiche assistite sono i seguenti. Innanzitutto, sotto endoscopia spinale, il PLL può essere distinto in modo più dettagliato, consentendo una dissezione nitida utilizzando i punzoni Kerrison. L'endoscopio fornisce una visione più chiara del midollo spinale, consentendo al chirurgo di valutare con precisione l'adeguatezza della decompressione e di ridurre efficacemente il rischio di lesioni del midollo spinale. Inoltre, l'uso di una fresa consente un'operazione di prossimità, garantendo una rimozione più precisa e completa degli speroni ossei. Rispetto all'occhio nudo e al microscopio, l'endoscopio offre una visualizzazione superiore durante l'esposizione e la decompressione delle articolazioni non covertebrali bilaterali.
In secondo luogo, l'endoscopio spinale offre una maggiore libertà d'uso grazie all'angolo di visione integrato di 30° e alla testa della fresa regolabile, che consente un intervallo di decompressione più ampio. Questa caratteristica migliora la flessibilità e la precisione quando si lavora in regioni anatomiche complesse. In terzo luogo, l'endoscopia mediata dall'acqua consente un'identificazione più accurata dei punti di sanguinamento. Per il sanguinamento al margine posteriore del corpo vertebrale, la sonda a radiofrequenza curva può raggiungere e indirizzare con precisione il sito di sanguinamento, migliorando significativamente l'efficacia emostatica e la precisione chirurgica. In quarto luogo, il sistema endoscopico riduce al minimo l'interferenza delle mani del chirurgo, riducendo il numero di punti ciechi nel campo chirurgico. Il design coassiale dell'endoscopio si allinea con le abitudini operative dei chirurghi endoscopici, prevenendo le collisioni degli strumenti e garantendo procedure più fluide ed efficienti.
Tuttavia, l'applicazione delle tecniche endoscopiche spinali presenta anche alcune sfide, come il prolungamento del tempo operatorio e la necessità di chirurghi con competenze chirurgiche avanzate e conoscenze dettagliate di microanatomia. Inoltre, sebbene la chirurgia endoscopica offra un campo visivo più ampio, il campo può essere ancora limitato in casi estremamente complessi. Con il continuo progresso della tecnologia e i miglioramenti negli strumenti chirurgici, riteniamo che l'uso dell'endoscopia spinale nella chirurgia del rachide cervicale maturerà gradualmente e che il tempo operatorio diminuirà ulteriormente.
Divulgazioni
Gli autori non hanno conflitti di interesse da dichiarare.
Riconoscimenti
Nessuno
Materiali
| Name | Company | Catalog Number | Comments |
| 75% alcohol | Hebei Ruihe Medical Equipment Co., Ltd | CC-01A | PEEK |
| Anterior Cervical Nail Plate Fixation System | Hebei Ruihe Medical Equipment Co., Ltd | PN-03 | Plate:TA3G, Nail:TC4 |
| Cervical Fusion Cage | |||
| cisatracurium besylate | SPINENDOS GmbH | SP081430.030 | Inner diameter:4.3 mm; Outer diameter:7.0 mm; Field angle: 80 °; Visual angle: 30 °; Working length: 181 mm |
| Endoscope system | SPINENDOS GmbH | SP082628.351 | Φ2.5 mm × 310 mm |
| Endoscopic forceps | SPINENDOS GmbH | SP082700.040L | Φ4.0 mm × 360 mm |
| Endoscopic hook | XIYI | MQZ | Φ3.2 mm × 328 mm |
| Endoscopic rongeur | ELLIQUENCE | DTF-40 | 40 cm |
| etomidate | SPINENDOS GmbH | SP082781.835 | Φ2.5 mm × 330 mm |
| High-speed burr | Neusoft Corporation | ||
| Interventional radiology | Ferrosan Medical Devices A/S | MS0010 | |
| iodine | Sichuan Guona Technology Co.,LTD | NNBP/40D/ | |
| Neusoft PACS/RIS | Elliquence, LLC | DTF-40 | |
| n-HA/PA66 | SPINENDOS GmbH | SP082615.265 | Φ7.2 mm × 178 mm |
| sufentanil citrate injection | |||
| SURGIFLO Haemostatic Matrix | |||
| Trigger-Flex Bipolar System | |||
| Working sheath |
Riferimenti
- Bakhsheshian, J., Mehta, V. A., Liu, J. C. Current diagnosis and management of cervical spondylotic myelopathy. Global Spine J. 7 (6), 572-586 (2017).
- McCormick, J. R., Sama, A. J., Schiller, N. C., Butler, A. J., Donnally, C. J. Cervical spondylotic myelopathy: A guide to diagnosis and management. J Am Board Fam Med. 33 (2), 303-313 (2020).
- Visocchi, M., et al. Hybrid implants in anterior cervical decompressive surgery for degenerative disease. J Craniovertebr Junction Spine. 12 (1), 54-60 (2021).
- Lee, C. J., Boody, B. S., Demeter, J., Smucker, J. D., Sasso, R. C. Long-term radiographic and functional outcomes of patients with absence of radiographic union at 2 years after single-level anterior cervical discectomy and fusion. Global Spine J. 10 (6), 741-747 (2020).
- Luo, H. T., et al. Meta-analysis of the treatment of cervical spondylosis by microscopy-assisted and traditional anterior cervical decompression under direct vision. Chin J Tissue Eng Res. 24 (9), 1369-1377 (2020).
- Marawar, S., et al. National trends in anterior cervical fusion procedures. Spine (Phila Pa 1976). 35 (15), 1454-1459 (2010).
- Bollati, A., Galli, G., Gandolfini, M., Marini, G., Gatta, G. Microsurgical anterior cervical disk removal without interbody fusion. Surg Neurol. 19 (4), 329-333 (1983).
- Damodaran, O., Lee, J., Lee, G. Microscope in modern spinal surgery: Advantages, ergonomics and limitations. ANZ J Surg. 83 (4), 211-214 (2013).
- Liu, L., Dong, J., Wang, D., Zhang, C., Zhou, Y. Clinical outcomes and quality of life in elderly patients treated with a newly designed double tube endoscopy for degenerative lumbar spinal stenosis. Orthop Surg. 14 (7), 1359-1368 (2022).
- Han, S., et al. Clinical application of large channel endoscopic systems with full endoscopic visualization technique in lumbar central spinal stenosis: A retrospective cohort study. Pain Ther. 11 (4), 1309-1326 (2022).
- Liang, J., Li, H., Tao, Y., Yuan, W., Wang, H. Efficacy and complications of unilateral biportal endoscopic spinal surgery for lumbar spinal stenosis: A meta-analysis and systematic review. World Neurosurg. 159, e91-e102 (2022).
- Tian, X., Rudd, S., Yang, D., Ding, W., Yang, S. Anterior cervical hybrid decompression and fusion surgery to treat multilevel cervical spondylotic myelopathy. J Vis Exp. (196), e65034 (2023).
- Sun, X., et al. The frequency and treatment of dural tears and cerebrospinal fluid leakage in 266 patients with thoracic myelopathy caused by ossification of the ligamentum flavum. Spine (Phila Pa 1976). 37 (12), E702-E707 (2012).
- Wang, T., et al. Anterior cervical discectomy and fusion versus anterior cervical corpectomy and fusion in multilevel cervical spondylotic myelopathy: A meta-analysis. Medicine (Baltimore). 95 (49), e5437 (2016).
- Nakajima, H., et al. Long-term outcome of anterior cervical decompression with fusion for cervical ossification of posterior longitudinal ligament including postsurgical remnant ossified spinal lesion. Spine (Phila Pa 1976). 44 (24), E1452-E1460 (2019).
- Ruetten, S., Komp, M., Merk, H., Godolias, G. Full-endoscopic anterior decompression versus conventional anterior decompression and fusion in cervical disc herniations. Int Orthop. 33 (6), 1677-1682 (2009).
- Wu, Z. P., Wei, Z. Y., Song, X. L. Comparison of efficacy between endoscope-assisted anterior cervical discectomy and fusion (ACDF) and open ACDF in the treatment of single-segment cervical spondylotic myelopathy. J Orthop Surg Res. 19 (1), 35 (2024).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneEsplora altri articoli
This article has been published
Video Coming Soon