Method Article
Endoskopgestützte anteriore zervikale Diskektomie und Fusion zur Behandlung der zervikalen spondylotischen Myelopathie
In diesem Artikel
Zusammenfassung
Wir beschreiben eine minimalinvasive Operation mit endoskopgestützter anteriorer zervikaler Diskektomie und Fusion bei der zervikalen spondylotischen Myelopathie.
Zusammenfassung
Die zervikale spondylotische Myelopathie (CSM) ist eine häufige Ursache für zervikale Rückenmarkserkrankungen. Die Wirbelsäulenendoskopie bietet chirurgische Vorteile wie eine vergrößerte Sicht und ein wasservermitteltes klares Operationsfeld. Diese Studie beschreibt ein endoskopgestütztes Verfahren zur anterioren zervikalen Diskektomie und Fusion (ACDF). Die Ergänzung der traditionellen ACDF-Chirurgie um die Wirbelsäulenendoskopie vergrößert das Operationsfeld und ermöglicht präzisere Operationen, wodurch die chirurgische Sicherheit verbessert wird. Postoperativ zeigten die Patienten signifikante Verbesserungen der neurologischen Funktion, ohne Komplikationen wie Dysphagie, Hämatom oder Rückenmarksverletzungen. Die postoperative Bildgebung zeigte, dass die Rückenmarkskompression vollständig entlastet wurde, mit ausreichender Dekompression des Rückenmarks und optimaler Platzierung des Fusionskäfigs. Das klare Gesichtsfeld, das die Wirbelsäulenendoskopie bietet, verbessert die Identifizierung der anatomischen Strukturen des Gebärmutterhalses während der Operation und reduziert effektiv das Risiko von Verletzungen des Rückenmarks und der Nerven. Die endoskopgestützte ACDF hat hervorragende klinische und radiologische Ergebnisse bei der Behandlung von CSM gezeigt.
Einleitung
Die zervikale spondylotische Myelopathie (CSM) ist eine der schwereren Formen der zervikalen Spondylose. CSM ist eine Gruppe von Syndromen, die durch degenerative Veränderungen der Halswirbelsäule verursacht werden, die zu einer Degeneration der umgebenden Strukturen wie Bandscheiben und Bänder führen. Diese Strukturen komprimieren anschließend das Rückenmark, was zu Funktionsstörungen der Gliedmaßen oder sogar zu Lähmungen führt. Eine frühzeitige Diagnose und rechtzeitiges Eingreifen sind entscheidend für die Verbesserung der Patientenprognose. Ein chirurgischer Eingriff ist häufig erforderlich, wenn konservative Behandlungen versagen oder sich die Funktionsstörung des Rückenmarks verschlimmert 1,2.
Für die Behandlung der zervikalen spondylotischen Myelopathie (CSM) stehen mehrere chirurgische Optionen zur Verfügung, darunter die traditionelle anteriore zervikale Diskektomie und Fusion (ACDF), die anteriore zervikale Korpektomie und Fusion (ACCF), der zervikale Bandscheibenersatz (CDR) und die Hybridchirurgie (HS), die ACDF und CDR3 kombiniert. Die traditionelle anteriore zervikale Diskektomie und Fusion (ACDF) ist ein gängiger Behandlungsansatz für CSM, der die Symptome durch direkte Dekompression des Rückenmarks und der Nervenwurzeln wirksam lindert. Diese traditionelle Operation hat jedoch Einschränkungen, darunter ein enges Operationsfeld und Herausforderungen bei der intraoperativen Hämostase. Diese Probleme sind besonders ausgeprägt bei Patienten mit einer Ossifikation des hinteren Längsbandes (OPLL), die verhindert, dass das Kompressionsmaterial während der Operation vollständig entfernt wird, und das Risiko einer Rückenmarksverletzung erheblich erhöht 4,5,6. Im Jahr 1983 berichtete Bollati von 57 vorderen Gebärmutterhalsoperationen, die mit Hilfe eines Mikroskops durchgeführt wurden; Diese Patienten zeigten deutlich reduzierte postoperative Komplikationen und eine erhöhte Sicherheit und Wirksamkeit7. Im Vergleich zu herkömmlichen ACDF bieten mikrochirurgische Techniken gewisse Vorteile; Herausforderungen wie unzureichende Präzision, schlechte Hand-Auge-Koordination und blinde Flecken im chirurgischen Bereich sind jedoch nach wie vor vorhanden, was die klinische Anwendung dieser Techniken einschränkt8.
Endoskopische Operationstechniken der Wirbelsäule, die sich durch eine größere visuelle Klarheit, eine hervorragende Gewebeidentifizierung und operative Flexibilität auszeichnen, wurden bei Operationen an der Lendenwirbelsäule häufig eingesetzt und haben günstige klinische Ergebnisse erzielt 9,10,11. Aus diesem Grund haben wir endoskopische Techniken der Wirbelsäule mit der traditionellen ACDF kombiniert, um die Ossifikation oder das freie Nucleus pulposus-Gewebe, das sich vor dem Rückenmark befindet, unter dem klaren Operationsfeld des Wirbelsäulenendoskops gründlich zu entfernen. Dieser Ansatz beseitigt blinde Flecken, die mit herkömmlichen Operationen verbunden sind, und reduziert das Risiko einer intraoperativen Rückenmarksverletzung erheblich. In diesem Artikel sollen die wichtigsten technischen Aspekte der endoskopgestützten ACDF vorgestellt werden. Da die traditionelle ACDF-Chirurgie in früheren Studien ausführlich beschrieben wurde12, wird sie in diesem Artikel nicht wiederholt.
Protokoll
Diese Studie wurde von der Ethikkommission des Hebei General Hospital genehmigt. Die Einverständniserklärung wurde von allen einzelnen Teilnehmern eingeholt.
1. Präoperative Vorbereitung
- Legen Sie den Patienten vor der Operation in Rückenlage auf das Krankenhausbett, mit weichen Kissen unter beiden Schultern und einem zylindrischen Kissen unter dem Hinterkopf, um die Halswirbelsäule in einer überstreckten Position zu halten.
HINWEIS: Dieser Schritt dient zwei Zwecken: (1) dem Patienten die Anpassung an die chirurgische Position zu ermöglichen und (2) im Wachzustand zu beurteilen, ob die Überstreckung die neurologischen Symptome verschlimmert. - Operationsplanung auf dem Bild: Machen Sie eine präoperative Computertomographie (CT) mit sagittalen und koronalen Rekonstruktionen, um eine Ossifikation des hinteren Längsbandes (OPLL) zu erkennen. Führen Sie eine Magnetresonanztomographie (MRT) durch, um die präoperative Rückenmarkskompression zu beurteilen.
HINWEIS: Der Abstand der Ossifikation auf sagittalen CT-Bildern kann bei der Bestimmung des oberen und unteren Bereichs des Fensters hilfreich sein.
2. Hautmarkierung und Anästhesie
- Legen Sie den Patienten in Rückenlage auf den Operationstisch und nehmen Sie Hautmarkierungen am chirurgischen Segment vor.
- Desinfizieren Sie die Operationsstelle, indem Sie zweimal Jod auftragen und anschließend 75 % Alkohol mit kreisenden Bewegungen von der Inzisionsstelle nach außen auftragen. Planen Sie den Schnitt als Querschnitt am rechten vorderen Hals.
- Das chirurgische Desinfektionsprogramm erstreckt sich hauptsächlich auf den vorderen Hals und die obere Brust. Achten Sie darauf, dass er sich vertikal vom unteren Rand des Unterkiefers bis zum oberen Rand des Brustbeins und des Schlüsselbeins erstreckt und horizontal die lateralen Ränder der Musculus sternocleidomastoideus auf beiden Seiten erreicht.
- Verabreichen Sie die Präoxygenierung mit einer 5 l/min reinen Sauerstoff-Gesichtsmaske für mindestens 3 Minuten, um eine Pulssauerstoffsättigung von 100 % aufrechtzuerhalten, bevor Sie die Einleitung der Vollnarkose einleiten. Lassen Sie einen einzigen Anästhesisten intravenös Sufentanilcitrat-Injektion (0,3-0,5 μg/kg), Cisatracuriumbesylat zur Injektion (0,15-0,20 mg/kg) und Etomidat-Injektion (0,2-0,4 mg/kg) verabreichen, während das Elektrokardiogramm (EKG), der Blutdruck und die Sauerstoffsättigung kontinuierlich überwacht werden, um die intraoperative Sicherheit zu gewährleisten.
3. Exposition des betroffenen Segments
- Machen Sie einen etwa 3 cm langen Querschnitt am rechten vorderen Hals (Abbildung 1).
- Unter Verwendung des Smith-Robinson-Ansatzes wird die vordere Seite des Halswirbelkörpers und der Bandscheibe12 freigelegt. Verwenden Sie eine intraoperative C-Bogen-Fluoroskopie, um den Ziel-Bandscheibenraum zu bestätigen.
- Den Anulus fibrosus des betroffenen Segments einschneiden und nach und nach die Bandscheibe und die Knorpelendplatten entfernen, bis der hintere Rand des Wirbelkörpers erreicht ist.
- Installieren Sie einen Caspar-Retraktor und setzen Sie das Wirbelsäulenendoskopsystem in den Zwischenwirbelraum ein (Abbildung 2).
4. Endoskopische Eingriffe an der Halswirbelsäule
- Unter endoskopischer Visualisierung der Wirbelsäule werden knöcherne Ausläufer am hinteren Rand des Halswirbelkörpers behandelt und der Zwischenwirbelraum vergrößert. Mit einem Fräser den oberen und unteren Knochensporn sowie die Ansatzpunkte des Anulus fibrosus entfernen.
- Der Bereich der Knochenentfernung auf beiden Seiten erstreckt sich bis zu den unbedeckten Tebragelenken; Bestimmen Sie das Ausmaß der kranialen und kaudalen Exzision auf der Grundlage der Lokalisation und der Größe der Ossifikation, die in der präoperativen Bildgebung beobachtet wurde, und stellen Sie eine ausreichende Exzision an beiden Enden sicher.
- Exzidieren Sie den tiefen Anulus fibrosus. Verwenden Sie abwechselnd eine Nucleus-pulposus-Zange, Kerrison-Stanzen und andere Werkzeuge, um den Spinalkanal zu dekomprimieren und die Dekompression schrittweise in Richtung Rückenmark auszudehnen (Abbildung 3).
HINWEIS: Während des Entgratungsprozesses wurden die Schleiftechniken des Querschleifens und des Traktionsschleifens nach oben priorisiert, um eine übermäßige Entfernung des oberflächlichen Knochens zu vermeiden und so die knöcherne Endplatte zu schützen. Durch den Einsatz eines Wirbelsäulenendoskops mit 30°-Winkel, Kippbarkeit und multidirektionalem Grat wurde der Dekompressionsbereich weiter erweitert und eine höhere chirurgische Präzision gewährleistet.
- Schneiden Sie das hintere Längsband (PLL) weich an, um das Rückenmark freizulegen. Nachdem der Anulus fibrosus und die oberflächliche Schicht der PLL eingeschnitten wurden, wird mit einem Kerrison-Stempel und einem Hakenmesser die weiche PLL durchtrennt und der Raum zwischen der PLL und dem Rückenmark getrennt (Abbildung 4).
HINWEIS: Sobald der Spalt zwischen dem Rückenmark und der PLL getrennt ist, wird die anschließende Dekompression erheblich einfacher. Die PLL-Entfernung und die Freilegung des Rückenmarks sind wichtige Schritte in diesem Verfahren. - Bei Patienten mit OPLL beginnen Sie den Eingriff mit der Entfernung der weichen PLL und der Freilegung des Rückenmarks. Verwenden Sie einen Nervenwurzeldissektor, um den Raum zwischen der Ossifikation und dem Rückenmark zu beurteilen und zu bestätigen, ob eine Adhäsion zwischen der Ossifikation und der Dura mater besteht. Verwenden Sie eine 45°-Nucleus pulposus-Zange oder eine Kerrison-Stanze, um das verknöcherte Band allmählich zu entfernen, bis die Dura mater vollständig freigelegt ist. Führen Sie eine endoskopische Visualisierung durch, um zu überprüfen, ob die Pulsation der Dura mater zufriedenstellend ist (Abbildung 5).
HINWEIS: Während dieses Prozesses wurden abwechselnd ein Fräser, ein Nervenwurzeldissektor, eine Nucleus pulposus-Zange oder eine Kerrison-Stanze verwendet, um die Betriebsflexibilität und -sicherheit zu erhöhen. - Verwenden Sie bipolare Elektrokoagulationssonden für die Blutstillung und tragen Sie flüssige Gelatine auf, um die Blutung zu kontrollieren. Sobald bestätigt ist, dass das Operationsfeld frei von aktiven Blutungen ist, wird das Wirbelsäulenendoskop langsam zurückgezogen (Abbildung 6).
HINWEIS: Vermeiden Sie eine schnelle Entfernung des Wirbelsäulenendoskops, um einen durch Unterdruck verursachten Duralvorfall zu vermeiden. - Füllen Sie einen entsprechend großen Titan-Netzkäfig mit autologem Knochen und führen Sie ihn in den Zwischenwirbelraum ein. Wählen Sie eine Titanplatte, die lang genug ist, um das chirurgische Segment abzudecken, und implantieren Sie sechs Schrauben in die Wirbel, um die Titanplatte zu sichern, gemäß dem Standardverfahren des traditionellen ACDF12 , um postoperative Stabilität und erfolgreiche Fusion zu gewährleisten.
5. Nachsorge
- Führen Sie eine kontinuierliche EKG-Überwachung durch und verabreichen Sie intermittierende Sauerstoffinhalation und -vernebelung; Ermutigen Sie den Patienten zum Husten und Ausspucken.
- Beurteilen Sie die Schmerzintensität des Patienten durch Befragung und verabreichen Sie bei Bedarf umgehend nichtsteroidale Analgetika.
- Überwachen Sie Veränderungen der Muskelkraft der Gliedmaßen und der sensorischen Funktion genau.
- Entfernen Sie den Drainageschlauch, wenn das Drainagevolumen innerhalb von 24 h postoperativ weniger als 30 ml beträgt.
Ergebnisse
An dieser Studie nahmen 20 Patienten teil, die sich von Januar 2024 bis November 2024 einer endoskopgestützten ACDF-Operation unterzogen hatten. Das Durchschnittsalter betrug 62,2 Jahre, und die Studienstichprobe umfasste 9 Frauen und 11 Männer. Die durchschnittliche Operationszeit betrug 125,5 min und das mittlere Volumen des Blutverlusts 59,0 ml (Tabelle 1 und Tabelle 2). Alle Patienten erreichten eine erfolgreiche Linderung der Rückenmarkssymptome, mit niedrigeren postoperativen Werten der visuellen Analogskala (VAS) im Vergleich zu den präoperativen Werten und signifikant verbesserten postoperativen JAA-Werten. Die durchschnittliche Verbesserungsrate des JAA-Scores betrug 60,7 %. Es traten keine Komplikationen wie Dysphagie, Hämatom oder Rückenmarksverletzung auf (Tabelle 1 und Tabelle 2). Die postoperative Bildgebung bestätigte die vollständige Entfernung des Kompressionsmaterials, eine ausreichende Dekompression des Rückenmarks und die korrekte Platzierung des Fusionskäfigs (Abbildung 7 und Abbildung 8).
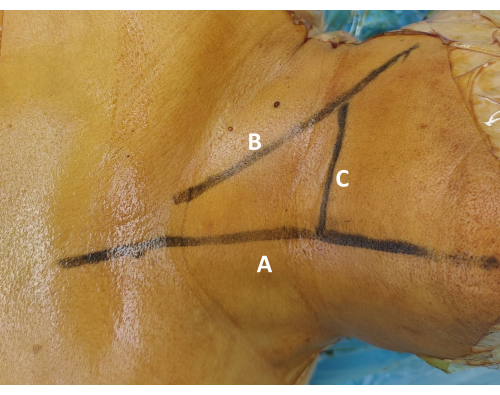
Abbildung 1: Oberflächenmarkierung des chirurgischen Segments. (A) Zeichnen Sie die Mittellinienmarkierung entlang der Trachealmittellinie, um die chirurgische Symmetrie zu gewährleisten. (B) Zeichnen Sie die transversale Lokalisationslinie entlang des oberen Randes des Schlüsselbeins. Palpieren Sie den M. sternocleidomastoideus und den Krikoidknorpel, um diese Markierung zu steuern. (C) Bestätigen Sie die Markierung der Zielebene mit Hilfe der Durchleuchtungskontrolle und markieren Sie die entsprechende Hautprojektion der vorgesehenen Bandscheibe. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.

Abbildung 2: Präoperative Eingriffe bei der spinalen Endoskopie. (A) Intraoperative Positionierung der C-Bogen-Fluoroskopie. (B) Einbau eines Caspar-Retraktors. (C) Spinale Endoskopie. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
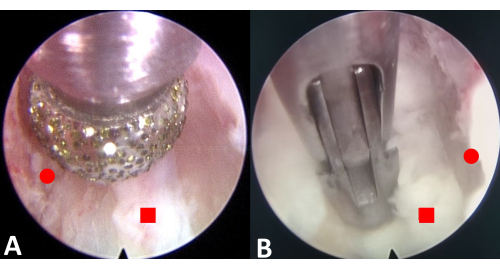
Abbildung 3: Endoskopische Exzision der Osteophyten und des Anulus fibrosus. (A) Entgraten Sie die oberen und unteren Osteophyten. (B) Den Anulus fibrosus resezieren. Der rote Kreis steht für den Osteophyten und das rote Quadrat für den Anulus fibrosus. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
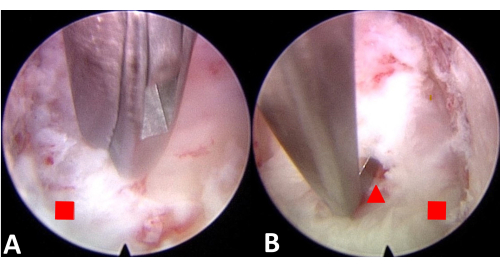
Abbildung 4: Endoskopische Inzision der PLL und Trennung der PLL vom Rückenmark, um Platz zu schaffen. (A) Inzision der PLL. (B) Trennen Sie die PLL vom Rückenmark. Das rote Quadrat stellt das hintere Längsband dar, das rote Dreieck das Rückenmark. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.

Abbildung 5: Endoskopische Exzision der Ossifikation. (A) Beurteilen Sie den Raum zwischen dem verknöcherten Gewebe und dem Rückenmark. (B) Das verknöcherte Band ist zu entfernen. Das rote Dreieck stellt das Rückenmark dar, der rote Pfeil zeigt auf die Verknöcherung des hinteren Längsbandes. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.

Abbildung 6: Hämostase. (A) Blutungspunkt. (B) Blutstillung unter endoskopischer Visualisierung. Das Sternchen stellt den Blutungspunkt dar. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
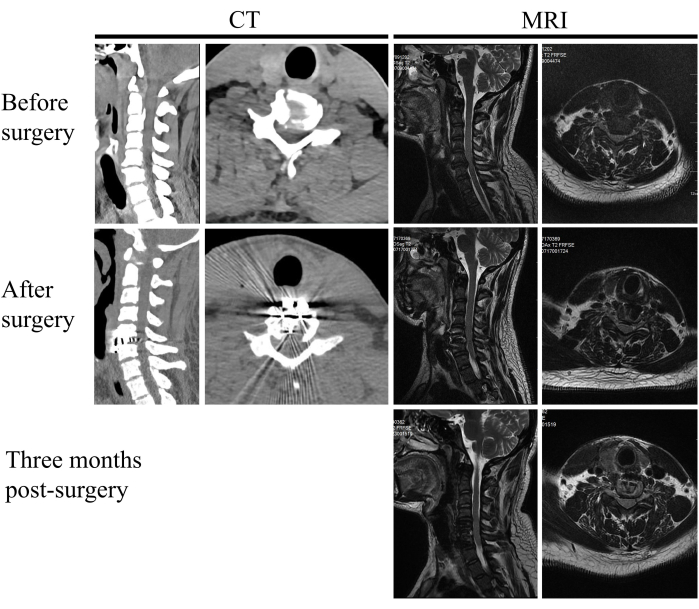
Abbildung 7: Prä- und postoperative Bildgebung. Ein Patient mit zervikaler spondylotischer Myelopathie vor der Operation, nach der Operation und 3 Monate nach der Operation. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
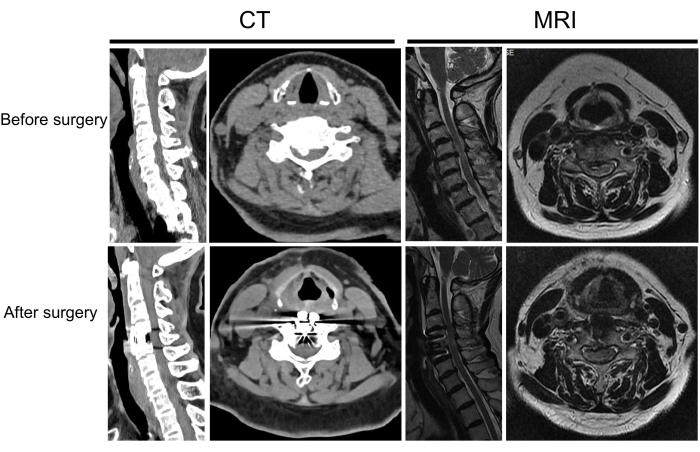
Abbildung 8: Prä- und postoperative Bildgebung eines anderen Patienten. Ein Patient mit zervikaler spondylotischer Myelopathie vor und nach der Operation. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
Tabelle 1: Patienteninformationen. Bitte klicken Sie hier, um diese Tabelle herunterzuladen.
Tabelle 2: Chirurgische Merkmale und postoperative Ergebnisse. Bitte klicken Sie hier, um diese Tabelle herunterzuladen.
Diskussion
Die anteriore zervikale Diskektomie und Fusion (ACDF) ist eine gängige chirurgische Methode zur Behandlung der zervikalen spondylotischen Myelopathie (CSM) und hat zufriedenstellende klinische Ergebnisse13,14. Die traditionelle Chirurgie steht jedoch vor Herausforderungen wie einem begrenzten Operationsfeld und Schwierigkeiten bei der Blutstillung. Besonders ausgeprägt sind diese Probleme bei einer Verknöcherung des hinteren Längsbandes (OPLL) oder einem Bandscheibenvorfall aus der Ferne; In diesen Fällen kann das Kompressionsmaterial intraoperativ nicht vollständig entfernt werden, und das Risiko einer Rückenmarksverletzung bleibt hoch15.
Mit den Fortschritten in der minimal-invasiven Wirbelsäulenchirurgie hat die Anwendung der mikroskopischen Endoskopie bei ACDF allmählich zugenommen, wodurch das Operationsfeld erweitert und die operative Präzision verbessert wurde. Das mikroskopgestützte Verfahren hat jedoch immer noch Einschränkungen, wie z.B. eine schlechte Hand-Auge-Koordination und blinde Flecken im Sichtfeld8. Die vollendoskopische anteriore zervikale Diskektomie (FACD) ist ein minimal-invasives Verfahren. Im Vergleich zur konventionellen Chirurgie reduziert die FACD die Schädigung des Weichgewebes, die Operationszeit und die Komplikationen erheblich. Der Genesungsprozess ist schnell, ohne dass zusätzliche chirurgische Eingriffe erforderlich sind16.
Die endoskopgestützte ACDF bietet jedoch mehrere Vorteile gegenüber der vollendoskopischen vorderen zervikalen Dekompression, insbesondere in Bezug auf die postoperative Stabilität, breitere Indikationen und eine einfache chirurgische Durchführung. Durch die Integration der interkorporalen Fusion mit einem Titankäfig und einer Plattenfixierung wird die segmentale Stabilität verbessert und das Risiko eines postoperativen Bandscheibenhöhenverlusts oder eines Rezidivs minimiert, was bei vollendoskopischen Techniken ohne Fusion ein Problem darstellt. Darüber hinaus eignet sich die endoskopgestützte ACDF besser für mehrstufige Erkrankungen, schwere Bandscheibendegenerationen und Fälle mit Ossifikation des hinteren Längsbandes (OPLL), bei denen eine vollendoskopische Dekompression unzureichend sein kann. Diese Technik bietet auch ein breiteres Operationsfeld, was eine umfassendere neuronale Dekompression ermöglicht und das Risiko einer Restkompression verringert. Darüber hinaus folgt es dem Standard-ACDF-Verfahren, was die Anwendung für Chirurgen im Vergleich zum technisch anspruchsvollen vollendoskopischen Ansatz erleichtert.
Während die vollendoskopische anteriore Dekompression für ausgewählte Fälle mit einstufigem Bandscheibenvorfall von Vorteil ist, bleibt die endoskopgestützte ACDF eine vielseitigere und reproduzierbarere Option für ein breiteres Spektrum von Erkrankungen der Halswirbelsäule. Die endoskopgestützte ACDF hat hervorragende klinische und radiologische Ergebnisse erzielt und eine zuverlässige Wirksamkeit und hohe chirurgische Sicherheit bewiesen. Wu et al.17. ergab, dass die endoskopgestützte ACDF signifikante Vorteile gegenüber der herkömmlichen ACDF bietet, darunter ein klareres Operationsfeld, weniger intraoperativer Blutverlust und ein geringeres Risiko für Nervenverletzungen. Sie berichteten jedoch auch von einer längeren Operationszeit aufgrund der Komplexität der endoskopischen Techniken. Unsere Ergebnisse stimmen mit ihren Ergebnissen überein, da unsere Studie auch eine leicht verlängerte Operationszeit bei endoskopgestützter ACDF zeigte. Nichtsdestotrotz hat die verlängerte Dauer keinen signifikanten Einfluss auf die klinischen Ergebnisse, und die Vorteile einer verbesserten Visualisierung und eines geringeren Traumas überwiegen diese Einschränkung, was die endoskopgestützte ACDF zu einer praktikablen Alternative zu herkömmlichen ACDF.As Als neues Vergrößerungswerkzeug für ACDF bietet die spinale Endoskopie eine klarere Visualisierung und eine größere operative Flexibilität, wodurch diese Probleme effektiv gelöst werden.
Die Vorteile der endoskopisch assistierten Operation sind wie folgt. Zunächst kann unter der spinalen Endoskopie die PLL detaillierter unterschieden werden, was eine scharfe Dissektion mit Kerrison-Stanzen ermöglicht. Das Endoskop bietet eine klarere Sicht auf das Rückenmark, so dass der Chirurg die Angemessenheit der Dekompression genau beurteilen und das Risiko einer Rückenmarksverletzung effektiv minimieren kann. Darüber hinaus ermöglicht die Verwendung eines Fräsers eine Operation in unmittelbarer Nähe, wodurch eine präzisere und gründlichere Entfernung von Knochensporen gewährleistet wird. Im Vergleich zum bloßen Auge und zum Mikroskop bietet das Endoskop eine bessere Visualisierung bei der Freilegung und Dekompression der beidseitigen freiliegenden Tebragelenke.
Zweitens bietet das Wirbelsäulenendoskop mit seinem integrierten 30°-Blickwinkel und dem verstellbaren Fräskopf eine erhöhte Operationsfreiheit, was einen breiteren Dekompressionsbereich ermöglicht. Diese Funktion erhöht die Flexibilität und Präzision bei der Arbeit in komplexen anatomischen Regionen. Drittens ermöglicht die wasservermittelte Endoskopie eine genauere Identifizierung von Blutungspunkten. Bei Blutungen am hinteren Rand des Wirbelkörpers kann die gekrümmte Radiofrequenzsonde die Blutungsstelle präzise erreichen und versorgen, was die hämostatische Wirksamkeit und die chirurgische Präzision erheblich verbessert. Viertens minimiert das endoskopische System die Interferenz durch die Hände des Chirurgen und reduziert die Anzahl der toten Flecken im Operationsfeld. Das koaxiale Design des Endoskops passt sich den Operationsgewohnheiten endoskopischer Chirurgen an, verhindert Instrumentenkollisionen und sorgt für reibungslosere und effizientere Eingriffe.
Die Anwendung endoskopischer Techniken der Wirbelsäule bringt jedoch auch gewisse Herausforderungen mit sich, wie z. B. eine verlängerte Operationszeit und die Anforderung an Chirurgen mit fortgeschrittenen chirurgischen Fähigkeiten und detaillierten Kenntnissen der Mikroanatomie. Obwohl die endoskopische Chirurgie ein breiteres Gesichtsfeld bietet, kann das Feld in extrem komplexen Fällen immer noch eingeschränkt sein. Mit der kontinuierlichen Weiterentwicklung der Technologie und der Verbesserung der chirurgischen Instrumente glauben wir, dass der Einsatz der Wirbelsäulenendoskopie in der Halswirbelsäulenchirurgie allmählich ausgereift sein wird und dass die Operationszeit weiter verkürzt wird.
Offenlegungen
Die Autoren haben keine Interessenkonflikte anzugeben.
Danksagungen
Nichts
Materialien
| Name | Company | Catalog Number | Comments |
| 75% alcohol | Hebei Ruihe Medical Equipment Co., Ltd | CC-01A | PEEK |
| Anterior Cervical Nail Plate Fixation System | Hebei Ruihe Medical Equipment Co., Ltd | PN-03 | Plate:TA3G, Nail:TC4 |
| Cervical Fusion Cage | |||
| cisatracurium besylate | SPINENDOS GmbH | SP081430.030 | Inner diameter:4.3 mm; Outer diameter:7.0 mm; Field angle: 80 °; Visual angle: 30 °; Working length: 181 mm |
| Endoscope system | SPINENDOS GmbH | SP082628.351 | Φ2.5 mm × 310 mm |
| Endoscopic forceps | SPINENDOS GmbH | SP082700.040L | Φ4.0 mm × 360 mm |
| Endoscopic hook | XIYI | MQZ | Φ3.2 mm × 328 mm |
| Endoscopic rongeur | ELLIQUENCE | DTF-40 | 40 cm |
| etomidate | SPINENDOS GmbH | SP082781.835 | Φ2.5 mm × 330 mm |
| High-speed burr | Neusoft Corporation | ||
| Interventional radiology | Ferrosan Medical Devices A/S | MS0010 | |
| iodine | Sichuan Guona Technology Co.,LTD | NNBP/40D/ | |
| Neusoft PACS/RIS | Elliquence, LLC | DTF-40 | |
| n-HA/PA66 | SPINENDOS GmbH | SP082615.265 | Φ7.2 mm × 178 mm |
| sufentanil citrate injection | |||
| SURGIFLO Haemostatic Matrix | |||
| Trigger-Flex Bipolar System | |||
| Working sheath |
Referenzen
- Bakhsheshian, J., Mehta, V. A., Liu, J. C. Current diagnosis and management of cervical spondylotic myelopathy. Global Spine J. 7 (6), 572-586 (2017).
- McCormick, J. R., Sama, A. J., Schiller, N. C., Butler, A. J., Donnally, C. J. Cervical spondylotic myelopathy: A guide to diagnosis and management. J Am Board Fam Med. 33 (2), 303-313 (2020).
- Visocchi, M., et al. Hybrid implants in anterior cervical decompressive surgery for degenerative disease. J Craniovertebr Junction Spine. 12 (1), 54-60 (2021).
- Lee, C. J., Boody, B. S., Demeter, J., Smucker, J. D., Sasso, R. C. Long-term radiographic and functional outcomes of patients with absence of radiographic union at 2 years after single-level anterior cervical discectomy and fusion. Global Spine J. 10 (6), 741-747 (2020).
- Luo, H. T., et al. Meta-analysis of the treatment of cervical spondylosis by microscopy-assisted and traditional anterior cervical decompression under direct vision. Chin J Tissue Eng Res. 24 (9), 1369-1377 (2020).
- Marawar, S., et al. National trends in anterior cervical fusion procedures. Spine (Phila Pa 1976). 35 (15), 1454-1459 (2010).
- Bollati, A., Galli, G., Gandolfini, M., Marini, G., Gatta, G. Microsurgical anterior cervical disk removal without interbody fusion. Surg Neurol. 19 (4), 329-333 (1983).
- Damodaran, O., Lee, J., Lee, G. Microscope in modern spinal surgery: Advantages, ergonomics and limitations. ANZ J Surg. 83 (4), 211-214 (2013).
- Liu, L., Dong, J., Wang, D., Zhang, C., Zhou, Y. Clinical outcomes and quality of life in elderly patients treated with a newly designed double tube endoscopy for degenerative lumbar spinal stenosis. Orthop Surg. 14 (7), 1359-1368 (2022).
- Han, S., et al. Clinical application of large channel endoscopic systems with full endoscopic visualization technique in lumbar central spinal stenosis: A retrospective cohort study. Pain Ther. 11 (4), 1309-1326 (2022).
- Liang, J., Li, H., Tao, Y., Yuan, W., Wang, H. Efficacy and complications of unilateral biportal endoscopic spinal surgery for lumbar spinal stenosis: A meta-analysis and systematic review. World Neurosurg. 159, e91-e102 (2022).
- Tian, X., Rudd, S., Yang, D., Ding, W., Yang, S. Anterior cervical hybrid decompression and fusion surgery to treat multilevel cervical spondylotic myelopathy. J Vis Exp. (196), e65034 (2023).
- Sun, X., et al. The frequency and treatment of dural tears and cerebrospinal fluid leakage in 266 patients with thoracic myelopathy caused by ossification of the ligamentum flavum. Spine (Phila Pa 1976). 37 (12), E702-E707 (2012).
- Wang, T., et al. Anterior cervical discectomy and fusion versus anterior cervical corpectomy and fusion in multilevel cervical spondylotic myelopathy: A meta-analysis. Medicine (Baltimore). 95 (49), e5437 (2016).
- Nakajima, H., et al. Long-term outcome of anterior cervical decompression with fusion for cervical ossification of posterior longitudinal ligament including postsurgical remnant ossified spinal lesion. Spine (Phila Pa 1976). 44 (24), E1452-E1460 (2019).
- Ruetten, S., Komp, M., Merk, H., Godolias, G. Full-endoscopic anterior decompression versus conventional anterior decompression and fusion in cervical disc herniations. Int Orthop. 33 (6), 1677-1682 (2009).
- Wu, Z. P., Wei, Z. Y., Song, X. L. Comparison of efficacy between endoscope-assisted anterior cervical discectomy and fusion (ACDF) and open ACDF in the treatment of single-segment cervical spondylotic myelopathy. J Orthop Surg Res. 19 (1), 35 (2024).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenWeitere Artikel entdecken
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten