Method Article
Semptomatik Uterin Fibroidlerin Tedavisinde Uterin Arterlerin Embolizasyonunun Lublin Protokolü
* Bu yazarlar eşit katkıda bulunmuştur
Bu Makalede
Özet
Burada, semptomatik uterin fibroidlerin tedavisi için beş bölüme ayrılmış bir uterin arter embolizasyon yöntemi sunuyoruz: kalifikasyon, hazırlık, performans, işlem sonrası bakım ve takip ziyaretleri. Bu protokol, jinekologlar ve girişimsel radyologlar arasında yakın işbirliği gerektirir ve yukarıdaki prosedürün uygun şekilde yürütülmesini sağlar.
Özet
Uterus miyomları, uterus kası stromasını oluşturan düz kas dokusundan köken alan iyi huylu tümörlerdir. Rahim miyomları kadınlarda en sık görülen iyi huylu tümörlerdir. Kadınların %20-50'sinde miyomlar asemptomatiktir ve herhangi bir tedavi gerektirmez. Rahim miyomlarının ana semptomları bol adet kanaması, anormal uterin kanama ve bası semptomlarıdır. Basınç semptomları pelvik ağrı sendromuna, idrara çıkma bozukluklarına ve kabızlığa neden olabilir.
Şu anda kullanılan tedavi yöntemleri arasında cerrahi tedavi, farmakolojik tedavi ve minimal invaziv prosedürler yer almaktadır. En sık uygulanan minimal invaziv yöntem rahim atardamarlarının embolizasyonudur. Bu prosedür şu anda semptomatik uterin fibroidler için yaygın olarak kabul edilen bir tedavi yöntemidir ve Ulusal Sağlık ve Klinik Mükemmellik Enstitüsü tarafından ağır adet kanaması kılavuzlarında bu şekilde kabul edilmiştir.
Bu karmaşık bir prosedürdür ve jinekologlar ile girişimsel radyologlar arasında yakın işbirliği gerektirir. Semptomatik uterin fibroidlerin tedavisinde uterin arter embolizasyonu için geçerli bir protokol sunuyoruz. Protokol beş bölüme ayrılmıştır. İlk iki bölüm jinekologlar ve girişimsel radyologlar için tasarlanmıştır ve bir hastanın embolizasyon için adım adım nasıl nitelendirileceğini ve hazırlanacağını açıklar. Girişimsel radyologlara yönelik olan üçüncü bölümde embolizasyonun nasıl yapılması gerektiği anlatılmaktadır. Dördüncü bölüm, embolizasyondan sonra hastalara bakan jinekologlara veya hastane koğuş doktorlarına yöneliktir. Protokolün bu bölümü, Hasta Kontrollü Analjezi (PCA) pompası kullanılarak embolizasyon sonrası ağrıyı tedavi etmek için bir yöntem sunar. Beşinci bölüm, uterin arter embolizasyonunun etkilerinin ve geç komplikasyonlarının değerlendirilmesi ile prosedürü tamamlar.
Beş bölümün tümü, alanda yeni olan klinisyenlere, uzmanlara ve araştırmacılara yönelik tek tip bir protokol oluşturur.
Giriş
Uterus miyomları, uterus kası stromasını oluşturan düz kas dokusundan köken alan iyi huylu tümörlerdir. Kollajen, fibronektin ve proteoglikan içeren çok miktarda hücre dışı maddeden oluşan monoklonal tümörlerdir. Miyomlar, sıkıştırılmış kas lifleri, kollajen lifleri, nörolifler ve kan damarlarındanoluşan ince bir psödokapsül ile çevrilidir 1,2. Miyomların patofizyolojisi tam olarak anlaşılamamıştır, ancak esas olarak seçici ve dokuya özgü epigenetik değişikliklerin neden olduğu monoklonal proliferasyona dayanıyor gibi görünmektedir3. Uterus fibroidlerine neden olan tek bir gen bulunamamıştır. Bununla birlikte, çoklu kutanöz ve uterus leiomyomatozis gibi nadir uterus fibroid sendromlarının varlığı, Krebs döngüsü4'te yer alan bir mitokondriyal enzim olan fumarat hidratazı kodlayan bir gene bağlanmıştır. Miyomların %50'sinde ortaya çıkan 7, 12 ve 14. kromozomlarda kromozom 7 delesyon ve translokasyonlarının varlığı primerdeğil sekonder görünmektedir 5,6,7.
Rahim fibroidlerinin büyümesinin düzenleyicileri, yumurtalıklar (östrojenler ve progesteron) tarafından üretilen steroid hormonları, büyüme faktörleri, anjiyogenez ve apoptozdur. Yaş, erken menarş, Afrikalı-Amerikalı ırk, kalıtım, nulliparite, obezite, polikistik over sendromu, diyabet, hipertansiyon, D vitamini eksikliği, soya sütü kullanımı, alkol ve kafein tüketimi dahil olmak üzere uterus fibroidlerinin gelişimi için risk faktörleri de tanımlanmıştır8.
Rahim miyomları kadınlarda üreme organlarının en sık görülen iyi huylu tümörleridir. Bu tümörler ilk olarak 1793 yılında Londra'daki St George's Hastanesi'nde Matthew Baillie tarafından tanımlanmıştır. Mevcut epidemiyolojik veriler, uterus fibroidlerinin insidansını doğru bir şekilde belirtmemektedir, çünkü bunların büyük bir kısmı teşhis edilmemiştir. Uterus fibroidlerinin tüm hastaların %5.4 ila %77'sinde meydana geldiği tahmin edilmektedir. Amerika Birleşik Devletleri'nde prevalansı Avrupa'dan daha yüksektir, olası neden ırksal farklılıklardır8.
Doğurganlık çağındaki kadınlar arasında miyomların yaklaşık %30'u anormal uterin kanama şeklinde klinik belirtiler verebilir ve bu da hastalarda yetersiz kanlanma ile sonuçlanır9. Çoğu durumda, hastalarda uterusta bulunan küresel lezyonlar olan birden fazla myom vardır. Boyutları ve konumları değişebilir. Vakaların% 90'ında rahim gövdesinde bulunurlar. Çapları birkaç milimetreden 20 cm'yekadar olabilir 10.
FIGO (Fédération Internationale de Gynécologie et d'Obstétrique) sınıflandırması, endometriyumun yakınlığına bağlı olarak onları 0-8 arasında gruplara ayırır (sayı daha düşük, endometriyum daha yakın olacaktır) (Şekil 1)11. Vakaların yaklaşık% 50-75'inde fibroidler asemptomatiktir. Rahim miyomlarının en sık görülen belirtileri bol adet kanaması, anormal rahim kanaması ve bası belirtileridir. Miyomlar infertilite vakalarının yaklaşık %10'u ile ilişkilidir ve %1-3'ünde tek nedendir12. Asemptomatik uterin fibroidler genellikle sadece düzenli bir tıbbi kontrolden geçerken, semptomatik fibroidler tedavi için bir endikasyondur13.
Halen kullanılan rahim miyomları için tedavi yöntemleri arasında cerrahi tedavi, farmakolojik tedavi ve minimal invaziv prosedürler yer almaktadır 13,14,15,16,17,18. Cerrahi tedavi myomektomi (abdominal ve histeroskopik) ve histerektomiyi içerir. Hem miyomektomi hem de histerektominin yaşam kalitesi üzerinde olumlu bir etkisi vardır19. Histerektomi, geri dönüşü olmayan doğurganlık kaybı ile ilişkilidir; Bu nedenle, birçok kadın başka tedavi seçenekleri arar20.
Abdominal miyomektomi fertilitenin korunmasına izin verir. Miyomların büyüklüğüne ve sayısına ve ayrıca cerrahın tecrübesine bağlı olarak, bu işlem laparotomi veya laparoskopi ile yapılabilir. Kanamalar histerektomiye göre daha az sıklıkta olmasına rağmen, genel morbidite benzerdir. Histeroskopik myomektomi, abdominal miyomektomiye göre daha güvenli, daha az invaziv bir yöntemdir ve submüköz miyomların (FIGO 0) tedavisine olanak sağlar. Daha büyük tip 2 fibroidleri tamamen çıkarmak için sonraki histeroskopik prosedürler gerekebilir21.
Levonorgestrel salgılayan rahim içi araçlar, ağır adet kanaması için etkili bir tedavi yöntemidir, ancak miyomların boyutunu küçültmez. Deforme olmuş uterus boşluğu olan hastalarda kullanımları sınırlıdır. GnRH analogları esas olarak miyomların boyutunu ve perioperatif kan kaybını azaltmak için preoperatif bir ajan olarak kullanılır. Ayrıca histerektomi ve miyomektomi sırasında dikey insizyon yüzdesini azaltırken vajinal prosedür olasılığını arttırırlar20.
Kısa vadede, seçici progesteron reseptör modülatörleri myom hacmini azaltır ve amenoreyi indükler. Bununla birlikte, uzun vadeli etkinlik ve güvenlik daha fazla araştırma gerektirir. Aromataz inhibitörleri ile birlikte, aneminin ameliyat öncesi tedavisi ve myom hacminin azaltılması için başka seçenekler de olabilir22. Bazı çalışmalar, D vitamininin fibroidlerin büyümesini ve semptomların başlamasını yavaşlatabileceğini veya önleyebileceğini düşündürmektedir23.
Nanopartiküllerle birleştirilmiş 2-metoksiestradiol kullanan yeni yöntemler de geliştirilme aşamasındadır24. Miyomların tedavisinde kullanılan minimal invaziv yöntemler arasında uterin arter embolizasyonu (BAE), manyetik rezonans kılavuzluğunda odaklanmış ultrason cerrahisi (MRgFUS), laparoskopik uterin arter tıkanıklığı (LUAO) ve radyofrekans miyolizi yer alır14,25. Ultrason kılavuzluğunda Yüksek Yoğunluklu Odaklanmış Ultrason (US-HIFU) yeni, hala deneysel, minimal invaziv bir yöntemdir26,27.
Terapötik damar tıkanıklığı ve uterusa giden kan akışını bloke etme yöntemleri 120 yıldan fazla bir süre önce belirtilmiştir. 1894'te Kelly, inatçı pelvik kanamayı kontrol etmek için onkolojik bir histerektomi sırasında iç iliak arterlerin ligasyonunu sundu, bu o zamanlar cerrahi prosedürden sonra yaygın bir komplikasyondu28. Daha sonra, Sack (1973), forseps doğumundan sonra masif doğum sonrası kanamanın tedavisinde aynı tekniğin etkin kullanımını tanımlamıştır. Her iki durumda da histerektomi yapılmadan hemostaz sağlandı29. 1979'da Heaston ve ark. ve Brown ve ark., doğum sonrası kanamayı kontrol etmek için emilebilir jelatin süngerler kullanarak pelvik arterlerin embolizasyonunu bağımsız olarak tanımladılar30,31.
BAE ilk olarak 1991 yılında Fransa'da semptomatik uterin fibroidler için bir tedavi yöntemi olarak kullanılmıştır32. Başlangıçta miyomektomi sonrası kan kaybını azaltmak için kullanıldı. 1995 yılında Ravina ve ark. semptomatik uterin fibroidler için birincil tedavi yöntemi olarak bu prosedürü önermiştir33. Amerika Birleşik Devletleri'nde, uterin arter embolizasyonu 1997'de başarıyla gerçekleştirildi34.
Semptomatik miyomlu kadınlarda uterusun korunmasına artan ilgi, BAE'yi minimal invaziv miyom tedavisinde ön plana çıkarmaktadır 14,18,35,36,37. 2000 yılında, Kraliyet Kadın Doğum Uzmanları ve Jinekologlar Koleji ve Kraliyet Radyologlar Koleji Ortak Çalışma Grubu, BAE ile ilgili kılavuzlar yayınlamak için kuruldu. O zamanlar, BAE deneysel bir yöntem olarak kabul edildi (dünya çapında 7.000'den az prosedür gerçekleştirildi). Kılavuzların yayınlanmasından bu yana, dünya çapında 100.000'den fazla BAE prosedürü gerçekleştirilmiştir. Ayrıca, BAE'yi diğer cerrahi prosedürlerle karşılaştıran beş randomize kontrollü çalışma yapılmıştır. Araştırma sonuçları, BAE'nin kısa ve orta vadede (birkaç yıla kadar) oldukça etkili olduğunu ve düşük orta (örneğin rahim enfeksiyonu) ve ciddi (yaşamı tehdit eden) komplikasyon riski olduğunu göstermektedir38,39. Randomize çalışmalarda, daha kısa hastanede yatış süreleri, daha hızlı iyileşme ve günlük aktivitelere dönüş BAE lehine konuşmaktadır. Cerrahi prosedürlerin daha ucuz olduğu ve daha az sıklıkta yeniden müdahale gerektirdiği kanıtlanırken, istatistiksel anlamlılık korunmuştur32. Bu prosedür şu anda semptomatik uterus fibroidleri için yaygın olarak kabul edilen bir tedavi yöntemidir ve Ulusal Sağlık ve Klinik Mükemmellik Enstitüsü (NICE) tarafından ağır adet kanamasıkılavuzlarında bu şekilde kabul edilmiştir 40.
Şu anda, Avrupa, Kuzey Amerika ve Avustralya'dan bilimsel topluluklar tarafından oluşturulan semptomatik uterin fibroidlerin tedavisinde BAE'nin kullanımına ilişkin 11 öneri bulunmaktadır. Çoğu durumda, öneriler tutarlıdır, ancak sapma iki tutarsızlıkla ilgilidir. Birincisi, saplı submukozal (FIGO 0) ve subserozal (FIGO 7) miyomun BAE için kontrendikasyon olup olmadığıdır. İkincisi, gelecekteki hamilelik ilan eden kadınların bu prosedür için uygun olup olmayacağıdır41. Amerikan Kadın Doğum Uzmanları ve Jinekologlar Koleji (ACOG) (2008) uterus fibroidlerinin tedavisi için ilginç bir kılavuz sunmuştur. Tutarlı bilimsel kanıtlara (Seviye A) dayanarak, ACOG, BAE'yi fibroidlerin tedavisi için tipik endikasyonlarla uterusu korumak isteyen uygun nitelikli kadınlar için etkili ve güvenli bir yöntem olarak tanımladı. Aynı zamanda, ACOG önerileri jinekologlar ve girişimsel radyologlar arasında yakın işbirliğine duyulan ihtiyacı vurguladı. Yayınlanan kılavuzlarda, ACOG doğurganlığı koruma arzusunu tek kontrendikasyon (göreceli) olarak kabul etti42.
En son önerilerden biri 2013 yılında Kraliyet Kadın Doğum Uzmanları ve Jinekologlar Koleji (RCOG) ve 2015 yılında Kanada Kadın Doğum Uzmanları ve Jinekologlar Derneği (SOGC) tarafından yayınlanmıştır41. Bu makalenin geri kalan kısmında yazarlar yukarıdaki önerileri kullanacaklardır. RCOG ve SOGC yönergelerine göre, semptomatik miyomlu herhangi bir hasta, kontrendikasyon olmaması ve prosedürün faydalarının (semptomların çözülmesi) komplikasyon riskinden daha ağır basması koşuluyla embolizasyon için aday olabilir. Uterus fibroidlerinin minimal invaziv bir prosedür olarak embolizasyonunun ihmal edilebilir sayıda ciddi komplikasyon taşıdığı unutulmamalıdır. Bu nedenle, çoğu durumda faydalar komplikasyon riskinden daha ağır basar 14,32,43.
BAE sonrası yüksek klinik etkinlik ve komplikasyonların önlenmesi için uygun bir hasta yeterliliği çok önemlidir. BAE'nin ana endikasyonu semptomatik uterus fibroidleridir ve ağır adet kanaması, dismenore, ağrı, disparoni ve idrar veya gastrointestinal sistem üzerindeki diğer olumsuz etkilere neden olur. Miyomları adenomyozdan veya adenomyozis ile birlikte var olan miyomlardan ayırt etmek gerekir, çünkü böyle bir durumda BAE daha az etkilidir ve prosedür tekniğinindeğiştirilmesini gerektirir 14,32,43,44,45,46,47. Semptomatik uterus fibroidleri olan kadınlarda BAE prosedürünü gerçekleştirmek için spesifik endikasyonlar arasında ameliyatın reddedilmesi, kan transfüzyonu için rıza olmaması ve daha önce başarısız uterus fibroidleri ameliyatı yer alır.
Yukarıdaki endikasyonlarda BAE cerrahi tedaviye alternatif olarak tedavi edilmelidir. Bununla birlikte, az sayıda vakada, işlem sonrası komplikasyonların cerrahi müdahale ihtiyacına yol açabileceği hastalara bildirilmelidir 14,32,43. RCOG yönergelerine göre, BAE'nin miyomun olası bir kısırlık nedeni olduğu bir durumda kullanılması, kısırlık ve yardımlı üreme tedavisinde uzmanlaşmış bir jinekoloğun özel bakımı ve uygun değerlendirmesini gerektirir. Miyomların varlığına bağlı kısırlık mutlak değildir ve birçok kadın herhangi bir müdahale olmadan hamile kalacaktır. Bu nedenle, erkek partnerindeğerlendirilmesi de dahil olmak üzere diğer olası kısırlık nedenlerini dışlamak mantıklıdır 14,32,43.
Bu nedenle, RCOG ve SOGC'nin önerilerine göre, adaylar, fibroid benzeri klinik semptomları olan pelvisteki patolojilerin dışlandığı semptomatik uterin fibroidleri olan kadınlar olmalıdır41,43.
Bu prosedürün mutlak kontrendikasyonları arasında mevcut veya yeni genital enfeksiyon, klinik faktörlere veya yetersiz görüntülemeye bağlı tanısal şüpheler, asemptomatik fibroidler, yaşayabilir gebelik ve radyolojik kontrast maddelerin kullanımı için kontrendikasyonlar yer alır.
Göreceli kontrendikasyonlar arasında, teorik olarak pedinkül nekrozu nedeniyle endometriyumdan ayrılabilen ve nadir durumlarda sepsis ile sonuçlanan saplı submukozal (FIGO 0) ve subserozal (FIGO 7) fibroidler bulunur. Bu durumlarda, BAE sadece işlem planlanmadan önce saplı miyomun histeroskopik veya laparoskopik olarak çıkarılması durumunda düşünülmelidir.
Mevcut literatürün miyomun boyutunun kendi başına bir kontrendikasyon olmadığını öne sürmesine rağmen, deneyimler, büyük miyomlu (özellikle kompresyon semptomlarıyla ilişkili) hastaları BAE için nitelendirirken son derece dikkatli olunması gerektiğini göstermektedir, çünkü hacimdeki azalma semptomları hafifletmek ve hasta beklentilerini karşılamak için yetersiz olabilir14,32, 43,48.
BAE'den sonra başarılı gebeliğe dair birçok rapor vardır, ancak mevcut kanıtlar genç kadınlarda farmakolojik veya cerrahi tedaviye (myomektomi) alternatif olarak kullanımını tam olarak desteklememektedir49. Bu nedenle, hamile kalma isteğini beyan eden kadınlarda bu işlem çok dikkatli kullanılmalıdır (çünkü BAE'den sonra miyomektomi sonrasına göre daha düşük gebelik oranı, daha yüksek düşük oranı, uterus rüptürü, plasenta akretası ve olumsuz gebelik sonuçları vardır)32,50,51,52,53,54,55. Jinekologlar olarak, hamilelik arayan kadınlar için BAE'yi önermiyoruz. Bizim için, tedavi eksikliğinin yaşamı tehdit edebileceği ameliyat veya kan nakli için reddetme gibi BAE için ek endikasyonlar olması koşuluyla, göreceli bir kontrendikasyondur.
RCOG yönergelerine göre, semptomatik uterin fibroidleri olan genç kadınlarda doğurganlığı koruma veya iyileştirme arzusu, BAE32'ye göreceli bir kontrendikasyondur. Buna karşılık, SOGC kılavuzları, benzer durumlarda BAE'nin fibroidler için bir tedavi seçeneği olarak önerilmemesini önermektedir, çünkü bu tür kadınlarda güvenlik ve etkinlik belirlenmemiştir14,43. Benzer bir bakış açısı, Amerikan Üreme Tıbbı Derneği (ASRM), Amerikan Kadın Doğum Uzmanları ve Jinekologlar Koleji (ACOG), Amerikan Radyoloji Koleji (ACR), Avustralya Kraliyet ve Yeni Zelanda Kadın Doğum Uzmanları ve Jinekologlar Koleji (RANZCOG) ve diğerleri dahil olmak üzere diğer bilimsel topluluklar tarafından temsil edilmektedir ve miyomektomi sonrası doğurganlık sonuçlarının arttığını belirtmektedir 41,43,56. BAE, özellikle miyomektomi (çoklu fibroidler) için elverişsiz özelliklere sahip, doğurganlığı korumak veya iyileştirmek isteyen kadınlar için yalnızca NICE tarafından önerilmiştir57.
Genel olarak, BAE prosedürleri adet döngüsünün herhangi bir aşamasında gerçekleştirilebilir32. Ancak döllenme veya implantasyon aşamasında gebeliği dışlamak için ideal bir yöntem olmadığını varsayarsak, erken gebeliği dışlamak için merkezimizde 10. siklus gününe kadar yapılmaktadır. Çoğu durumda, hastalar işlem günü jinekoloji servisine kabul edilir. Uygun muayeneler ve jinekolojik konsültasyon sağlandığı takdirde bir hastanın vasküler cerrahi servisine kabul edilmesine izin verilir. Bir jinekolog ve bir girişimsel radyolog, miyomların embolizasyonu için kalifikasyon gerçekleştirir. Jinekolojik yeterlilik, tıbbi öykü, muayene, üreme organının ultrason değerlendirmesi ve miyom tipini içerir. Ek olarak, rahim içindeki herhangi bir maligniteyi dışlamak için servikal (PAP) smear ve endometriyal biyopsi gereklidir. Yumurtalıkların ultrason taramasının şüpheli olduğu durumlarda ROMA testi (Over Malignitesi Riski Algoritması) gereklidir.
Tartışılması gereken ayrı bir konu uterus sarkomu, özellikle de bu uterus tümörlerinin %70'ini oluşturan leiomyosarkomdur (LMS). Miyom nedeniyle ameliyat edilen hastalarda LMS prevalansı düşüktür ve %0,13-%0,29 olarak tahmin edilmektedir58,59. LMS insidansındaki artış 40 yaş üstü kadınlarda görülmektedir. LMS'nin iyi huylu miyomlara benzeyebileceği için tedaviden önce teşhis edilmesi zordur60. Çoğu LMS'nin önceden var olan miyomlarla ilgisi yoktur ve LMS'nin uterus miyomları ile bir ilişkisi olduğuna dair bir kanıt yoktur61. Hem uterus fibroidleri hem de LMS hızla büyüme eğilimindedir. Bu nedenle, boyut veya büyüme hızı malign uterus tümörü için bir risk faktörü değildir60.
Şu anda, leiomyosarkomu net bir şekilde tanımlamamıza ve leiomyoma60,62'den ayırt etmemize izin verecek güvenilir laboratuvar veya görüntüleme testleri yoktur. Leiomyosarkom tanısında endometrial biyopsinin duyarlılığı %86'dır. Bu nedenle, negatif bir biyopsi sonucu, kötü huylu bir uterus tümörünün varlığını dışlamaz. Kontrastlı MRG şu anda uterus tümörleri için en uygun tanı yöntemidir. LMS tanısında bu testin duyarlılığı %94 60'tır.
Daha önce de belirtildiği gibi, yukarıdaki testler malign uterus tümörlerinin% 100'ünü dışlamaz. Bu nedenle, uterus tümörünün histopatolojik olarak doğrulanması olasılığı olmadan, tedaviden sonra LMS tanısını uzatma riski vardır. BAE kalifikasyonu sırasında hasta bu konuda bilgilendirilmelidir.
Tam kan sayımı (CBC) ve pıhtılaşma testleri (INR, APTT), renal panel (kreatinin, üre), tiroid uyarıcı hormon (TSH), foliküler fazda anti-Müllerian hormon (AMH) (önerilir) veya folikül uyarıcı hormon (FSH) konsantrasyonu, C-reaktif protein (CRP), genel idrar testi ve vajinal smear (aerobik vajinal kültür) yapılması, embolizasyon sonrası olası komplikasyonların (enfeksiyonlar, iyatrojenik over hasarı, Gadolinyum bazlı kontrast maddelerden sonra önceki böbrek yetmezliğinin yoğunlaşması, iyot bazlı kontrast madde sonrası hipertiroidi vakalarında tirotoksikoz)63,64. FSH testinin 40 yaşın altında önerilmediğini lütfen unutmayın, çünkü FSH genç kadınlardayumurtalık rezervindeki değişikliklerin hassas bir göstergesi değildir 50,65.
Girişimsel bir radyolog, hastaları tıbbi geçmişe ve manyetik rezonans görüntülemeye (MRI) dayalı olarak prosedür için nitelendirir. Tıbbi öykü toplanırken, prosedürün kendisi kadar yararları ve olası komplikasyonlar da hastayla tartışılmalıdır. Hastanın BAE ile ilgili beklentileri de tartışılmalıdır. MRG, üreme organı ve komşu yapıların diğer patolojilerini dışlamanın yanı sıra, prosedürün teknik fizibilitesi için fibroidlerin ve anatominin morfolojisini ve yerini değerlendirmeyi amaçlar 35,36,37,57.
BAE, rahim, yumurtalıklar ve pelvis içindeki çevre dokulara kan akışını sürdürürken tüm miyomların damar sistemini tamamen bloke etmeyi amaçlamaktadır. BAE'nin teknik yönleri hala bir dereceye kadar gelişiyor.
Uterin arterlerin embolizasyonu, intravasküler embolizasyon alanında uygun yetkinliğe sahip girişimsel radyologlar tarafından yapılır. İşlem floroskopi rehberliğinde gerçekleştirilir. Kasık bölgesindeki delinmeden femoral artere, aorta, internal iliak artere ve uterin artere kadar bir vasküler kateterin perkütan olarak yerleştirilmesini içerir. Kateter uterin arterin derinliklerine yerleştirildikten ve stabil bir pozisyon elde edildikten sonra, kontrast ile karıştırılan embolizasyon ajanı, reflü ve "hedef dışı" embolizasyonu önleyecek şekilde floroskopik kontrol altında enjekte edilir. Miyomların vasküler yatağı, embolizasyon materyalinin tipine bağlı olarak 500-900 μm'lik partiküller kullanılarak kapatılır - normal boyutlar 700 μm'dir. Staz kan akımı sağlanana kadar embolizasyona devam edilir. İşlemin sonunda kateter çıkarılır ve damar erişim yeri manuel basınç ve pansuman veya mekanik kapatıcı ile sabitlenir. İşlem yaklaşık 0,5-1,0 saat sürer. BAE sırasında yumurtalık tarafından emilen ortalama iyonlaştırıcı radyasyon dozu 0.04-0.22 (Gy: gri) arasında değişir ve ortalama tahmini etkili doz 22-34 (mSv: millisievert) arasında değişir. Ortalama floroskopi süresi yaklaşık 22 dk 66,67'dir.
Çoğu miyomun damar sistemi uterus arterlerinden gelir. Miyomların sadece yaklaşık %5-10'u ek olarak yumurtalık arterleri tarafından sağlanır. Arteriyel uterus anastomozları vakaların yaklaşık% 10'unda, utero-over% 10-30'unda görülür. Embolize dokulara kan akışının kesilmesi iskemik nekroza, ardından hiyalin dejenerasyonuna veya pıhtılaşma nekrozuna neden olur. Bu süreç birkaç ay sürer 68,69.
BAE'nin etkinliği, semptomların çözülmesine veya azalma derecesine bağlıdır. Aşırı adet kanaması, pelvik ağrı ve basınç semptomlarının tedavisi için BAE için klinik etkinlik indeksi sırasıyla %81-96, %70-%100 ve %46-%100'dür. İşlemden sonraki 3-6 ay içinde miyom hacminde gözlenen azalma %25-%60 idi 33,70,71,72. Miyomun ortalama çap küçülmesi 2.2 cm57 idi.
Miyom hacmindeki azalma her zaman klinik semptomların düzelmesi veya azalması ile ilişkili değildir. BAE sonrası uzun süreli takipte, hastaların% 70'inden fazlası işlemden sonraki 5 yıl içinde klinik semptomlarda düzelme veya önemli ölçüde azalma bildirirken,% 16-23'ü yeniden müdahale gerektirdi73,74.
Erken BAE etkisini değerlendirirken, bu yayının yazarları, Sanal Organ Bilgisayar Destekli AnaLiz (VOCAL) kullanarak, vasküler indekslerin ölçümlerini gerçekleştiren üç boyutlu (3D) ultrasonun kullanılmasını önermektedir: vaskülarizasyon indeksi (VI), akış indeksi (FI) ve vaskülarizasyon akış indeksi (VFI)75.
Embolizasyon sonrası ağrı, başarılı BAE'nin (bir komplikasyonla karıştırılmamalıdır) erken (yaklaşık 24 saat süren) beklenen bir etkisidir ve aktif olarak tedavi edilmelidir. Bu klinik semptom, iskemik miyomun doku yıkım ürünlerinin salınmasından kaynaklanır. Tedavi, yeterli ağrı kontrolü, hidrasyon ve olası antibiyotik tedavisini içerir32,43. İşlemden sonra 24 saat boyunca sürdürülen epidural anestezi (EA), ağrıyı tamamen kabul edilebilir bir düzeye önemli ölçüde azaltır, ancak Hasta Kontrollü Analjezi (PCA) ile karşılaştırıldığında daha yüksek bir maliyet ve daha yüksek komplikasyon riski76.
Embolizasyon sonrası ağrı yönetimi derlemelerinde başka yaklaşımlar da mevcuttur. BAE sırasında ağrı kesici ilaçların polivinil alkol molekülleri ve elektroakupunktur anestezisi ile karışımlarının kullanılmasından bahsetmeye değer. Her iki yöntem de bir hastane ortamında gerçekleştirilen BAE prosedürlerinin sayısını sınırlamayı amaçlıyordu 77,78. İşbirliği yaptığımız ve işbirliği yaptığımız merkezlerde bu yöntemleri kullanmıyoruz.
BAE'nin erken komplikasyonları genellikle anjiyografi prosedürüne bağlı lokal komplikasyonlardır. Bu advers olay grubu nadirdir (vakaların% 1'inden daha azında görülür) ve esas olarak kasık hematomu, arteriyel tromboz, arteriyel diseksiyon ve psödo-anevrizma, kontrast maddelere alerjik reaksiyonlar, işlem sırasında damardaki kateterin manipülasyonu sonucu uterin arterde bir spazm ile ilgilidir (birkaç dakika geçtikten sonra geçici bir olay olarak kabul edilir ve işleme devam edilebilir, spazm devam ederse, Verapamil (2.5-5 mg) veya Nitrat (100-150 μg) intraarteriyal olarak verilebilir) ve "hedef olmayan" embolizasyon 32,37,38.
Diğer pelvik organların "hedef dışı" embolizasyonu ve müteakip iskemisi hakkında da birkaç rapor vardır. Bu komplikasyon, prosedürün kötü uygulanmasının bir sonucu olarak ortaya çıkabileceği gibi, anastomozların ve pelvik vaskülatür anatomik varyantlarının varlığına bağlı olarak da ortaya çıkabilir. Hedef dışı embolizasyonun özel bir durumu, bazı hastalarda rahim damarları ile yumurtalıklar arasındaki anastomozlardan kaynaklanan yumurtalık hasarıdır79,80.
Miyom nekrozunun sonucu, hastaların yaklaşık% 10-15'inde işlemden sonraki 30 gün içinde ortaya çıkan bir embolizasyon sonrası sendromdur. Birlikte veya tek tek ortaya çıkabilen bu sendromun belirtileri arasında bulantı, kusma, halsizlik, düşük dereceli ateş, alt karın ağrısı ve yüksek lökosit seviyeleri yer alır. Bu genellikle 10-14 gün içinde kaybolan kendi kendini sınırlayan bir sendromdur. Bu komplikasyonu tedavi etmek için analjezikler ve antienflamatuar ilaçlar kullanılır32. Embolizasyon sonrası sendromun semptomlarını sepsis gibi daha ciddi komplikasyonlarla ayırt etmek önemlidir. Bu, özellikle söz konusu semptomların iki haftadan uzun sürdüğü durumlarda geçerlidir 32,37,38.
Enfeksiyon potansiyel olarak BAE'den sonra en ciddi komplikasyondur ve vakaların yaklaşık% 0,5'inde görülür32,38. 24-48 saat boyunca devam eden, yüksek ateş (38.5 °C ve üzeri) ve sert ve ağrılı karın durumunda, sepsisten şüphelenilmelidir. Bu durumda, tedavi sadece antibiyotik tedavisinin kullanılmasını değil, aynı zamanda uterusun çıkarılması ihtiyacını da gerektirebilir. İkinci durumda, vakaların% 1'inden daha azında, hastanın hayatı için bir tehdit oluşturabilir. Sepsis, BAE büyük bir uterusta (20 cm'den fazla veya tek bir miyomun çapı 9 cm'den büyük olduğunda ve ayrıca büyük submukoz fibroidlerin bir arada bulunması durumunda) yapıldığında daha sık görülür37,38.
BAE'den sonra (işlemden 30 günden fazla), submukoz fibroidlerin embolizasyonundan sonra ortaya çıkan geç bir komplikasyon, fibroidlerin belirgin, nekrotik fragmanlarının servikal kanaldan atılmasıdır. Vakaların yaklaşık% 10'unda görülür 32,81,82. BAE'den sonra kadınların yaklaşık% 16'sı, nekrotik fibroidlerin uterustan atılmasının bir sonucu olarak birkaç haftadan birkaç aya kadar bol miktarda vajinal akıntıya sahip olabilir83. BAE prosedüründen sonra, menstrüasyonda önemli bir kısalma ve bolluğunda bir azalma gözlenir, bu da bu prosedürün yararlı bir etkisi olarak kabul edilir. Bununla birlikte, tam amenore, embolizasyon sonrası yumurtalık yetmezliğinin etkisi olarak ele alınır50,84.
BAE'den sonra amenore genellikle geçicidir ve birkaç döngü ile sınırlıdır. Kalıcı amenore, 40 yaşın üzerindeki kadınların yaklaşık% 15'inde ve bu yaşın altındaki kadınların yaklaşık% 1'inde görülür ve erken menopoz semptomlarına neden olur. Kendi araştırmamızda genç kadınlarda (33–40 yaş) yumurtalık rezervinin azalması sonucu doğurganlıkta azalma saptanmıştır65. BAE'den sonra amenore bildiren kadınların yaklaşık% 85'inin 45 yaşın üzerinde olduğu tahmin edilmektedir85. Yaşlı kadınlarda amenore insidansındaki artışın nedeninin, yumurtalık rezervinin azalması ve yumurtalık dokusunun "hedef dışı" embolizasyonun neden olduğu iskemiye daha fazla duyarlılığından kaynaklandığı ileri sürülmüştür86.
BAE prosedürü, prosedürden geçen kadınların cinsel işlevini de etkiler. BAE'den sonra cinsel fonksiyonun iyileşmesi kadınların% 26'sı tarafından bildirilmiştir,% 10'unda bozulma bulundu ve kadınların% 64'ünde değişme olmadı. Cinsel işlev bozukluğunun olası bir nedeni, BAE prosedürünün bir sonucu olarak klitoris, serviks ve korpus uteri'nin anormal damar sistemidir74.
Protokol
Yazarlar, protokolün Lublin Tıp Üniversitesi yerel Etik Komitesi'nin yönergelerini takip ettiğini beyan eder.
1. BAE prosedürü için yeterlilik
NOT: Bu, jinekologlara ve girişimsel radyologlara yöneliktir.
- Hastayı BAE prosedürünün detayları hakkında bilgilendirin.
- BAE prosedürü için endikasyonları ve kontrendikasyonları tartışın.
- Uterus fibroidlerinin tedavisinde BAE'nin varsayımlarını ve alternatif yöntemleri (Giriş'te açıklanmıştır) hastayla tartışın.
- UYARI! Hastaya BAE'nin radikal bir prosedür olmadığını bildirin (miyom çıkarılmayacaktır).
- UYARI! Hastaya, BAE'den sonra uterus fibroidlerinin histopatoloji raporunu almayacağını bildirin.
- UYARI! Hastaya 1.000 rahim tümöründen 1-3 vakasının malign (LMS) olabileceğini bildirin. BAE kalifikasyonu sırasında gerçekleştirilen endometriyal biyopsi ve MRG'nin leiomyosarkom tanısında oldukça hassas olduğunu, ancak %100 olmadığını hastayla tartışın. Hastayı leiomyosarkom için BAE yapmanın tanı ve uygun tedaviyi geciktirebileceği konusunda bilgilendirin. Bu gerçeği tıbbi kayıtlara not edin.
- Hasta bilerek BAE'nin yapılmasını istiyorsa bu Protokole devam edin.
- Kalifikasyonun iki aşamada gerçekleştiğini hastaya bildirin. Bir jinekolog tarafından kalifikasyon, endikasyonların ve kontrendikasyonların analizini içerirken, girişimsel bir radyolog BAE'nin teknik yeteneklerini değerlendirir.
- Bir jinekolojik konsültasyon planlayın veya gerçekleştirin ve BAE'den önce girişimsel radyolog ile bir konsültasyon planlayın.
- Mümkünse, poliklinikte mümkün olduğunca çok sayıda kalifikasyon prosedürü gerçekleştirin.
- Hastanın BAE için endikasyonları olduğundan emin olun: semptomatik uterus fibroidleri (menometroraji, metroraji, dismenore, disparoni, kronik pelvik ağrı); cerrahi tedavinin reddedilmesi; kan nakli için rıza yok; Daha önce başarısız uterin fibroids ameliyatı. Bunları tıbbi geçmişte not edin.
- Hastaya miyom (lar) ın semptomlarını sorun.
- BAE'nin etkinliğini ve hastanın beklentilerini tartışın ( Temsili Sonuçlarda).
- Hastanın daha önce rahim fibroidleri için tedavi edilip edilmediğini sorun. Hangi yöntemin kullanıldığından emin olun.
- Hasta cerrahi tedaviyi veya kan transfüzyonunu reddederse, yazılı bir ifade alın.
- BAE prosedürü için kalifiye olan hastanın mutlak kontrendikasyonları olmadığından emin olun: asemptomatik fibroidler; uygulanabilir bir hamilelik; mevcut veya yeni genital enfeksiyon; klinik faktörler veya yetersiz görüntüleme nedeniyle tanısal şüpheler; radyolojik kontrast maddelerin kullanımı için kontrendikasyonlar; MRG'de leiomyosarkomun özellikleri; Palyasyon için veya cerrahiye ek olarak yapılmadığı sürece rahim veya yumurtalık malign tümörü87. Bunları tıbbi geçmişte not edin.
- Hasta asemptomatik miyomlara rağmen BAE'yi talep ederse, bu tür vakaların prosedür için uygun olmadığını açıklayın. Hastaya asemptomatik miyomların sadece düzenli jinekolojik izleme gerektirdiğini açıklayın.
- BAE'ye göreceli kontrendikasyonlar varsa (büyük fibroidler ve üreme planları), bunları hastayla tartışın ve bu gerçeği tıbbi kayıtlara not edin.
- Giriş bölümünde açıklanan göreceli kontrendikasyonla ilgili olası komplikasyonlara odaklanın, hastanın prosedürü anladığından ve kabul ettiğinden emin olun.
- Uterin arter embolizasyonunun sonraki etkilerini ve komplikasyonlarını hastayla tartışın (girişe bakınız) ve bu gerçeği tıbbi kayıtlara not edin.
- Hastayla konuşurken, embolizasyon sonrası ağrıya özellikle dikkat edin.
- Embolizasyon sonrası ağrı tedavilerini tartışın.
- Jinekolojik bir yeterlilik gerçekleştirin.
- Tıbbi öykü toplayın ve jinekolojik muayene yapın.
- Miyomların boyutunu ve tipini değerlendirmek için üreme organlarının ultrason değerlendirmesini yapın (FIGO sınıflandırması)88.
- Miyomun boyutunu ve yerini tahmin etmek için vajinal bir prob kullanın (Şekil 2). BAE ile tedavi edilen uterus miyomları FIGO sınıflamasına göre 2-5 (ideal olarak 3-4) olmalı ve çap 10 cm'yi geçmemelidir.
- Pelvis ultrason taramasının protokolünü tıbbi kayıtlara dahil edin.
- Ultrason taraması sonucunun BAE prosedürü için yeterlilik için endikasyonlar verdiğinden emin olun.
- Pelvis içindeki malign süreçleri dışlayın.
- Hastanın servikal (PAP) smear ve endometriyal biyopsi için güncel (tercihen 6 ay içinde gerçekleştirilmiş) sonuçları olduğundan emin olun.
- Pelvik ultrason sırasında, yumurtalıkları değerlendirmek ve yapılarının doğru olduğunu doğrulamak için vajinal probu kullanın. Şüpheniz varsa, önceki ultrason taramasını kontrol edin veya ROMA testini gerçekleştirin.
- Rahim tümörünü LMS özellikleri ve BAE teknik yetenekleri açısından değerlendirmek için bir MRI sipariş edin.
- Servikal (PAP) smear, endometriyal biyopsi, ultrason taraması (muhtemelen ROMA testi) ve tıbbi kayıtlardaki MRG sonuçlarına dikkat edin.
- Sonuçlar yanlışsa, hastayı prosedürden diskalifiye edin.
- Hastaları jinekolojik kalifikasyonun sonuçları hakkında bilgilendirin.
- Bu gerçeği tıbbi kayıtlara not edin. Hastayı hastaneye sevk edin.
- BAE prosedürü için randevu alın ve hastanın döngünün 10. gününden önce olması gerektiğini unutmayın.
- Hastaya ameliyatı reddedip reddetmediğini sorun. Reddetme durumunda, hastanın bilgilendirilmiş onamında veya tıbbi kayıtta bu gerçeği not edin.
- Ameliyatı reddeden semptomatik fibroidleri olan hastalar BAE'ye hak kazanır.
- Potansiyel komplikasyonları değerlendirmek ve önlemek için BAE'den en az 7 gün önce aşağıdaki testleri yapın: vajinal smear'ın mikrobiyolojik testi (aerobik vajinal kültür); idrar tahlili; seçilmiş kan testleri: CBC, Pıhtılaşma testleri (INR, APPT), Renal panel (kreatin, üre), TSH, CRP.
- Sonuçları tıbbi kayıtta açıklayın.
- Hastaya, yanlış sonuçların onu prosedür için diskalifiye ettiğini bildirin.
- Foliküler fazda AMH (önerilen) veya FSH (40 yaş altı önerilmez) serum seviyelerini test ederek hastanın yumurtalık rezervini kontrol edin. Yukarıdaki testin, hedef olmayan embolizasyonun bir sonucu olarak yumurtalık hasarını değerlendirmede yardımcı olacağını hastayla tartışın. Bu gerçeği tıbbi kayıtlara not edin.
- BAE'ye hak kazanan hastalar, gebelik komplikasyonları riskinin artması nedeniyle hamile kalma iradesini beyan etmemelidir 14,32,38,50,51,52,89,90,91.
- BAE'den sonra artan gebelik komplikasyonları riski hakkında hastayı bilgilendirin.
- Hastanın bilgilendirilmiş onamında veya tıbbi kayıtta hamile kalma isteğini beyan etmediğine dikkat edin.
- Hasta gelecekte hala hamileliği dışlamıyorsa, ancak BAE'ye ihtiyaç duyuyorsa, BAE'den sonra olası gebelik komplikasyonları hakkında bilgilendirildiğine dair yazılı bir beyanda bulunun.
- Radyolojik kalifikasyon gerçekleştirin.
- Pelvik MRG'nin yapıldığından emin olun. MRG incelemesi, üreme organının ve bitişik yapıların diğer patolojilerinin dışlanmasına (BAE prosedürü için yeterlilik aşamasının 1.6.3.3.), fibroidlerin morfolojisini ve yerini ve embolizasyonun teknik fizibilitesi için anatomiyi değerlendirmeye izin verir (Şekil 3, Şekil 4). Değilse, MRG incelemesini ve girişimsel bir radyolog ile konsültasyonu düzenleyin.
- Görüntüleme incelemelerini analiz edin ve miyomların tipini ve boyutunu değerlendirin.
- Submukozal (FIGO 0-1) fibroidler bulunursa, hastayı uterus boşluğuna dökülme riski hakkında bilgilendirin. Tam atılım sepsise neden olabilirken, fragmanlardaki atılım genellikle asemptomatiktir50.
- Subserozal dar saplı, saplı (FIGO 7) miyomlar bulunursa, hastayı miyomun embolizasyon sonrası karın boşluğuna ayrılması riski hakkında bilgilendirin. Akut inflamasyona yol açabilir ve laparoskopik yeniden ameliyat gerekebilir92.
- Büyük miyomlar bulunursa, hastaya komplikasyon riskinin değişmeden kaldığını, ancak işlemin sonucunun küçük miyomlar için daha iyi olduğunu bildirin93.
- Hastanın bilgilendirilmiş onamında veya tıbbi kayıtta bu gerçeği not edin.
2. BAE prosedürüne hazırlık
NOT: Bu, jinekologlara veya vasküler cerrahlara ve girişimsel radyologlara yöneliktir.
- Hastayı hastaneye yatırın (jinekolojik veya vasküler cerrahi bölümü).
- Başvuru sırasında döngünün 10. gününden önce olduğundan emin olun.
- Jinekolojik muayene ve pelvisin ultrason taramasını yapın veya sipariş edin.
- BAE prosedürü için teşhis ve kalifikasyonun doğru olduğundan emin olun.
- BAE kalifikasyonundan bu yana yeni bir kontrendikasyonun ortaya çıkmadığından emin olun. Eğer öyleyse, diğer tedavi seçeneklerini önerin ve işlem tarihini değiştirin.
- 3D transvajinal ultrason taramasını (TVUS) gerçekleştirin ve VOCAL yazılım sınavını (BAE prosedürü 72,75'in etkinliğini değerlendirmek için kullanılır) kullanarak fibroidin (VI, FI ve VFI) hacim ve vaskülarizasyon indekslerini hesaplayın (giriş bölümünde açıklanmıştır) (Şekil 5 ve Şekil 6).
- Bu gerçeği tıbbi kayıtlara not edin.
- BAE'ye hak kazanan hastanın, BAE kalifikasyonu sırasında gerçekleştirilen testlere sahip olduğundan emin olun (BAE için Kalifikasyon'un 1.6.2, 1.6.3, 1.6.5 ve 1.6.6 adımlarında açıklanmıştır).
- Hasta bir jinekolog tarafından ön yeterlilik almışsa ve kan testleri, idrar testi ve MRG yoksa, testleri sipariş edin ve girişimsel bir radyologla bir konsültasyon ayarlayın (BAE Yeterliliği adım 1.7).
- "Hedef olmayan" embolizasyonun bir sonucu olarak yumurtalık hasarının değerlendirilmesini sağlamak için BAE'den önce AMH (önerilen) veya FSH (40 yaş altı önerilmez) serum seviyesini derecelendirin veya sipariş edin.
- Hastaya, test sonuçlarının yaklaşık bir gün içinde hazır olacağını ve BAE prosedürünün ancak bu sonuçları aldıktan sonra mümkün olacağını bildirin.
- Hastaya, yanlış sonuçların onu prosedür için diskalifiye ettiğini bildirin.
- UYARI! PAP smear, endometriyal biyopsi sonuçlarının eksik ya da yanlış çıkması durumunda; vajinal smear'ın mikrobiyolojik testi, hastayı BAE'den diskalifiye eder (bu sonuçları elde etmek için çok uzun bir süre). Doğru sonuçları aldıktan sonra yeniden kalifiye olun.
- Bu gerçeği tıbbi kayıtlara not edin.
- BAE'yi gerçekleştirmek için bilgilendirilmiş bir onay alın.
- Hastaya BAE ile ilgili tüm bilgileri sağlayın.
- BAE'nin olası komplikasyonlarını tartışın (giriş bölümünde açıklanmıştır).
- Hastaya düşünmesi ve soru sorması için zaman bırakın; Hastanın BAE prosedürünü gerçekleştirmek için bilgilendirilmiş bir onay vermesine izin verin.
- Hastaya, BAE başlayana kadar kararını değiştirme hakkına sahip olduğunu bildirin.
- Hasta BAE ile ilgili kararını değiştirirse, uterus fibroidleri için diğer tedavi seçeneklerini önerin (giriş bölümünde açıklanmıştır).
- Hastanın bilgilendirilmiş onamında veya tıbbi kayıtta bu gerçeği not edin.
- BAE prosedüründen hemen önce, BAE için Yeterlilik Bölüm 1.6.2, 1.6.3, 1.6.5 ve 1.6.6'da açıklanan testlerin yanı sıra 3D TVUS, MRG ve girişimsel bir radyolog ile konsültasyonun yapıldığını ve sonuçların doğru olduğundan emin olun.
- Testler eksikse veya sonuçlar yanlışsa bir hastayı BAE'den diskalifiye edin.
- Bu gerçeği tıbbi kayıtlara not edin.
- Hastayı bilgilendirin ve sabahtan işleme kadar gıda ve sıvı alma yasağına dikkat edin. Bunun istisnası, sabah ilaç dozunu almak için gereken az miktarda sıvıdır.
- Sabahları (BAE'den önce) hastanın oruç tuttuğundan emin olun.
- Hastanın ilaçları kendi kronik hastalıkları için aldığından emin olun.
- Bu gerçeği tıbbi kayıtlara not edin.
- Hastaya aşağıdaki ilaçları verin: 1 tablet anksiyolitik (örneğin, Estazolam) ağızdan, 1 doz intravenöz antibiyotik, intravajinal olarak 1 globül Metronidazol, Diklofenak 100 mg rektal fitil.
- Yukarıdaki ilaçları BAE'den yaklaşık 30-40 dakika önce verin.
- Bu gerçeği tıbbi kayıtlara not edin.
- Sol koltuk altı ve sağ kasıkların tıraş edilmesini sağlayarak ameliyat alanını hazırlayın.
- Cildin yukarıdaki bölgeleri tıraş edilmezse, nazikçe tıraş edin.
- Bu gerçeği tıbbi kayıtlara not edin.
- Hastanın rahim içi araç (RİA) olmadığından emin olun.
- Hastanın rahiminde bir RİA varsa, rahim boşluğunda enfeksiyon riskinin arttığını bildirin ve BAE'den önce çıkarmayı teklif edin.
- Hasta RİA'yı çıkarmayı kabul etmiyorsa, bu gerçeği hastanın bilgilendirilmiş onamında veya tıbbi kayıtta not edin.
- Hastanın ilaçlara, kontrast maddelere ve dezenfektanlara karşı herhangi bir alerjik reaksiyon bildirdiğinden emin olun ve bu gerçeği ve sonuçları tıbbi kayıtlara not edin.
3. BAE prosedürünün gerçekleştirilmesi
NOT: Bu, girişimsel radyologlara ve anestezistlere yöneliktir.
- Prosedürü steril koşullarda gerçekleştirin.
- Hastayı ameliyat masasına koyun ve bir hastane dezenfektanı kullanarak (uygun onay ile) sağ kasık bölgesini geniş çapta dezenfekte edin.
- Cerrahi örtüyü ameliyat bölgesinin etrafına yapıştırın (sağ kasık).
- Anestezi türünü seçin: lokal veya epidural anestezi (EA) ve hastanın seçimini tıbbi kayıtta not edin.
- BAE yerel anestezi altında.
- Anestezi (deri altı uygulama) ameliyat bölgesinde% 2 lignokain çözeltisi.
- Gerektiğinde intravenöz olarak 5 mg morfin uygulayın.
- BAE prosedürüne başlamadan önce lokal anestezinin çalışır durumda olduğundan emin olun.
- EA kapsamında BAE
- Hastayı EA için uygun şekilde hazırlayın.
- Cerrahi örtüyü yapıştırmadan önce EA'yı gerçekleştirin.
- EA prosedürü için kalifiye olan hastanın aşağıdaki kontrendikasyonlara sahip olmadığından emin olun EA: prosedür reddi, koagülopati, trombositopeni, hemolitik hastalık, antikoagülan alma, şok, epidural enjeksiyon bölgesinde enfeksiyon, bakteriyemi, lokal anestezik alerjisi, omurganın anatomik deformiteleri, artmış kafa içi basıncı, nörolojik hastalık, şiddetli aort veya mitral darlık94. Bu gerçeği tıbbi kayıtlara not edin.
- Bir anestezi uzmanını arayın ve EA isteyin.
- Bel bölgesindeki epidural boşluğa ince bir kateter yerleştirin ve anestezik verin (anestezistler için ele alınan prosedür).
- BAE prosedürüne başlamadan önce EA'nın çalışır durumda olduğundan emin olun.
- BAE prosedürü
- BAE prosedürünü floroskopi rehberliğinde Anjiyo Suit'te gerçekleştirin.
- Seldinger tekniği95,96 kullanarak vasküler sisteme erişim sağlayın (Şekil 7, Şekil 8 ve Şekil 9).
- Renal arterlerin hemen altındaki abdominal aorta bir pigtail kateter yerleştirin.
- Damarları görselleştirmek için anjiyografi yapın.
- Miyomları besleyen damarların anatomisini değerlendirmek ve prosedürü planlamak için aortonefrografi yapın (Şekil 10).
- Uterin arter ostiumunu ortaya çıkarmak için anterior-posterior ve oblik projeksiyonda internal iliak arterin anjiyografisini yapın.
- Delinme yeri ve kateterin özel şekli nedeniyle sol taraftan, ardından sağ taraftan başlayın. Damarın kalibresine bağlı olarak, ana kateter veya mikrokateter seçici olarak uterin artere sokulur (Şekil 11).
- Kateteri uterin arterin derinliklerine yerleştirin. Damarı hidrojel parçacıkları ile embolize edin. Büyüklüğü yaklaşık 500 μm olarak tahmin edilen uterus-over anastomozunun varlığı nedeniyle, "hedef dışı embolizasyon" riskini azaltmak için embolizasyon için önerilen partikül boyutu 700 μm'dir.
- Damardaki kan akışı tamamen engellenene kadar embolizasyona devam edin. Tedavinin son noktası, damardaki kontrast stazdır ve bu da etkili bir şekilde kapandığını kanıtlar.
- Uterin arterin embolizasyonunu aynı erişimle karşı tarafta gerçekleştirin. Tedavi yaklaşık 0,5 ila 1,0 saat66,67 sürer (Şekil 12).
- Kontrol anjiyografisi sırasında internal iliak artere yerleştirilen bir kateterden embolizasyonun etkinliğini değerlendirin. Aktif bir gölgeleme kanı akışının olmaması (uterus arterlerine), prosedürün teknik olarak doğru kabul edildiğini gösterir (Şekil 13).
- Kateteri dikkatlice çıkarın.
- Delinme bölgesini, sonraki 6 saat veya kapatma cihazı boyunca muhafaza edilmesi gereken basınçlı pansuman ile manuel sıkıştırma yoluyla kapatın (Şekil 14).
- Tıbbi kayıtlarda BAE'nin seyrini açıklayın.
4. BAE prosedürü sonrası hasta bakımı
NOT: Bu, jinekologlara veya vasküler cerrahlara ve anestezistlere yöneliktir.
- Analjezik tedaviye başlayın: hasta kontrollü analjezi (PCA) pompası veya EA.
- Hastayla analjezik tedavi seçeneklerini bilgilendirin ve tartışın.
- Hastaya, EA'nın PCA pompası76'ya kıyasla daha iyi ağrı kontrolü ve daha hızlı rehabilitasyon sağladığını bildirin.
- Bu gerçeği ve hastanın tıbbi kayıttaki seçimini not edin.
- Bir PCA pompası kullanılarak embolizasyon sonrası ağrının analjezik tedavisi.
- Şırıngayı morfin çözeltisi ile PCA pompası için hazırlayın.
- PCA pompası için 50 mL'lik şırıngayı 50 mg morfin ve% 0.9 NaCl çözeltisi (konsantrasyon 1 mg / mL) ile doldurun.
- PCA pompasını intravenöz kullanım için hazırlayın.
- Tahliyeyi şırıngaya bağlayın.
- Damar delinmesini bir kanül kullanarak yerleştirin.
- Şırıngayı PCA pompasına yerleştirin.
- Tahliyeyi doldurun, PCA pompasını çalıştırın.
- BAŞLAT düğmesini açın.
- PCA pompasını kilitleyin.
- PCA pompa parametrelerini ayarlayın (aşağıda listelenmiştir) (Şekil 15).
UYARI! Daha yüksek dozlarda Morfin solunum depresyonuna neden olabilir.- 1 mg / mL'lik bir Morfin konsantrasyonu kullanın. İsteğe bağlı bir doz morfin infüzyonu kullanın (intravenöz bolus) (Bolus p.) 0.5 mg'lık bir zaman aralığı ile, daha sonra bir sonraki isteğe bağlı infüzyon sağlanabilir (Kilitleme aralığı / [Karencja]) 5 dakika (solunum depresyonunu önlemek için). İsteğe bağlı 10 s infüzyon sırasında intravenöz morfin enjeksiyonu süresi kullanın.
- Yukarıdaki tüm adımların yapıldığından emin olun.
- PCA pompasında 24 saate kadar morfin sipariş edin.
- Ağrıyı Sayısal Derecelendirme Ölçeğine (NRS) göre izleyin. Tıbbi kayıttaki NRS değerini not edin.
- Ağrı Değerlendirme Kartını (PAC) kullanın.
- Hastaya, ağrı semptomları ortaya çıktığında, "joy-stick" e kendisinin basması gerektiğini ve böylece ilacı talep üzerine alması gerektiğini bildirin.
- Hastanın talimatları anladığından emin olun.
- İsteğe bağlı "intravenöz bolus" ila "boş bolus" miktarını gözlemleyin (kilitleme aralığı sırasında başlatıldı - BAE PROTOKOLÜ'nden sonra Hasta bakımı bölüm 4.2.3) (Şekil 16).
- "Boş bolus" ile isteğe bağlı "intravenöz bolus" oranı 2/1'den (%67 / %33) daha yüksek bir değere ulaşırsa, aşağıdaki prosedürü kullanın (Şekil 17, Şekil 18).
- Bir PCA pompası kullanarak ağrı kesici tedavinin etkinliğini artırmak ve morfin yan etkileri riskini azaltmak için, intravenöz enjeksiyonlarda ve standart dozlarda parasetamol veya steroid olmayan antienflamatuar ilaçlar kullanmayı düşünün.
- Hastanın yataktan ayrılması gereken durumlara dikkat edin.
- Pompayı kapatmayın.
- Tahliyeyi ayırın ve bir tıpa ile sabitleyin.
- Hasta geri döndüğünde dreni tekrar bağlayın.
- Şırıngayı morfin çözeltisi ile PCA pompası için hazırlayın.
- EA kullanarak embolizasyon sonrası ağrının analjezik tedavisi.
- BAE prosedürü için kullanılmışsa EA'ya devam edin.
- BAE prosedürü için lokal anestezi kullanılmışsa ve hasta epidural kateter yerleştirmeden önce EA istemişse, CBC ve pıhtılaşma testlerinin doğru olduğundan emin olun.
- EA prosedürü için uygun olan hastanın, BAE prosedürünün gerçekleştirilmesi bölüm 3.4.3'te açıklanan çelişkilere sahip olmadığından emin olun. Bu gerçeği tıbbi kayıtlara not edin.
- Bir anestezi uzmanını arayın ve EA isteyin.
- EA'nın çalışır durumda olduğundan emin olun.
- Anestezi uzmanı ile EA çalışma modunu (bolus veya sürekli) belirleyin. Bu gerçeği tıbbi kayıtlara not edin.
- Sürekli modda (CEA), bir anestezi uzmanına danışın ve infüzyon pompası ayarlarını kontrol edin.
- Bolus modunda (BEA), lokal anestezik ajanın uygulanması arasındaki zaman aralıklarını anestezi uzmanı ile tartışın.
- İhtiyaca bağlı olarak kateteri 24-48 saat koruyun.
- NRS ölçeği ile ağrıyı izleyin. Tıbbi kayıttaki NRS değerini not edin.
- PAC'yi kullanın.
- İhtiyaç duyulana kadar CEA/BEA'ya devam edin, en fazla 48 saat.
- Gerekirse PCA veya EA'dan sonra analjezik tedaviye devam edin.
- Parasetamol 3 x 1.0 g'ı intravenöz olarak sipariş edin.
- Diklofenak 2 x 50 mg rektal fitil sipariş edin.
- Yukarıdaki analjezik tedavi yeterli değilse, destekleyici analjezikler ekleyin.
- Ketoprofen 2 x 100 mg intravenöz olarak sipariş edin.
- Ağızdan Furazidin 3 x 100 mg sipariş ederek idrar yolu semptomlarını tedavi edin.
5. BAE prosedürü sonrası kontrol ziyareti
NOT: Bu jinekologlara yöneliktir.
- BAE'den sonraki ilk gün ilk kontrol muayenesini yapın.
- Hastanın genel durumunu değerlendirin.
- Hastanın vücut ısısını ölçün.
- NRS ölçeğine göre BAE'den sonra ağrıyı değerlendirin. PAC'yi kullanın.
- Vasküler kateterin yerleştirildiği yarayı değerlendirin.
- CBC ve pıhtılaşma testleri yapın.
- BAE'den sonra pelvik organların durumunu değerlendirmek için bir TVUS gerçekleştirin.
- Fibroidin (VI, FI ve VFI) hacim ve vaskülarizasyon indekslerini değerlendirmek için hacim probu kullanarak bir 3D TVUS gerçekleştirin.
- Herhangi bir komplikasyon yoksa ve embolizasyon sonrası ağrı oral analjeziklerle kontrol altına alınmışsa, hastayı eve taburcu edin.
- Hastaya, hastaneye yatıştan sonra ateş, karın ağrısı ve cerahatli vajinal akıntı meydana gelirse, hastanın derhal tıbbi yardım alması gerektiğini bildirin.
- Bir sonraki kontrol ziyaretini BAE'den 3 ay sonra gerçekleştirin.
- Jinekolojik muayene, CBC testi ve AMH veya FSH serum seviyesi gerçekleştirin.
- BAE'den sonra pelvik organların durumunu değerlendirmek için MRI veya TVUS yapın (Şekil 19).
- Miyomun (VI, FI ve VFI) hacim ve vaskülarizasyon indekslerini değerlendirmek için hacim probu kullanarak 3D TVUS gerçekleştirin.
- BAE'den 6 ay sonra son kontrol ziyaretini gerçekleştirin.
- Jinekolojik muayene, CBC testi ve AMH veya FSH serum seviyesi gerçekleştirin.
- BAE'den sonra pelvik organların durumunu değerlendirmek için bir TVUS gerçekleştirin.
- Miyomun (VI, FI ve VFI) hacim ve vaskülarizasyon indekslerini değerlendirmek için hacim probu kullanarak 3D TVUS gerçekleştirin.
- BAE'nin etkinliğini değerlendirin.
- BAE'den önce ve sonra CBC testinin sonuçlarını karşılaştırın.
- BAE'den önce ve sonra fibroidin (VI, FI ve VFI) hacimlerini ve vaskülarizasyon indekslerini karşılaştırın.
- "Hedef olmayan" embolizasyonun bir sonucu olarak BAE sırasında yumurtalıklarda iyatrojenik hasar olasılığını değerlendirmek için BAE öncesi ve sonrası serum AMH veya FSH seviyelerini karşılaştırın.
- Hastaya uterin arter embolizasyonundan sonra düzenli jinekolojik kontrollerden geçmesi gerektiğini bildirin.
- Seçilmiş vakalarda (fibroid semptomlarında azalma yok, şüpheli doku sınırı veya diğer ek incelemelerde şüphe yok), BAE'den bir yıl sonra bir MRG yapın (Şekil 20).
Sonuçlar
2009'dan 2019'a kadar olan dönemde 557 BAE prosedürü gerçekleştirildi. Hastaların yaş ortalaması 38 (31-53 yaş) idi. 547 hastada (%98.2) teknik başarı sağlandı.
2009-2013 yılları arasında 32 ila 52 yaşları arasındaki 206 hastadan oluşan grupta (ortalama yaş: 39 yıl) BAE işleminden 3 ay sonra fibroid hacmindeki ortalama azalma (MRG hacim değerlendirmesi) %62 idi. En küçük azalma %9 idi (hyalinize fibroidli hasta). Ayrılmış submukozal fibroid (FIGO 0) olan hastalarda tam redüksiyon (% 100) sağlandı. Hastaların% 90'ı BAE prosedüründen sonra memnuniyet bildirmiştir64.
29-52 yaş arası 65 hastadan oluşan bir grupta (ortalama yaş: 43.1 yıl) BAE'den 3 ay sonra (ultrason VOCAL hacim değerlendirmesi) fibroid hacmindeki ortalama azalma %50.1 (%2.7-%93.5) idi. BAE prosedüründen önce, medyan fibroid hacmi 101cm3 (23.6 ila 610.0cm3 arasında) iken, 3 ay sonra medyan fibroid hacminin 50.4cm3'e (6.9 ila 193.9cm3 aralığında) düşmesi gözlendi. Spearman korelasyon testi, başlangıçtaki baskın fibroid hacmi ile yüzde hacim azalması arasında istatistiksel olarak anlamlı, ancak nispeten zayıf bir pozitif korelasyon (R = 0.33; p = 0.006) gösterdi. İlginç bir şekilde, daha küçük fibroidler, BAE'den 3 ay sonra fibroid hacminde büyük bir azalma değişkenliği gösterirken, daha büyük fibroidler BAE'ye karşı stabil, öngörülebilir bir reaksiyon gösterdi72.
BAE'den 3 ay sonra 17 hastadan oluşan grupta doppler vasküler indekslerde (VI, FI ve VFI) azalma gözlendi. VI ve VFI'daki azalma yüzdesi %95.4 iken, FI'daki azalma %58.3 idi75.
Yumurtalık rezervinin değerlendirilmesi, BAE'den 3 ay sonra 33-40 yaş arası (ortalama yaş: 35 yıl) 30 hastada yapıldı. Ortalama dominant miyom hacmi 107.75cm3 (dağılım 87.4-131.1cm3) idi. Yumurtalık rezervinin aşağıdaki belirteçleri araştırıldı: antral folikül sayısı (AFC), AMH, inhibin B (INHB), FSH ve estradiol (E2). AFC (%56.7; p < 0.001), AHM (%36.7; p < 0.001), INHB (%46.7; p < 0.001) ve E2 (%43.3; p < 0.001) değerinde anlamlı azalma gözlendi. Eş zamanlı olarak FSH serum düzeyinde anlamlı bir artış (%43.4; p < 0.001) gözlenmiştir65.
BAE işleminden üç ay sonra, submukozal miyomu (FIGO 0) (6 cm ve 8 cm çapında) olan iki hastada, miyomların belirgin, nekrotik fragmanlarının servikal kanaldan atılması sırasında uterus inversiyonu gözlendi ve bu da acil histerektomi ile sonuçlandı.
BAE işleminden sonraki gün NRS ölçeğinde 60 hastada PCA (BAE Protokolünden sonra Hasta bakımının 4.2 prosedürü) kullanımı ile embolizasyon sonrası ağrı azalması (PAC'ye göre) değerlendirildi. BAE'den hemen sonra medyan NRS 10 (dağılım 5-10) iken, tedaviden sonra medyan NRS 4 (dağılım 1-5) olarak derecelendirildi. Spearman'ın ilk fibroid hacmi (medyan 194.5 cm3, aralık 79-411 cm3) ile BAE'den hemen sonraki NRS arasındaki korelasyon testi istatistiksel olarak anlamlı, güçlü bir pozitif korelasyon gösterdi (R = 0.6; p < 0.001), oysa tedaviden sonra fibroidlerin başlangıç hacmi ile NRS arasındaki korelasyon istatistiksel olarak anlamlı, zayıf bir pozitif korelasyon gösterdi (R = 0.34; p < 0.001). Yukarıdaki ilişkiler incelendiğinde, BAE'den sonraki majör fibroidlerin BAE'den sonra daha güçlü embolizasyon sonrası ağrıya neden olduğu sonucuna varılabilir. Ancak daha küçük miyomların BAE sonrası embolizasyon sonrası ağrılarının PKA kullanımı ile tedavisi daha iyi sonuçlar vermektedir.
Temsili Sonuçlar için özetlenmiş veriler Tablo 1'de verilmiştir.

Şekil 1: FIGO uterin fibroidler sınıflaması. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Resim 2: Transvajinal ultrason taraması kullanılarak yapılan pelvik muayene.
73 x 50 x 55 mm boyutlarında bir uterus fibroidi (FIGO 5) görülebilir. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 3: BAE için ön yeterlilikte Pelvik MRG muayenesi.
Sagital kesitte kitle etkisi olan büyük bir uterus miyomu (FIGO 2-5) görülür. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
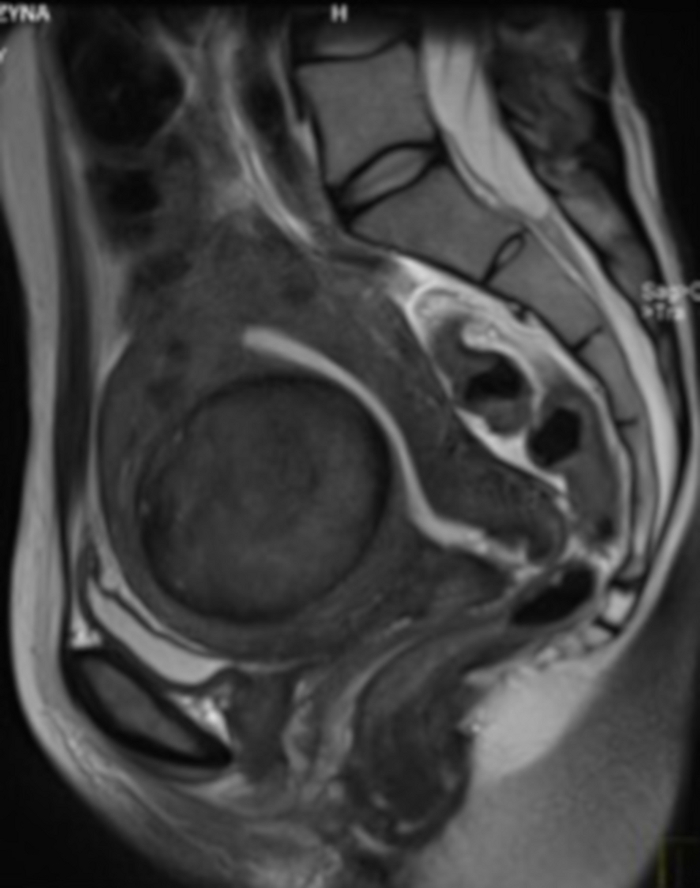
Şekil 4: BAE için ön yeterlilikte Pelvik MRG muayenesi.
Sagital bölümde görülebilir, uterus fibroidi (FIGO 2-5). Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
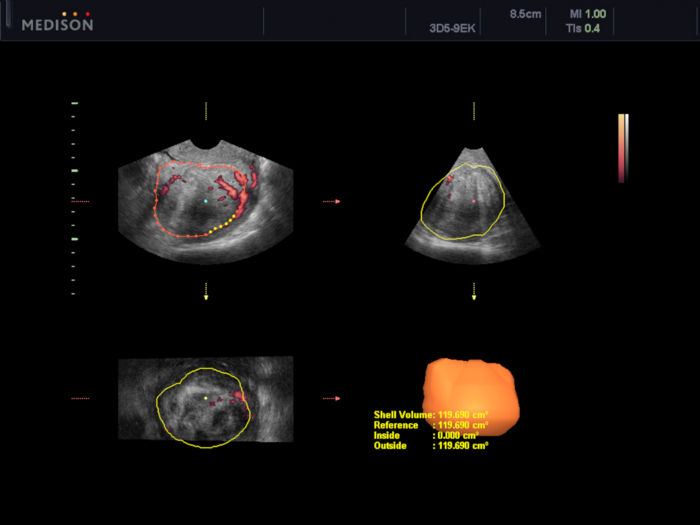
Şekil 5: VOCAL yazılımı kullanılarak uterus fibroid hacminin değerlendirilmesi.
Bu durumda, hacmin 119,7cm3 olduğu tahmin edilmektedir. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 6: VOCAL yazılımı kullanılarak uterus fibroidinin vaskülarizasyonunun değerlendirilmesi.
Bu olguda vaskülarizasyon indeksleri hesaplandı (VI 4.85, FI 25.38 ve VFI 1.23). Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 7: Resimde anjiyografik laboratuvarın bir parçası görülmektedir.
Sol alt köşede, daha fazla aletin sokulduğu açıkta kalan bir kasık ile hasta. Sol üst köşede, anjiyografinin C kolu görülebilir. Sağ üst köşede, operatörün giriş aracını izlediği monitörler görünür. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 8: Arteriyel ponksiyonlar için bir set.
Alttan: bir iğne, bir tanıtıcı ile bir vasküler kilit ve bir kılavuz. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
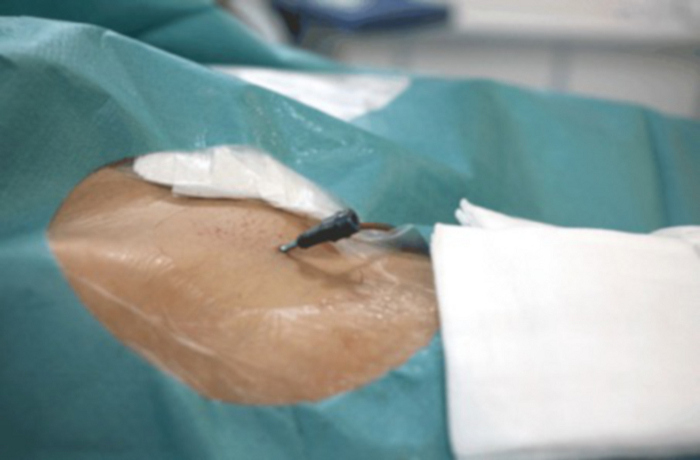
Şekil 9: Femoral artere yerleştirilmiş görünür vasküler kilit ile kasıkların yakın çekimi. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 10: Solda, abdominal aorta yerleştirilen bir kateterden alınan anjiyografi.
Uterus miyomlarının görünür vasküler yatağı. Karşılaştırma için (sağda), BAE'den sonra gerçekleştirilen bir kontrol testi. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 11: Uterin arterlerin proksimal kısımlarına yerleştirilen RUC kateteri kullanılarak yapılan selektif anjiyografi.
Uterus fibroidlerinin görünür vasküler yatağı. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
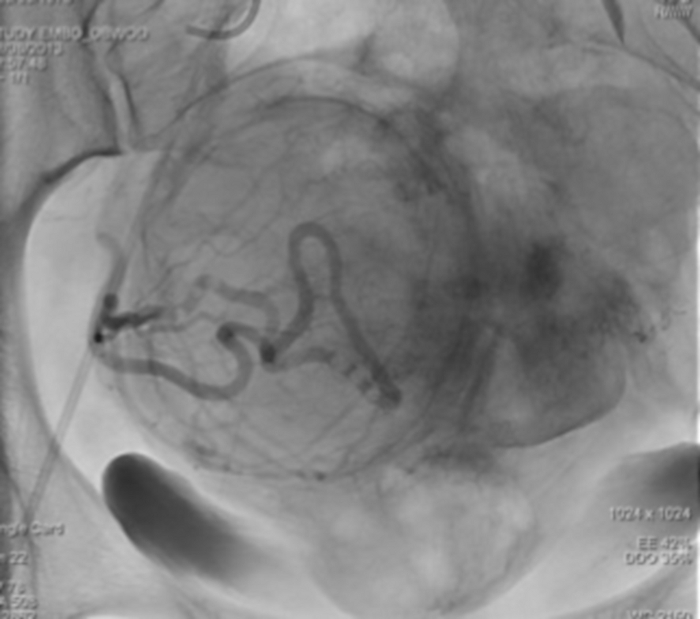
Şekil 12: Kontrast maddenin sağ uterin arterdeki stazısını gösteren tek röntgen görüntüleme. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
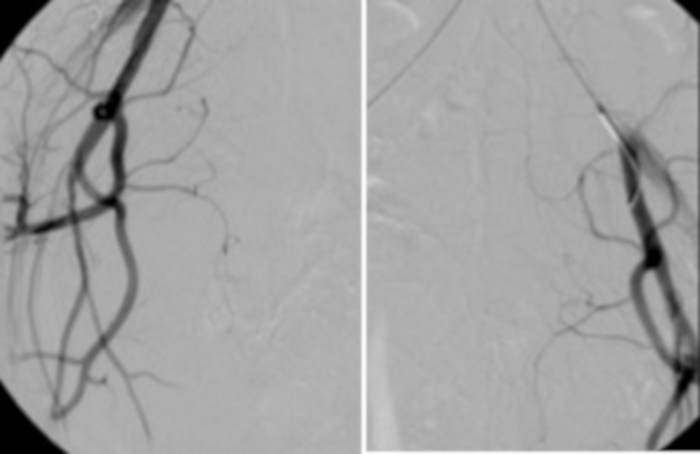
Şekil 13: Sırasıyla sol ve sağ iliak arterde bulunan ana kateterden yapılan kontrol anjiyografisi, uterin arterlere taze kan girişinin (gölgelenme) olmadığını doğrular. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
Şekil 14: BAE'nin tamamlanmasından sonraki vasküler erişim bölgesi.
Sağ kasıkta görünür 2 mm'lik kesi. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 15: BAE tedavisi sonrası embolizasyon sonrası ağrı için PCA pompası parametre ayarları (BAE PROTOKOLÜ sonrası Hasta bakımı bölüm 4.2.3). Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 16: PCA pompası çalışıyor.
İsteğe bağlı intravenöz bolusun "boş bolusa" oranı (BAE PROTOKOLÜ sonrası Hasta bakımı bölüm 4.2.6.2.): 1:1 (%50:%50). Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 17: PCA pompası çalışıyor.
İsteğe bağlı intravenöz bolusun "boş bolusa" oranı (BAE PROTOKOLÜ sonrası Hasta bakımı bölüm 4.2.6.3.) 1:2 (%33:%67). Bu, ek analjezik tedavi gerektirir (BAE PROTOKOLÜ'nden sonra Hasta bakımının 4.2.6.4. prosedürü). Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 18: PCA pompası çalışıyor.
İsteğe bağlı intravenöz bolusun "boş bolusa" oranı (BAE PROTOKOLÜ sonrası Hasta bakımı bölüm 4.2.6.3.): 1:3 (%25:%75). Bu, ek analjezik tedavinin devam etmesini gerektirir (BAE PROTOKOLÜ'nden sonra Hasta bakımının 4.2.6.4. prosedürü). Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 19: BAE işleminden 3 ay sonra Pelvik MRG incelemesi (Şekil 3'teki ile aynı durum).
Sagital bölümde görülen, işlemden öncekinden önemli ölçüde daha küçük, fibroid dokusunun farklı yoğunluğuna sahip bir uterus fibroididir (FIGO 5). Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
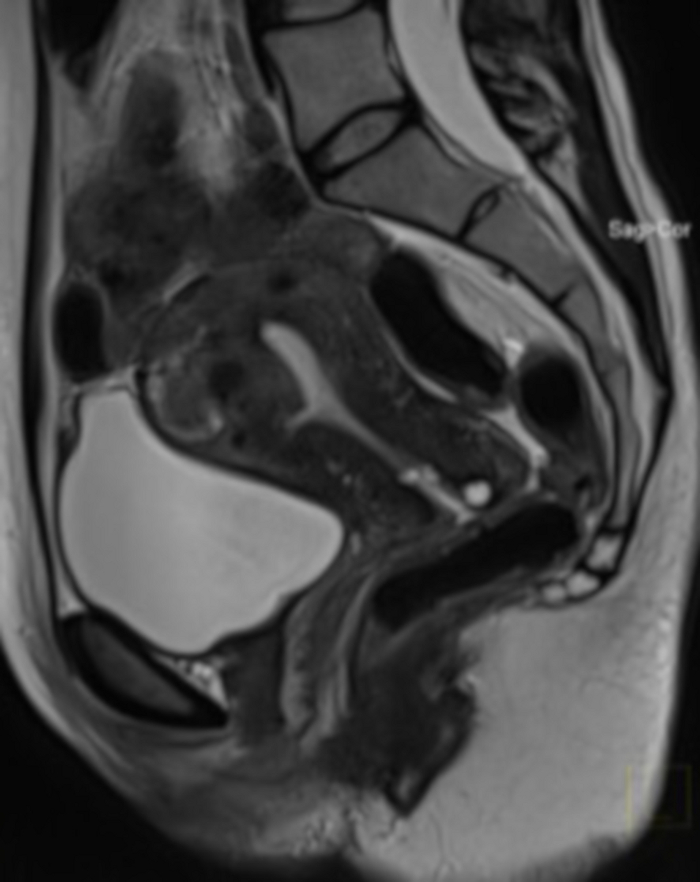
Şekil 20: BAE işleminden 1 yıl sonra Pelvik MRG incelemesi (Şekil 4'teki ile aynı durum).
Sagital bölümde görülebilen bir uterus fibroididir (FIGO 2-5), BAE'den sonra çok büyük bir hacim azalması ile. İşlem sonrası şüpheli doku sınırı nedeniyle MRG yapıldı (bimanuel muayenede miyom yapısını değerlendirme imkanı yoktu). Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
| TEMSILI SONUÇLAR / LUBLIN PROTOKOLÜ 64,65,72 | ||
| 2009'dan 2019'a kadar olan dönemde gerçekleştirilen BAE prosedürlerinin sayısı | 557 | |
| Teknik başarı | 547 hastada (%98.2) elde edildi | |
| 32 ila 52 yaşları arasındaki 206 hasta grubunda BAE'den 3 ay sonra fibroid hacminin ortalama azalması (MRG hacim değerlendirmesi) (ortalama yaş - 39 yıl) | 62.0% (9.0-100.0%) | |
| 29-52 yaş arası 65 hastadan oluşan grupta BAE'den 3 ay sonra (ortalama yaş – 43.1 yıl) fibroid hacminin ortalama azalması (ultrason VOCAL hacim değerlendirmesi) | 50.1% (2.7-93.5%) | |
| Yumurtalık rezervinin değerlendirilmesi | AFC'de azalma | %56,7 (p<0,001) |
| AMH'de azalma | %36,7 (p<0,001) | |
| INHB'de azalma | %46,7 (p<0,001) | |
| E2'de azalma | %43,3 (p<0,001) | |
| FSH'de artış | %43,4 (p<0,001) | |
| 60 hastadan oluşan grupta değerlendirilen PCA ("BAE sonrası hasta bakımı" PROTOKOLÜNÜN 2. prosedürü) kullanımı ile embolizasyon sonrası ağrının azaltılması (PAC'ye göre) | BAE'den hemen sonra medyan NRS | 10 (aralık 5-10) |
| BAE'den sonraki gün medyan NRS | 4 (aralık 1-5) | |
Tablo 1: Lublin Protokolüne uygun olarak gerçekleştirilen semptomatik uterin fibroidlerin tedavisinde BAE tekniğinin Temsili Sonuçları.
Tartışmalar
Uterus fibroidlerinin yapısı, boyutu, lokalizasyonu ve semptomlarındaki farklılıklar nedeniyle, tek tip bir BAE protokolünün oluşturulması kolay bir iş olmamıştır. Bu terapötik yöntemin varsayımları ile hastaların beklentileri arasında hem kalifikasyon aşamasında hem de tedavinin etkileri açısından birçok tutarsızlık olmuştur. Bir kereden fazla, BAE'ye sevk edilen hastalar herhangi bir klinik fibroid belirtisi bildirmedi ve bu uterus tümörlerinin radikal bir şekilde çıkarılmayacağının farkında değildi. Tek açık beklenti ameliyatsız miyomlardan kurtulmaktı.
Bu nedenle, hastanın bu yöntemin varsayımlarını anlaması, kabul etmesi ve uterus fibroid tedavisinin alternatif yöntemlerine ilişkin farklılıkları bilmesi önemlidir. Bilinçli seçimi (BAE Protokolü için Yeterlilik Bölüm 1.1.) kritik bir noktadır ve uygun şekilde uygulanması protokolün devam etmesine izin verecektir.
Protokolün uygulanması sırasında bazı prosedürler tekrarlanır. Bu, bu dergi tarafından benimsenen, bireysel komutların emir kipinde yazıldığı ve bir kişiye yönlendirildiği formülden amaçlanmıştır ve bu formülden kaynaklanmaktadır. Bununla birlikte, birkaç doktor genellikle kalifikasyon, hazırlık ve diğer BAE aşamalarında yer alır. Bunlar aynı zamanda protokolün kritik noktalarıdır; bunların ihmali, optimal olmayan koşullar altında veya kontrendikasyonların varlığı ile BAE ile sonuçlanabilir. Bu nedenle protokol 5 fasıla ayrılmıştır. Bu, çeşitli uzmanlar tarafından devam ettirilmesine izin verir ve tekrarlanan protokol noktaları daha sonra bağımsız olarak kontrol edilir.
Uterus fibroidlerinin tedavisinde tek tip bir uterin arter embolizasyonu protokolü oluşturmada ek bir zorluk, aynı prosedürle ilgili mevcut çok sayıda öneridir (11'e kadar)41. Varsayımları benzer olsa da, her zaman olduğu gibi, "şeytan ayrıntıda gizlidir", bu da ayrıntıların birleştirilmesini gerektiriyordu. BAE geçiren hastaların fibroidlerinin yeri veya üreme planları ile ilgili göreceli kontrendikasyonlar, nitelikler sırasında en tartışmalı olanlardır. SOGC tarafından önerilen daha katı kriterler uygulandığında, hastalar bu prosedürden çıkarılmalı, daha liberal RCOG önerileri ise BAE 14,32,43 için yeterliliğe izin vermelidir. Soru ne yapılacağıdır. Protokol oluşturma sırasında, kararı (kapsamlı literatürden ayrı olarak) vakalarımızın analizine ve kazanılan deneyime dayandırdık, bu da her hastaya bireysel bir yaklaşım gerektiriyor. Bu nedenle, protokol, göreceli kontrendikasyonları olan hastalarda BAE'nin performansını dışlamaz (BAE Protokolü yeterliliğinin 1.4 bölümleri). BAE için doğru yeterlilik ve hazırlık, terapötik başarının anahtarı gibi görünmektedir. Tekniğin kendisi de çok önemlidir, ayrıca sadece terapötik başarı veya hasta memnuniyetini değil, aynı zamanda yukarıda açıklanan komplikasyonların olmamasını da sağlayan BAE bakımı da çok önemlidir.
Miyom sayısından bağımsız olarak, tüm lezyonlar bir işlem sırasında embolize edilir. Genellikle, miyom ne kadar fazlaysa, enjekte edilecek embolizasyon materyali de o kadar fazla olacaktır. Bu, embolizasyonun süresini uzatır ancak prosedürü değiştirmez. Yumurtalık arterine bariz bir bağlantı görürsek BAE değiştirilebilir, bu da hedef dışı embolizasyon riskinin artmasına neden olabilir. Daha sonra böyle bir bağlantıyı kapatabiliriz (örneğin, bobinler kullanarak), böylece yumurtalıkların ve uterusun beslemesini ayırabilir ve daha sonra 700 μm partiküller kullanarak embolizasyona devam edebiliriz. Bobinleri implante etmek mümkün değilse, partikül çapını 900 μm'ye çıkarıyoruz.
Miyomların yumurtalık arterlerinin yanından sağlanabileceği bazı durumlar da vardır; Daha sonra uterin arterler hipoplastiktir. Bu durumlarda, embolizasyonu başarılı bir şekilde gerçekleştirmek için, yumurtalık arterine bir mikrokateter yerleştirilmeli ve yumurtalığı geçmeli, embolizasyon materyalini uterus vasküler yatağına bırakmalı ve uygun yumurtalık beslemesini sürdürmelidir.
Embolizasyonun şüphesiz avantajı, teknik olarak zor bir prosedür olmaması ve sofistike ekipman gerektirmemesidir.
Protokolün güçlü noktaları, hastaların en az yarısının BAE'ye hak kazanırken duymadığı embolizasyon sonrası ağrının tedavisi ile ilgili noktalardır. Önerdiğimiz standart prosedür, bir PCA pompasının kullanılmasıdır (BAE Protokolünden sonra Hasta bakımının 4.2 bölümü) ve elde edilen sonuçlar böyle bir tedavinin yüksek etkinliğini doğrulamaktadır.
BAE protokolünde gelecekteki değişikliklerle ilgili olarak, iltihaplanma ve sepsis riski nedeniyle işlemden önce RİA'nın rahimden çıkarılmasını gerektiren BAE Protokolü'ne hazırlık bölümünün 10. bölümünü değiştirmek mümkün görünmektedir. Büyük takip çalışmalarında, bir RİA varlığı ile birlikte pelviste enfeksiyon riski 1300'de 1'den azdır49.
BAE, ilk kullanımından bu yana deneysel bir yöntem olarak ele alınmıştır, çünkü bu prosedürün etkinliğinin değerlendirilmesini ve kısa ve uzun vadeli dönemlerde verebileceği komplikasyonların incelenmesini gerektirmiştir. Bu yıllar boyunca, endikasyonlar ve kontrendikasyonlar yeni test sonuçlarına ve klinik gözlemlere dayalı olarak değiştirilmiştir. Birkaç randomize kontrollü çalışma da dahil olmak üzere mevcut veriler, BAE'yi etkinliği ve güvenliği iyi belirlenmiş semptomatik uterus fibroidleri için değerli bir tedavi yöntemi olarak kabul etmektedir.
Yukarıdaki protokolün oluşturulması, on yıl boyunca jinekologların ve cerrahi radyologların yakın işbirliğinin bir sonucu olarak kazanılan güncel literatürün, ilgili önerilerin ve deneyimlerin kapsamlı bir analizinden kaynaklanmaktadır.
Açıklamalar
Yazarların ifşa edecek hiçbir şeyi yok.
BEYANAT:
FIGO uterin fibroids sınıflandırmasını gösteren Şekil 1'in yazarı olarak Piotr Szkodziak, figürün herhangi bir değişiklik yapılmadan bilimsel ve eğitimsel uygulamalar için ücretsiz kullanımına izin verir. Şekli değiştirme niyeti yazar (piotr.szkodziak@gmail.com) tarafından kabul edilmelidir.
Teşekkürler
Yazarlar, Lublin Tıp Üniversitesi 3. Kürsü ve Jinekoloji Anabilim Dalı ve Girişimsel Radyoloji ve Nöroradyoloji Anabilim Dalı'nın tüm ekibine Uterin Arterler Embolizasyonu Lublin protokolünün uygulanmasındaki yardımları için teşekkür eder.
Malzemeler
| Name | Company | Catalog Number | Comments |
| 2% lignocaine in an ampoule | Intended for interventional radiologist (section 3) | ||
| Access to Angio Suite for Minimally Invasive Vascular Surgery | Intended for interventional radiologist (section 3) | ||
| Angiogarfic set | Balton | INT5F | (5 Fr sheath, needle, guidewire) Intended for interventional radiologist (section 3) |
| Angiografic kit | Panep | 44000291 | (Sterile Disposable Angiography DRAPE) Intended for interventional radiologist (section 3) |
| Cervical (PAP) smear kit | Intended only for the gynecologist (section 1) | ||
| Diagnostic lab (possibility to use) | Necessary to perform laboratory tests (section 1, 2 and 5) | ||
| Disinfectant | Intended for interventional radiologist (section 3) | ||
| Dressings | Intended for interventional radiologist (section 3) | ||
| Embozene 700 μm | Varian Medical | 17020-SI | (Particles) Intended for interventional radiologist (section 3) |
| Epidural anesthesia kit | Intended only for the anesthesiologist (section 3 and 4) | ||
| Equipment for gynecological examination | Intended only for the gynecologist (section 1 and 2) | ||
| Intravaginal antibiotic | Intended for the gynecologist or vascular surgeons (section 2) | ||
| Intravenous antibiotic | Intended for the gynecologist or vascular surgeons (section 2) | ||
| Intravenous nonsteroidal anti-inflammatory drug | Intended for the gynecologist or vascular surgeons (section 4) | ||
| Morphine in ampoules | Intended for interventional radiologist and gynecologist or vascular surgeons (section 3, 4) | ||
| MRI lab (possibility to use) | Intended for interventional radiologist (section 1 and 2) | ||
| Oral anxiolytic | Intended for the gynecologist or vascular surgeons (section 2) | ||
| Oral Furazidin | Intended for the gynecologist or vascular surgeons (section 4) | ||
| Oral Paracetamol or nonsteroidal anti-inflammatory drug | Intended for the gynecologist or vascular surgeons (section 4) | ||
| Pain Assessment Card | Intended for the gynecologist or vascular surgeons (section 4) | ||
| Patient Controlled Analgesia Pump | Intended for the gynecologist or vascular surgeons (section 4) | ||
| Progreate Microcathete PROGREA 2.7 Fr x 130 cm STR w/Marker + GW 100 mm x 2.7 Fr | Terumo | MC-PE27131 | (Microcatheter) Intended for interventional radiologist (section 3) |
| RADIFOCUS GUIDE WIRE M Standard Angled 0.032”/0.81 mm 180 cm 30 mm flex | Terumo | RF-GA32183M | (Guidewire) Intended for interventional radiologist (section 3) |
| RADIFOCUS OPTITORQUE 5 Fr x 80 cm Cobra 2 Middle SH0 | Terumo | RH-AB55108M | (Catheter) Intended for interventional radiologist (section 3) |
| RADIFOCUS OPTITORQUE 5 Fr x 80 cm UFE Type 1 19 SH0 | Terumo | RH-AUB5108M | (Catheter) Intended for interventional radiologist (section 3) |
| Rectal nonsteroidal anti-inflammatory drug | Intended for the gynecologist or vascular surgeons (section 2, 4) | ||
| Shaving kit | Intended for the gynecologist or vascular surgeons (section 2) | ||
| Single-use Endometrial Biopsy Kit | Intended only for the gynecologist (section 1) | ||
| Solution of 0,9% NaCl | Intended for the gynecologist or vascular surgeons (section 4) | ||
| Ultrasound machine with 3D-transvaginal probe | Intended only for the gynecologist (section 2 and 5) | ||
| Ultrasound machine with transvaginal probe | Intended only for the gynecologist (section 1 and 2) |
Referanslar
- Tinelli, A., et al. Myoma pseudocapsule: A distinct endocrino-anatomical entity in gynecological surgery. Gynecological Endocrinology. 25 (10), 661-667 (2009).
- Tinelli, A., et al. Myomas: anatomy and related issues. Minerva Ginecologica. 68 (3), 261-273 (2016).
- Laganà, A. S., et al. Epigenetic and genetic landscape of uterine leiomyomas: a current view over a common gynecological disease. Archives of Gynecology and Obstetrics. 296 (5), 855-867 (2017).
- Vanharanta, S., et al. Distinct expression profile in fumarate-hydratase-deficient uterine fibroids. Human Molecular Genetics. 15 (1), 97-103 (2006).
- Hug, K., et al. Physical mapping of the uterine leiomyoma t(12;14)(q13-15;q24.1) breakpoint on chromosome 14 between SPTB and D14S77. Genes, Chromosomes & Cancer. 11 (4), 263-266 (1994).
- Ozisik, Y. Y., et al. Cytogenetic findings in a symplastic leiomyoma. Cancer Genetics and Cytogenetics. 67 (1), 79-80 (1993).
- Ozisik, Y. Y., Meloni, A. M., Surti, U., Sandberg, A. A. Deletion 7q22 in uterine leiomyoma. A cytogenetic review. Cancer Genetics and Cytogenetics. 71 (1), 1-6 (1993).
- Sparic, R., Mirkovic, L., Malvasi, A., Tinelli, A. Epidemiology of uterine myomas: A review. International Journal of Fertility and Sterility. 9 (4), 424-435 (2016).
- Stewart, E. A. Uterine fibroids. Lancet. 357 (9252), 293-298 (2001).
- Williams, A. R. W. Uterine fibroids - what's new. F1000Research. 6, 2109(2017).
- Stewart, E. A. Uterine fibroids. The New England Journal of Medicine. 372 (17), 1646-1655 (2015).
- Al-Hendy, A., Myers, E. R., Stewart, E. Uterine fibroids: burden and unmet medical need. Seminars in Reproductive Medicine. 35 (6), 473-480 (2017).
- de la Cruz, M. S. D., Buchanan, E. M. Uterine fibroids: Diagnosis and treatment. American Family Physician. 95 (2), 100-107 (2017).
- Vilos, G. A., et al. The management of uterine leiomyomas. Journal of Obstetrics and Gynaecology Canada. 37 (2), 157-178 (2015).
- Stewart, E. A. Uterine fibroids. The New England Journal of Medicine. 372 (17), 1646-1655 (2015).
- Sabry, M., Al-Hendy, A. Medical treatment of uterine leiomyoma. Reproductive sciences (Thousand Oaks, Calif.). 19 (4), 339-353 (2012).
- Istre, O. Management of symptomatic fibroids: conservative surgical treatment modalities other than abdominal or laparoscopic myomectomy. Best Practice & Research. Clinical Obstetrics & Gynaecology. 22 (4), 735-747 (2008).
- Donnez, J., Dolmans, M. M. Uterine fibroid management: from the present to the future. Human Reproduction Update. 22 (6), 665-686 (2016).
- Rogers, T. S., Bieck, A. M. Management of Uterine Fibroids. American Family Physician. 99 (5), (2019).
- Chwalisz, K., Taylor, H. Current and Emerging Medical Treatments for Uterine Fibroids. Seminars in Reproductive Medicine. 35 (6), 510-522 (2017).
- Saridogan, E. Surgical treatment of fibroids in heavy menstrual bleeding. Women's Health. 12 (1), London, England. 53-62 (2016).
- Fritton, K., Borahay, M. A. New and Emerging Therapies for Uterine Fibroids. Seminars in Reproductive Medicine. 35 (6), 549-559 (2017).
- Ciavattini, A., et al. Hypovitaminosis D and "small burden" uterine fibroids: Opportunity for a Vitamin D supplementation. Medicine (Baltimore). 95 (52), (2016).
- Friend, D. R. Drug delivery for the treatment of endometriosis and uterine fibroids. Drug Delivery and Translational Research. 7 (6), 829-839 (2017).
- Donnez, J., Courtoy, G. E., Dolmans, M. M. Fibroid management in premenopausal women. Climacteric: The Journal of the International Menopause Society. 22 (1), 27-33 (2019).
- Maksym, R. B., Wierzba, W., Baranowski, W. E. P23.06: The feasibility of uterine fibroid treatment with advanced ultrasound-guided HIFU system: preliminary report. Ultrasound in Obstetrics & Gynecology. 48, 242(2016).
- Lee, J. S., Hong, G. Y., Lee, K. H., Song, J. H., Kim, T. E. Safety and efficacy of ultrasound-guided high-intensity focused ultrasound treatment for uterine fibroids and adenomyosis. Ultrasound in Medicine and Biology. 45 (12), 3214-3221 (2019).
- Burbank, F. History of uterine artery occlusion and subsequent pregnancy. American Journal of Roentgenology. 192 (6), 1593-1600 (2009).
- Sack, R. A. Bilateral internal iliac (hypogastric) artery ligation to control obstetric and gynecologic hemorrhage. A ten-year review at the community hospital level. American Journal of Obstetrics and Gynecology. 116 (4), 493-497 (1973).
- Brown, B. J., Heaston, D. K., Poulson, A. M., Gabert, H. A., Mineau, D. E., Miller, F. J. Uncontrollable postpartum bleeding: A new approach to hemostasis through angiographic arterial embolization. Obstetrics and Gynecology. 54 (3), 361-365 (1979).
- Heaston, D. K., Mineau, D. E., Brown, B. J., Miller, F. J. Transcatheter arterial embolization for control of persistent massive puerperal hemorrhage after bilateral surgical hypogastric artery ligation. American Journal of Roentgenology. 133 (1), 152-154 (1979).
- Royal College of Obstetricians and Gynaecologists Clinical recommendations on the use of uterine artery embolization (UAE) in the management of fibroids. Royal College of Radiologists. , Available from: https://www.rcog.org.uk/globalassets/documents/guidelines/23-12-2013_rcog_rcr_uae.pdf (2013).
- Ravina, J. H., et al. Arterial embolization to treat uterine myomata. The Lancet. 346 (8976), 671-672 (1995).
- Goodwin, S. C., Vedantham, S., McLucas, B., Forno, A. E., Perrella, R. Preliminary experience with uterine artery embolization for uterine fibroids. Journal of Vascular and Interventional Radiology. 8 (4), 517-526 (1997).
- Kohi, M. P., Spies, J. B. Updates on uterine artery embolization. Seminars in Interventional Radiology. 35 (1), 48-55 (2018).
- Gupta, J. K., et al. Cochrane Database of Systematic Reviews Uterine artery embolization for symptomatic uterine fibroids (Review). Cochrane Database of Systematic Reviews. (12), (2014).
- Naredi, N., Bhattacharyya, T. K. Uterine Artery Embolization: A Nonsurgical Cure for Fibroids. South Asian Federation of Obstetrics and Gynecology. 1 (3), (2009).
- Memtsa, M., Homer, H. Complications associated with uterine artery embolization for fibroids. Obstetrics and Gynecology International. 2012 (290542), 1-5 (2012).
- Dutton, S., Hirst, A., McPherson, K., Nicholson, T., Maresh, M. A UK multicentre retrospective cohort study comparing hysterectomy and uterine artery embolization for the treatment of symptomatic uterine fibroids (HOPEFUL study): Main results on medium-term safety and efficacy. BJOG: An International Journal of Obstetrics and Gynaecology. 114 (11), 1340-1351 (2007).
- Heavy menstrual bleeding: assessment and management (CG44). Nice guidelines. National Collaborating Centre for Women's and Children's Health (UK). , Available from: https://www.nice.org.uk/guidance/cg44 (2007).
- Chen, H. T., Athreya, S. Systematic review of uterine artery embolization practice guidelines: are all the guidelines on the same page. Clinical Radiology. 73 (5), 507(2018).
- American College of Obstetricians and Gynecologists. American College of Obstetricians and Gynecologists ACOG practice bulletin. Alternatives to hysterectomy in the management of leiomyomas. Obstetrics and Gynecology. 112 (2), 387-400 (2008).
- Carranza-Mamane, B., et al. The Management of Uterine Fibroids in Women With Otherwise Unexplained Infertility. Journal of Obstetrics and Gynaecology Canada. 37 (3), 277-285 (2015).
- Wozniak, S., Czuczwar, P., Szkodziak, P. R., Pyra, K., Paszkowski, T. EP26.01: Value of "elasto strain ratio" ultrasound elastography in the diagnosis of adenomyosis: preliminary study. Ultrasound in Obstetrics & Gynecology. 50, 381(2017).
- Szkodziak, P. R., Wozniak, S., Czuczwar, P., Wrona, W., Trzeciak, K., Paszkowski, T. OP24.04: Value of "elasto strain ratio" ultrasound elastography in the diagnosis of intramural uterine fibroids: preliminary study. Ultrasound in Obstetrics & Gynecology. 50, 126(2017).
- Popovic, M., Puchner, S., Berzaczy, D., Lammer, J., Bucek, R. A. Uterine artery embolization for the treatment of adenomyosis: A review. Journal of Vascular and Interventional Radiology. 22 (7), 901-909 (2011).
- de Bruijn, A. M., et al. Uterine Artery Embolization for the Treatment of Adenomyosis: A Systematic Review and Meta-Analysis. Journal of Vascular and Interventional Radiology. 28 (12), (2017).
- Bérczi, V., et al. Safety and Effectiveness of UFE in Fibroids Larger than 10 cm. CardioVascular and Interventional Radiology. 38 (5), 1152-1156 (2015).
- Stępniak, A. Uterine artery embolization in the treatment of symptomatic fibroids - State of the art 2018. Przeglad Menopauzalny. 17 (4), 141-143 (2018).
- Czuczwar, P., et al. The influence of uterine artery embolization on ovarian reserve, fertility, and pregnancy outcomes - A review of literature. Przeglad Menopauzalny. 15 (4), 205-209 (2016).
- Firouznia, K., Ghanaati, H., Sanaati, M., Jalali, A. H., Shakiba, M. Pregnancy after uterine artery embolization for symptomatic fibroids: A series of 15 pregnancies. American Journal of Roentgenology. 192 (6), 1588-1592 (2009).
- Bonduki, C. E., et al. Pregnancy after uterine arterial embolization. Clinics. 66 (5), 807-810 (2011).
- Yeaton-Massey, A., Loring, M., Chetty, S., Druzin, M. Uterine rupture after uterine artery embolization for symptomatic leiomyomas. Obstetrics and Gynecology. 123 (2), Part 2 418-420 (2014).
- Takahashi, H., Hayashi, S., Matsuoka, K., Kitagawa, M. Placenta accreta following uterine artery embolization. Taiwanese Journal of Obstetrics and Gynecology. 49 (2), 197-198 (2010).
- Takeda, J., et al. Spontaneous uterine rupture at 32 weeks of gestation after previous uterine artery embolization. Journal of Obstetrics and Gynaecology Research. 40 (1), 243-246 (2014).
- Practice Committee of American Society for Reproductive Medicine in collaboration with Society of Reproductive Surgeons. Myomas and reproductive function. Fertility and Sterility. 90 (5), 125-130 (2008).
- Uterine artery embolization for fibroids (Interventional procedures guidance [IPG367]). Nice Guidelines. National Institute for Health and Clinical Excellence (NICE). , Available from: http://publications.nice.org.uk/uterine-artery-embolization-for-fibroids-ipg367 (2010).
- Leibsohn, S., d'Ablaing, G., Mishell, D. R., Schlaerth, J. B. Leiomyosarcoma in a series of hysterectomies performed for presumed uterine leiomyomas. American Journal of Obstetrics and Gynecology. 162 (4), 968-976 (1990).
- Parker, W. H., Fu, Y. S., Berek, J. S. Uterine sarcoma in patients operated on for presumed leiomyoma and rapidly growing leiomyoma. Obstetrics and Gynecology. 83 (3), 414-418 (1994).
- Ricci, S., Stone, R. L., Fader, A. N. Uterine leiomyosarcoma: Epidemiology, contemporary treatment strategies and the impact of uterine morcellation. Gynecologic Oncology. 145 (1), 208-216 (2017).
- Felix, A. S., et al. The etiology of uterine sarcomas: A pooled analysis of the epidemiology of endometrial cancer consortium. British Journal of Cancer. 108 (3), 727-734 (2013).
- Roberts, M. E., Aynardi, J. T., Chu, C. S. Uterine leiomyosarcoma: A review of the literature and update on management options. Gynecologic Oncology. 151 (3), 562-572 (2018).
- Schieda, N., et al. Gadolinium-Based Contrast Agents in Kidney Disease: A Comprehensive Review and Clinical Practice Guideline Issued by the Canadian Association of Radiologists. Canadian Journal of Kidney Health and Disease. 5, 1-17 (2018).
- Pyra, K., et al. Uterine artery embolization for the treatment of symptomatic uterine fibroids. (Embolizacja tętnic macicznych w leczeniu objawowych mięśniaków macicy). Postępy Nauk Medycznych. 28 (2), 88-94 (2015).
- Czuczwar, P., Stepniak, A., Milart, P., Paszkowski, T., Wozniak, S. Comparison of the influence of three fibroid treatment options: Supracervical hysterectomy, ulipristal acetate and uterine artery embolization on ovarian reserve - An observational study. Journal of Ovarian Research. 11 (1), (2018).
- Nocum, D. J., Robinson, J., Liang, E., Thompson, N., Reed, W. The factors contributing to the total radiation exposure of patients during uterine artery embolization. Journal of Medical Radiation Sciences. 66 (3), 200-211 (2019).
- Nikolic, B., Spies, J. B., Lundsten, M. J., Abbara, S. Patient radiation dose associated with uterine artery embolization. Radiology. 214 (1), 121-125 (2000).
- Colgan, T. J., et al. Pathologic features of uteri and leiomyomas following uterine artery embolization for leiomyomas. The American Journal of Surgical Pathology. 27 (2), 167-177 (2003).
- Weichert, W., et al. Uterine arterial embolization with tris-acryl gelatin microspheres: a histopathologic evaluation. The American Journal of Surgical Pathology. 29 (7), 955-961 (2005).
- Walker, W. J., Pelage, J. P. Uterine artery embolization for symptomatic fibroids: clinical results in 400 women with imaging follow up. BJOG An International Journal of Obstetrics and Gynaecology. 109 (11), 1262-1272 (2002).
- Ravina, J. H., Aymard, A., Ciraru-Vigneron, N., Clerissi, J., Merland, J. J. Uterine fibroids embolization: results about 454 cases. Gynécologie, Obstétrique & Fertilité. 31 (7-8), 597-605 (2003).
- Czuczwar, P., et al. Predicting the results of uterine artery embolization: Correlation between initial intramural fibroid volume and percentage volume decrease. Przeglad Menopauzalny. 13 (4), 247-252 (2014).
- Lohle, P. N. M., et al. Long-term Outcome of Uterine Artery Embolization for Symptomatic Uterine Leiomyomas. Journal of Vascular and Interventional Radiology. 19 (3), 319-326 (2008).
- Walker, W. J., Barton-Smith, P. Long-term follow up of uterine artery embolization - An effective alternative in the treatment of fibroids. BJOG: An International Journal of Obstetrics and Gynaecology. 113 (4), 464-468 (2006).
- Czuczwar, P., et al. Influence of ulipristal acetate therapy compared with uterine artery embolization on fibroid volume and vascularity indices assessed by three-dimensional ultrasound: Prospective observational study. Ultrasound in Obstetrics and Gynecology. 45 (6), 744-750 (2015).
- Van Der Kooij, S. M., et al. Epidural analgesia versus patient-controlled analgesia for pain relief in uterine artery embolization for uterine fibroids: A decision analysis. CardioVascular and Interventional Radiology. 36 (6), 1514-1520 (2013).
- Pisco, J. M., et al. Pelvic Pain after Uterine Artery Embolization: A Prospective Randomized Study of Polyvinyl Alcohol Particles Mixed with Ketoprofen versus Bland Polyvinyl Alcohol Particles. Journal of Vascular and Interventional Radiology. 19 (11), 1537-1542 (2008).
- Pisco, J. M., et al. Uterine Artery Embolization under Electroacupuncture for Uterine Leiomyomas. Journal of Vascular and Interventional Radiology. 20 (7), 863-870 (2009).
- Pelage, J. P., et al. Uterine embolization. Journal de Radiologie. 81 (12), 1873-1874 (2000).
- Pelage, J. P., et al. Uterine Fibroid Vascularization and Clinical Relevance to Uterine Fibroid Embolization. RadioGraphics. 25, suppl 1 99-117 (2005).
- Siskin, G. P., et al. Outpatient uterine artery embolization for symptomatic uterine fibroids: Experience in 49 patients. Journal of Vascular and Interventional Radiology. 11 (3), 305-311 (2000).
- Salehi, M., Jalilian, N., Salehi, A., Ayazi, M. Clinical Efficacy and Complications of Uterine Artery Embolization in Symptomatic Uterine Fibroids. Global Journal of Health Science. 8 (7), (2015).
- Worthington-Kirsch, R., et al. The Fibroid Registry for outcomes data (FIBROID) for uterine embolization: Short-term outcomes. Obstetrics and Gynecology. 106 (1), 52-59 (2005).
- Paszkowski, T., et al. Uterine artery embolization - clinical problems. Polish Gynaecology. 84 (12), (2013).
- Spies, J. B., et al. Fibroid Registry Investigators. The FIBROID Registry: symptom and quality-of-life status 1 year after therapy. Obstetrics & Gynecology. 106 (6), 1309-1318 (2005).
- Chrisman, H. B., et al. The impact of uterine fibroid embolization on resumption of menses and ovarian function. Journal of Vascular and Interventional Radiology. 11 (6), 699-703 (2000).
- Maciel, C., Tang, Y. Z., Sahdev, A., Madureira, A. M., Vilares-Morgado, P. Preprocedural MRI and MRA in planning fibroid embolization. Diagnostic and Interventional Radiology. 23 (2), 163-171 (2017).
- Laughlin-Tommaso, S. K., et al. Clinical limitations of the International Federation of Gynecology and Obstetrics (FIGO) classification of uterine fibroids. International Journal of Gynecology and Obstetrics. 139 (2), 143-148 (2017).
- Vilos, G. A. Uterine fibroids: relationships to reproduction. Minerva Ginecologica. 55 (5), 417-423 (2003).
- McLucas, B. Pregnancy following uterine artery embolization: An update. Minimally Invasive Therapy and Allied Technologies. 22 (1), 39-44 (2013).
- Karlsen, K., Hrobjartsson, A., Korsholm, M., Mogensen, O., Humaidan, P., Ravn, P. Fertility after uterine artery embolization of fibroids: a systematic review. Archives of Gynecology and Obstetrics. 297 (1), 13-25 (2018).
- Margau, R., et al. Outcomes after Uterine Artery Embolization for Pedunculated Subserosal Leiomyomas. Journal of Vascular and Interventional Radiology. 19 (5), 657-661 (2008).
- Spies, J. B., et al. The FIBROID registry: Symptom and quality-of-life status 1 year after therapy. Obstetrics and Gynecology. 106 (6), 1309-1318 (2005).
- Avilla-Hernandez, A., Singh, P. Epidural Anesthesia - StatPearls - NCBI Bookshelf. Statpearls. , 1(2019).
- Higgs, Z. C. J., Macafee, D. A. L., Braithwaite, B. D., Maxwell-Armstrong, C. A. The Seldinger technique: 50 Years on. Lancet. 366 (9494), 1407-1409 (2005).
- Seldinger, S. I. Catheter replacement of the needle in percutaneous arteriography: A new technique. Acta Radiologica. 39 (5), 368-376 (1953).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiDaha Fazla Makale Keşfet
This article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır