Method Article
Desmistificando o Ultrassom em Excesso Venoso (VExUS): Aquisição e Interpretação de Imagens
Neste Artigo
Resumo
A ultrassonografia point-of-care (POCUS) é frequentemente usada para avaliar o circuito hemodinâmico e detectar a presença de congestão venosa. O sistema de pontuação do Venous Excess Ultrasound (VExUS) foi desenvolvido para ajudar os médicos a prever o impacto da congestão venosa na disfunção orgânica. Este artigo tem como objetivo descrever a aquisição e interpretação de imagens VExUS.
Resumo
Os profissionais de muitas especialidades médicas devem avaliar com precisão o circuito hemodinâmico para fornecer o atendimento adequado ao paciente. A congestão venosa está cada vez mais implicada em uma série de complicações de múltiplos órgãos. No entanto, a avaliação hemodinâmica continua sendo um desafio devido à fisiologia complexa envolvida e à precisão diagnóstica inconsistente das ferramentas convencionais à beira do leito e das manobras de exame físico. Embora o cateterismo cardíaco direito seja considerado o padrão-ouro para medir a pressão venosa sistêmica, ele é invasivo e não é facilmente repetível e, portanto, ainda há necessidade de alternativas não invasivas. Mesmo os exames de ultrassonografia no local de atendimento da veia jugular interna ou da veia cava inferior têm limitações significativas em termos de precisão da avaliação do volume intravascular e correlação com a pressão venosa central. Para melhorar a precisão dos médicos à beira do leito na avaliação da congestão venosa, foi desenvolvido e validado um protocolo que utiliza sinais Doppler de onda pulsada (PW) das veias do fígado e dos rins para classificar o grau de congestão venosa presente nos pacientes. Embora esse sistema de pontuação, denominado Ultrassom Venoso em Excesso (VExUS), esteja sendo cada vez mais adotado em certas subespecialidades da medicina, como nefrologia e cuidados intensivos, ele permanece subutilizado na medicina como um todo. Isso provavelmente se deve, pelo menos em parte, às lacunas de conhecimento e à falta de treinamento nessa modalidade emergente. Para abordar essa lacuna educacional, este artigo descreverá a aquisição e interpretação de imagens VExUS.
Introdução
A avaliação do circuito hemodinâmico à beira do leito é fundamental para o cuidado diário do paciente agudo. Os efeitos deletérios da sobrecarga hídrica são cada vez mais reconhecidos mesmo fora de síndromes clínicas mais óbvias, como insuficiência cardíaca, e agora existem vários estudos mostrando que o balanço hídrico positivo está associado ao aumento da mortalidade1. Há um crescente corpo de evidências que mostra que mesmo baixos níveis de congestão venosa estão associados à disfunção orgânica2. Da mesma forma, o descongestionamento oportuno está associado a melhores resultados3. Esse circuito dinâmico de múltiplos órgãos envolve o coração direito e esquerdo, a resistência vascular sistêmica, as pressões da artéria pulmonar e o retorno venoso sequencial do lado direito, culminando na veia cava. É complexo e sua avaliação precisa continua sendo um desafio para os médicos à beira do leito. Médicos de várias especialidades tomam decisões regularmente com base nessa avaliação. Ferramentas convencionais à beira do leito e manobras de exame físico, incluindo avaliação da pressão venosa jugular, estão quase sempre disponíveis, mas permanecem não confiáveis 4,5,6,7,8,9. O ultrassom no local de atendimento (POCUS) é um exame de ultrassom limitado realizado à beira do leito e é interpretado pelo médico assistente para responder a perguntas clínicas focadas. Ele é integrado em tempo real com o histórico do paciente, exame físico e outros dados disponíveis para auxiliar no diagnóstico e tratamento. Nos últimos anos, a ultrassonografia se solidificou como uma extensão do exame físico10, melhorando a capacidade dos médicos de detectar congestão venosa11,12. Além disso, o POCUS pode orientar a terapia descongestiva, o que pode afetar positivamente os resultados dos pacientes 2,3.
Um protocolo específico que utiliza ultrassonografia que foi validado para auxiliar na avaliação hemodinâmica é o escore de ultrassonografia por excesso venoso, ou VExUS. Descrito pela primeira vez por Beaubien-Souligny et al.13 em 2020, esse sistema de pontuação foi originalmente validado em pacientes pós-cirurgia cardíaca como um preditor confiável de lesão renal aguda (LRA). Nos últimos anos, o VExUS também demonstrou ajudar na avaliação do volume intravascular em vários outros contextos clínicos 14,15,16,17. O VExUS avalia várias veias intra-abdominais para rastrear sinais ultrassonográficos associados à congestão. Esses sinais ultrassonográficos de congestão aparecem e progridem de forma incremental à medida que a congestão venosa piora, permitindo que o VExUS rastreie a congestão e potencialmente rastreie sua resposta à terapia ao longo do tempo.
Embora os componentes individuais do exame VExUS estejam em uso há muito tempo 18,19,20, sua combinação, bem como seu uso para monitorar a terapia ao longo do tempo, permanecem subutilizados, em parte devido à falta de familiaridade dos profissionais com a forma de realizar o exame. Acreditamos que essa lacuna no conhecimento é um dos principais fatores que impediram a adoção em larga escala do VExUS como a principal alternativa ao monitoramento cardíaco invasivo padrão-ouro das pressões venosas.
Para tentar resolver essa lacuna de conhecimento, este artigo descreve um protocolo instrucional para a realização do exame VExUS, que pode servir como um guia passo a passo para médicos à beira do leito. Este protocolo baseia-se na experiência coletiva de um grupo de médicos representando várias especialidades médicas (nefrologia, cuidados intensivos, medicina interna e anestesiologia) de vários centros médicos acadêmicos para descrever uma abordagem padronizada para aquisição e interpretação de imagens VExUS.
Protocolo
Todos os procedimentos realizados em estudos envolvendo participantes humanos aderiram aos padrões éticos do comitê institucional de pesquisa e à Declaração de Helsinque, incluindo suas alterações posteriores ou padrões éticos comparáveis. O consentimento informado por escrito foi obtido dos participantes humanos. A técnica de varredura abrangeu a seleção do transdutor, as configurações da máquina, o posicionamento do paciente, a varredura em modo B e a aquisição de imagens. Pacientes com volume incerto, suspeita de congestão venosa, insuficiência cardíaca, lesão renal aguda (LRA) e/ou doença renal crônica (DRC) foram incluídos no estudo, enquanto aqueles com doença renal em estágio terminal em diálise, cirrose conhecida ou trombose da veia porta ou qualquer condição que impedisse o uso seguro da sonda sobre o abdome foram excluídos. Os detalhes dos reagentes e equipamentos usados estão listados na Tabela de Materiais.
1. Seleção do transdutor
- Selecione um transdutor de baixa frequência: o transdutor de matriz de setor (também conhecido como "phased array"; 1-5 MHz) pode ser selecionado por sua pegada menor21; o transdutor curvilíneo (2-5 MHz) pode servir como substituto.
NOTA: Em algumas máquinas, a sonda curvilínea desativará o bloqueio do eletrocardiograma, enquanto a sonda da matriz setorial permitirá o bloqueio do eletrocardiograma. Mas se o gating de eletrocardiograma estiver disponível com a sonda curvilínea ou de matriz de setor, é preferível usar a curvilínea para maximizar a visualização do sinal Doppler colorido.
2. Configurações da máquina
- Para todas as visualizações, defina a profundidade de forma que o alvo da varredura apareça no terço médio da tela de ultrassom (a configuração típica é entre 16-20 cm).
- Para todas as visualizações, defina o ganho de forma que o lúmen dos vasos sanguíneos pareça anecóico (preto), as paredes dos vasos pareçam hiperecoicas (brilhantes) e as estruturas circundantes pareçam intermediárias entre esses extremos.
3. Posicionamento do paciente e do ultrassonografista
- Durante a maior parte do exame, posicione o paciente em decúbito dorsal.
- Ao obter imagens da veia cava inferior (VCI), peça ao paciente para levantar os pés na cama (ou seja, flexionar os quadris) para relaxar os músculos abdominais e permitir a otimização da imagem.
- Ao fazer imagens do rim direito, reposicione o paciente na posição de decúbito lateral esquerdo para melhor visualização do rim direito.
- Antes do exame, exponha a parte inferior do tórax e o abdômen do paciente.
- Posicione a máquina de ultrassom de forma que a mão dominante do ultrassonografista possa segurar a sonda de ultrassom. Isso permite uma manipulação mais precisa da sonda de ultrassom e libera a mão não dominante para operar a máquina de ultrassom. Por exemplo, ultrassonografistas destros devem se posicionar com o paciente do lado direito e vice-versa.
4. Modo, predefinições e configuração
- Selecione o modo bidimensional (2-D), também chamado de modo de brilho (modo B).
- Selecione a predefinição Cardíaco .
- Configure o bloqueio do eletrocardiograma conectando os eletrodos na máquina de ultrassom e colocando-os na orientação padrão na pele do paciente.
NOTA: O exame VExUS pode ser realizado na predefinição cardíaca ou abdominal , mas em muitas máquinas, a predefinição abdominal desativará o bloqueio do eletrocardiograma, enquanto a predefinição cardíaca permitirá o bloqueio do eletrocardiograma. Portanto, se o bloqueio de eletrocardiograma estiver disponível em uma determinada máquina, é preferível usar qualquer predefinição que permita o bloqueio de eletrocardiograma.
5. Imagem da veia cava inferior (VCI)
- Gel
- Aplique gel diretamente na sonda de ultrassom para maximizar a eficiência da varredura antes de adquirir cada imagem.
- Visão subxifóide
- Coloque a sonda abaixo do processo xifóide com o indicador apontando cranialmente (Figura 1).
- Ajuste a posição da sonda até que a VCI seja vista em seu diâmetro ântero-posterior máximo (Figura 2).
- Enquanto mantém o IVC no centro da tela, gire a sonda 90 graus no sentido anti-horário para obter um eixo curto view do IVC (Figura 3).
- Aquisição de clipe de cinema: Para máquinas configuradas para aquisição de imagem retrospectiva, clique em adquirir após a etapa 5.2.3. Para máquinas configuradas para aquisição de imagem prospectiva, clique em adquirir antes da etapa 5.2.3.
- Vista do flanco direito
- Em pacientes com contraindicações para imagens subxifóides, coloque a sonda ao longo da linha axilar anterior direita no plano coronal do corpo com o indicador da sonda apontando cranialmente (Figura 4).
- Ajuste a posição da sonda até que a VCI seja vista em seu diâmetro ântero-posterior máximo.
- Enquanto mantém o IVC no centro da tela, gire a sonda 90 graus no sentido anti-horário para obter um eixo curto view do IVC.
- Aquisição de clipe de cinema: Para máquinas configuradas para aquisição de imagem retrospectiva, clique em adquirir após a etapa 5.3.3. Para máquinas configuradas para aquisição de imagem prospectiva, clique em adquirir antes da etapa 5.3.3.
- Avaliação IVC
- Se a VCI tiver >2 cm de diâmetro máximo anterior-posterior (Figura 5), prossiga para a etapa 6.
- Se a VCI for <= 2 cm (Figura 3), a VExUS não é indicada. Use o julgamento clínico ou outras ferramentas para avaliar o status do volume.
6. Doppler da veia hepática
- Gel
- Aplique gel diretamente na sonda de ultrassom para maximizar a eficiência da varredura antes de adquirir cada imagem.
- Vista do flanco direito
- Coloque a sonda ao longo da linha axilar anterior direita no plano coronal do corpo com o indicador da sonda apontando cranialmente (Figura 4).
- Ajuste a posição da sonda até que a veia hepática seja visualizada esvaziando na VCI perto da junção cavo-atrial (Figura 6).
- Selecione o modo Doppler colorido na máquina de ultrassom.
- Mova a caixa de cores para que a maior parte da embarcação fique dentro de suas bordas.
- Selecione o modo PW Doppler na máquina de ultrassom.
- Mova a porta Doppler para que fique localizada dentro do lúmen da veia hepática.
- Ative o PW Doppler.
- Peça ao paciente para prender a respiração no final da expiração.
- Permita que ocorra uma tela inteira do rastreamento PW Doppler e clique em Congelar (ou equivalente) (Figura 7).
- Clique em Adquirir (ou equivalente) para salvar imagens estáticas do rastreamento de fluxo.
7. Doppler da veia porta
- Gel
- Aplique gel diretamente na sonda de ultrassom para maximizar a eficiência da varredura antes de adquirir cada imagem.
- Vista do flanco direito
- Coloque a sonda ao longo da linha axilar anterior direita no plano coronal do corpo com o indicador da sonda apontando cranialmente (Figura 4).
- Ajuste a posição da sonda até que a veia porta seja visualizada (Figura 8).
- Selecione o modo Doppler colorido na máquina de ultrassom.
- Mova a caixa de cores para que a maior parte do vaso fique dentro de suas bordas.
- Selecione o modo PW Doppler na máquina de ultrassom.
- Mova a porta Doppler para que ela fique localizada dentro do lúmen da veia porta.
- Ative o PW Doppler.
- Peça ao paciente para prender a respiração no final da expiração.
- Permita que ocorra uma tela inteira do rastreamento PW Doppler e clique em Congelar (ou equivalente) (Figura 9).
- Clique em Adquirir (ou equivalente) para salvar imagens estáticas do rastreamento de fluxo.
8. Imagem das veias parenquimatosas renais
- Gel
- Aplique gel diretamente na sonda de ultrassom para maximizar a eficiência da varredura antes de adquirir cada imagem.
- Vista do flanco direito
- Coloque a sonda ao longo da linha axilar anterior direita no plano coronal do corpo com o indicador da sonda apontando cranialmente (Figura 4).
- Ajuste a posição da sonda até que o rim direito seja visto no eixo longo view.
- Selecione o modo Doppler colorido na máquina de ultrassom.
- Amplie a caixa Doppler colorida para conter a maior parte do córtex renal (Figura 10).
- Selecione o modo PW Doppler na máquina de ultrassom.
- Mova a porta Doppler para um local dentro do córtex renal que tenha uma leitura Doppler colorida.
- Ative o PW Doppler.
- Peça ao paciente para prender a respiração no final da expiração.
- Permita que ocorra uma tela inteira do rastreamento PW Doppler e clique em Congelar (ou equivalente) (Figura 11).
- Clique em Adquirir (ou equivalente) para salvar imagens estáticas do rastreamento de fluxo.
Resultados
O primeiro passo para o exame VExUS envolve imagens da veia cava inferior (VCI) para determinar se há sinais de pressões atriais direitas elevadas que qualificariam o paciente para o restante do exame. Ao obter imagens da VCI, é importante visualizá-la das perspectivas longitudinal e transversal para ver o vaso em sua dimensão máxima. Se a VCI for maior que 2 cm em seu diâmetro ântero-posterior máximo, o restante do exame pode ser realizado.
O próximo passo seria traçar o fluxo Doppler através da veia hepática. Isso é visualizado de maneira ideal na porção da veia hepática mais próxima da VCI. Em pacientes sem congestão venosa, o padrão de fluxo Doppler na veia hepática se assemelha mais a um traçado venoso central padrão, com uma onda sistólica e diastólica (s e d, equivalente às ondas x e y) fluindo abaixo da linha média (ou seja, para longe da sonda, para a VCI). Esse fluxo é acompanhado por ondas "a" e "v", que representam o chute atrial e o átrio direito cheios, respectivamente.
Em pacientes sem congestão venosa, o fluxo sistólico da veia hepática é geralmente mais rápido que o fluxo diastólico. À medida que a congestão venosa aumenta, o fluxo de sangue da veia hepática para a VCI durante a sístole torna-se mais prejudicado. Na congestão leve, o fluxo sistólico torna-se mais lento que o fluxo diastólico. À medida que a congestão venosa se torna mais grave, o fluxo sistólico eventualmente se inverte, de modo que há fluxo para trás durante a sístole cardíaca. A reversão do fluxo sistólico se correlaciona com congestão venosa moderada a grave (Figura 12).
O próximo exame VExUS é o traçado Doppler da veia porta. Entre as veias hepática e porta estão os sinusóides hepáticos, que atuam como um leito para absorver as flutuações usuais de fluxo observadas nas veias centrais, como as veias hepática e jugular. Assim, o fluxo venoso na veia porta é geralmente contínuo e unidirecional em direção à sonda. Isso faz com que o fluxo seja medido como positivo (ou seja, acima da linha de base) no traçado Doppler. O fluxo normal da veia porta tem um índice de pulsatilidade (IP) inferior a 30%. O IP é definido como a medida da variação do fluxo sanguíneo durante o ciclo cardíaco. É calculado dividindo a diferença entre as velocidades máxima e mínima do fluxo pela velocidade máxima do fluxo. À medida que o paciente fica mais congestionado, o fluxo se torna mais pulsátil. A congestão leve tem um IP de 30% a 49% e o fluxo anormal moderado a grave é >50% pulsátil (Figura 13).
Finalmente, obtém-se o traçado de fluxo Doppler da veia intrarrenal. Depois de encontrar os rins, o Doppler colorido é usado para localizar regiões de fluxo. Em seguida, a porta Doppler pulsada é colocada sobre uma área de fluxo dentro do parênquima renal. Os pequenos vasos no córtex renal são tipicamente muito próximos uns dos outros, por isso é comum capturar o fluxo arterial e venoso simultaneamente. O fluxo arterial será positivo (acima da linha de base) e pode ser usado para determinar o índice de resistência renal (não faz parte do exame VExUS). O fluxo venoso será negativo (ou seja, abaixo da linha de base). O fluxo venoso será negativo e, normalmente, deve parecer contínuo. À medida que a congestão venosa aumenta, o fluxo venoso intrarrenal torna-se inicialmente pulsátil e bifásico com ondas sistólicas e diastólicas, indicando congestão venosa leve. À medida que a congestão aumenta em gravidade, o fluxo sistólico acabará cessando, levando a um fluxo pulsátil e monofásico apenas durante a diástole (Figura 14).
Depois que um paciente é excluído para o exame VExUS por ter uma VCI >2 cm de diâmetro máximo, todo o exame é realizado para dar ao paciente uma nota VExUS. Os traçados normais recebem uma pontuação de 0, os levemente anormais uma pontuação de 1 e os moderados a gravemente anormais uma pontuação de 2. O grau VExUS de um paciente é determinado pelo número de traçados anormais. Um grau VExUS de 1 é dado àqueles com uma VCI aumentada e qualquer combinação de pontuações 0 ou 1. Um grau VExUS de 2 é dado àqueles com uma VCI aumentada e pelo menos uma pontuação de 2. Um grau VExUS de 3 é dado àqueles com uma VCI aumentada e duas ou mais pontuações de 2. Um grau VExUS de 3 está intimamente associado ao risco de LRA devido à congestão venosa (Figura 15).
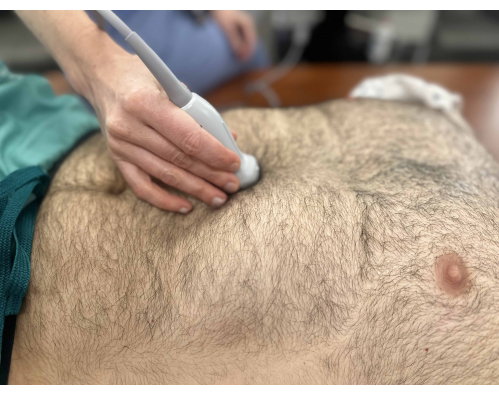
Figura 1: Transdutor para a área subxifóide para visualização da veia cava inferior na visão de eixo longo. O marcador da sonda está apontando para a cabeça do paciente. Clique aqui para ver uma versão maior desta figura.

Figura 2: Visão de eixo longo da veia cava inferior. Abreviaturas: RA, átrio direito; HV, veia hepática; VCI, veia cava inferior. Clique aqui para ver uma versão maior desta figura.
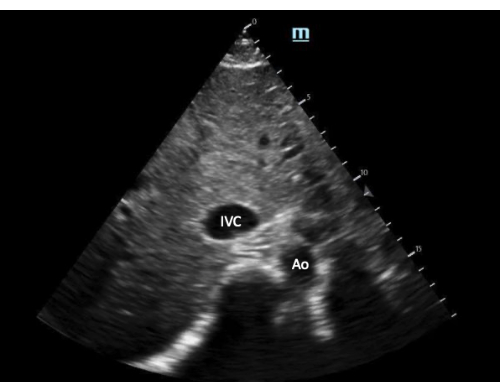
Figura 3: Visão de eixo curto da veia cava inferior. Abreviaturas: Ao, aorta; VCI, veia cava inferior. Clique aqui para ver uma versão maior desta figura.

Figura 4: Transdutor para a linha axilar anterior direita para visualização das veias hepática, portal e intrarrenal. O marcador da sonda está apontando para a cabeça do paciente e, portanto, não é visível na imagem. Clique aqui para ver uma versão maior desta figura.

Figura 5: Visão de eixo curto da veia cava inferior com diâmetro ântero-posterior maior que 2,0 cm. Abreviaturas: HV, veia hepática; VCI, veia cava inferior. Clique aqui para ver uma versão maior desta figura.
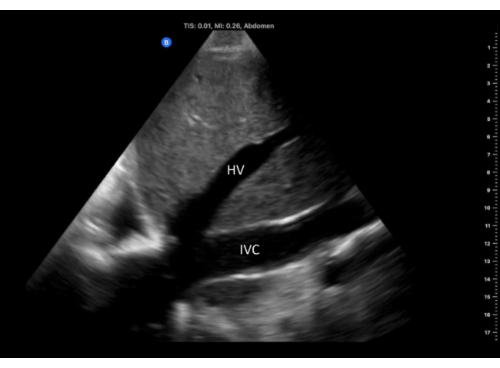
Figura 6: Visão de eixo longo da VCI com a veia hepática esvaziando nela, fotografada da janela do flanco direito. Abreviaturas: HV, veia hepática; VCI, veia cava inferior. Clique aqui para ver uma versão maior desta figura.

Figura 7: Porta Doppler pulsada dentro do lúmen da veia hepática com o traçado de fluxo. Imagem com Doppler colorido ativado. Clique aqui para ver uma versão maior desta figura.

Figura 8: Visão do eixo longo da veia porta, fotografada da janela do flanco direito. Abreviaturas: VP, veia porta. Clique aqui para ver uma versão maior desta figura.

Figura 9: Porta Doppler pulsada dentro do lúmen da veia porta, com o traçado de fluxo abaixo. Imagem com Doppler colorido ativado. Clique aqui para ver uma versão maior desta figura.
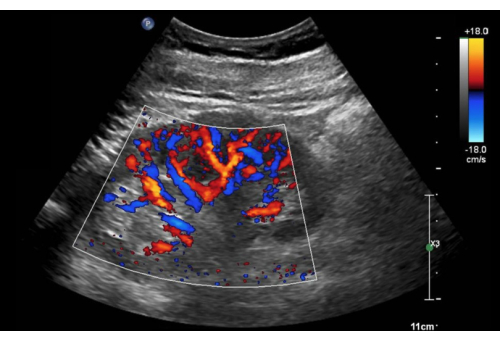
Figura 10: Visão do eixo longo do rim direito com Doppler colorido ativado. Clique aqui para ver uma versão maior desta figura.
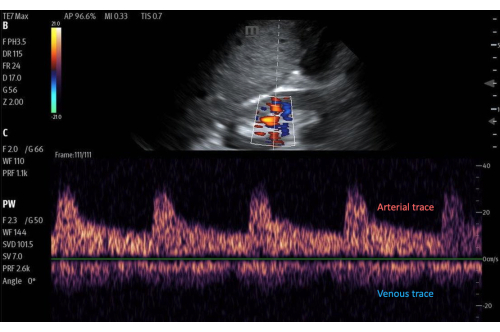
Figura 11: Porta Doppler pulsada em uma área de fluxo dentro do córtex renal, com o traçado de fluxo abaixo. Imagem com Doppler colorido ativado. Clique aqui para ver uma versão maior desta figura.

Figura 12: Diferentes fenótipos da forma de onda Doppler da veia hepática com graus variados de congestão. Esta figura foi reutilizada de Koratala, A.22. Clique aqui para ver uma versão maior desta figura.
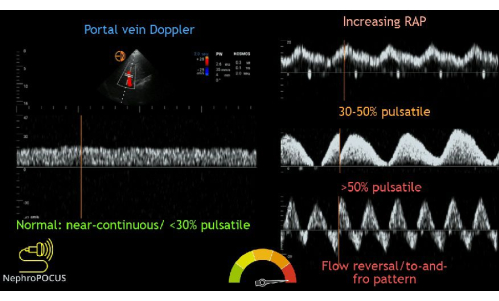
Figura 13: Diferentes fenótipos da forma de onda Doppler da veia porta com graus variados de congestão. Esta figura foi reutilizada de Koratala, A.22. Clique aqui para ver uma versão maior desta figura.
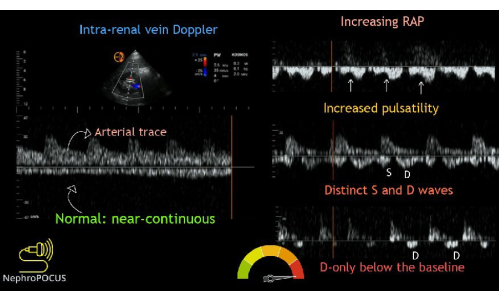
Figura 14: Diferentes fenótipos da forma de onda Doppler da veia intrarrenal com graus variados de congestão. Esta figura foi reutilizada de Koratala, A.22. Clique aqui para ver uma versão maior desta figura.

Figura 15: Combinação das várias formas de onda com uma descrição do sistema de pontuação VExUS. Esta figura foi reutilizada de Koratala, A.22. Clique aqui para ver uma versão maior desta figura.
Discussão
Etapas críticas
O VExUS foi desenvolvido em pacientes pós-cirurgia cardíaca para quantificar a congestão venosa de forma não invasiva, mas o utilitário se expandiu para seu uso para auxiliar na avaliação da congestão venosa e avaliação do estado hídrico em vários contextos clínicos. Para realizar o exame corretamente, várias etapas críticas devem ser consideradas. Primeiro, para maximizar o rendimento diagnóstico do exame, deve-se considerar os requisitos do exame VExUS ao selecionar um transdutor e predefinição23. Especificamente, o rendimento do exame é maximizado usando uma sonda curvilínea que permite o bloqueio do eletrocardiograma. Se a sonda curvilínea de um determinado dispositivo não permitir o bloqueio de eletrocardiograma, mas fios de eletrocardiograma compatíveis estiverem disponíveis, a próxima melhor escolha é uma sonda phased-array com bloqueio de eletrocardiograma. No entanto, se os fios de eletrocardiograma compatíveis com o dispositivo simplesmente não estiverem disponíveis, uma sonda curvilínea na predefinição cardíaca ou abdominal pode ser usada.
Em segundo lugar, é quase sempre útil visualizar o IVC nas visualizações de eixo longo e curto. Isso é necessário para excluir com mais precisão os pacientes dentro ou fora do protocolo. A visão de eixo longo da VCI é notoriamente propensa a erros, especialmente para ultrassonografistas menos experientes2. Se a VCI não for visualizada no plano correto, pode-se subestimar o tamanho do vaso. Para minimizar o erro, visualizá-lo na visão de eixo curto pode não apenas mostrar o diâmetro máximo de forma confiável, mas também pode ajudar a diferenciar a verdadeira colapsabilidade da VCI da pseudo-colapsabilidade (ou seja, movimento fora do plano do vaso11).
Terceiro, ao obter traçados de fluxo venoso, é importante manter uma mão de varredura estável assim que o PW Doppler for ativado. Ao contrário do Doppler de onda contínua, o PW Doppler usa uma "porta" a partir da qual analisa os sinais de ultrassom de um local específico ao longo do tempo. Uma vez que o PW Doppler é ativado, a imagem mostrada ao ultrassonografista é uma imagem estática obtida no momento de iniciar o modo PW Doppler. Se o ultrassonografista ou o paciente se moverem um em relação ao outro, a localização do portão mudará e alterará a precisão da imagem bidimensional exibida. Assim, é vital manter uma mão de varredura estável quando o vaso alvo estiver à vista e o modo PW Doppler estiver ativado. Além disso, fazer com que um paciente fique parado e prenda a respiração no final da expiração por alguns segundos ajuda a eliminar a variação respiratória enquanto o PW Doppler está sendo utilizado.
Finalmente, é importante notar que os exames VExUS não são apenas úteis no diagnóstico de congestão venosa, mas também são úteis no monitoramento da resposta ao tratamento ao longo do tempo24. Uma das principais utilidades desse sistema de pontuação é quando ele é implementado em série ao longo de uma hospitalização ou curso de tratamento para avaliar a eficácia das medidas descongestivas implementadas.
Modificações e solução de problemas
Dois aspectos do exame VExUS que geralmente frustram os alunos são (1) falta de disponibilidade de hardware de eletrocardiograma e (2) incapacidade de localizar o fluxo intrarrenal.
Dentro do exame VExUS, a interpretação de todas as três formas de onda Doppler extracardíacas é melhorada pelo eletrocardiograma. Dessas três formas de onda, o eletrocardiograma é o mais essencial para a avaliação do fluxo da veia hepática12. O traçado do fluxo da veia hepática contém várias ondas, algumas acima e outras abaixo da linha de base. Assim, muitas vezes é necessário usar o eletrocardiograma para identificar se cada onda é normal ou patológica e, especificamente, para determinar se a velocidade sistólica ou diastólica é mais rápida. Mas, na ausência de bloqueio de eletrocardiograma, pode-se usar os dados VExUS da veia não hepática na maioria dos casos para tirar conclusões sobre o estado de congestão de um paciente. Especificamente, mesmo que apenas 75% do exame seja realizado (VCI, veias portal e intrarrenal), em muitos casos, uma determinação suficiente pode ser feita sobre o estado de congestão que existe em qualquer paciente, especialmente porque apenas 2 padrões de fluxo gravemente anormais indicam o grau máximo de VExUS de 3. No entanto, uma abordagem sem eletrocardiograma tem maior probabilidade de gerar dados VExUS inconclusivos por dois motivos: (1) um traçado Doppler da veia intrarrenal sem eletrocardiograma pode ser difícil de interpretar se o sinal arterial intrarrenal não for proeminente e (2) para a veia porta, o bloqueio do eletrocardiograma pode ajudar a diferenciar a pulsatilidade respiratória da cardíaca. Por esses motivos, o uso de eletrocardiograma é preferido sempre que possível.
Em segundo lugar, encontrar o sinal de fluxo da veia intrarrenal pode ser um desafio25. Se o rim estiver localizado a mais de 16 cm da sonda, o aumento da atenuação das ondas de ultrassom durante sua jornada entre o transdutor e o rim pode causar degradação do sinal Doppler (ou seja, falta de cor). Isso pode ser melhorado movendo a sonda mais lateral e posteriormente no corpo do paciente, aproximando o rim do transdutor. Se o fluxo ainda não for visualizado, pode-se diminuir a escala Doppler para que ela detecte um fluxo mais lento. Uma velocidade de fluxo entre 12 cm/s e 25 cm/s é tipicamente suficiente para visualizar a vasculatura intrarrenal. Além disso, também é possível aumentar o ganho do Doppler para melhorar a sensibilidade ao fluxo, aumentando o rendimento dessa porção do exame. Ao aumentar o ganho, deve-se ter cuidado com a maior probabilidade de visualizar um artefato que pode ser confundido com fluxo. O modo Power Doppler também pode ser usado, pois normalmente é melhor na detecção de fluxo mais lento. Se, após essas modificações, um ultrassonografista ainda estiver tendo problemas para encontrar o fluxo no rim à direita, ele pode tentar o rim contralateral e implementar as mesmas alterações nesse lado.
Limitações
Embora o VExUS tenha surgido como um exame confiável e não invasivo para ajudar a orientar a avaliação do lado direito do circuito hemodinâmico, ele tem algumas limitações importantes. Primeiro, existem muitas condições nas quais o VExUS não é validado, incluindo cirrose e doença renal terminal (DRT)7. Na cirrose, há uma alteração nas pressões dentro do fígado, devido ao tecido fibroso, que pode alterar a capacidade do tecido hepático de servir como uma "esponja" que absorve as pressões cardíacas. Assim, tanto o fluxo hepático quanto o da veia porta podem ser alterados. Além disso, pode haver trombos hepáticos ou da veia porta que, novamente, podem levar a uma interpretação errônea do fluxo dentro desses vasos. Além disso, na DRT, os rins tornam-se atróficos com a diminuição do fluxo sanguíneo, dificultando a interpretação do fluxo venoso renal. No entanto, apesar dessas limitações, há relatos de casos demonstrando que o VExUS poderia potencialmente ter valor mesmo em pacientes com cirrose26 e/ou doença renal terminal27, servindo como um método para monitorar o tratamento da congestão venosa ao longo do tempo.
Em segundo lugar, é importante notar que o VExUS ainda é um novo protocolo para estimar a congestão venosa e, portanto, há alguns dados que sugerem que não é a maneira mais confiável ou útil de estimar a congestão venosa. Em um estudo observacional de 2023 publicado no Journal of Critical Care, Andrei et al. mostraram que, em uma coorte de pacientes de UTI, não houve associação significativa entre os escores VExUS e LRA ou mortalidade em 28 dias28. Esta foi uma pequena coorte; no entanto, a prevalência geral de congestão venosa moderada a grave foi baixa. Em um grupo com maior prevalência de congestão venosa, como pacientes com síndrome cardiorrenal, Islas-Rodriguez et al.29 mostraram que, embora o uso de VExUS para guiar a descongestão tenha ajudado a alcançar isso, não aumentou a probabilidade de recuperação da função renal.
Em terceiro lugar, há uma falta de consenso sobre a interpretação da VExUS em pacientes com disfunção ventricular direita pré-existente e/ou regurgitação tricúspide significativa. Conceitualmente, parece razoável usar o VExUS como um monitor de tendências nesses pacientes para tentar diferenciar disfunção versus falha da circulação cardíaca direita. No entanto, não temos conhecimento de nenhum estudo até o momento que tenha validado esse conceito.
Em quarto lugar, o VExUS exclui pacientes com VCIs que medem menos de 2,0 cm de diâmetro anterior-posterior, o que pode não detectar congestão venosa em pacientes com habitus corporal pequeno. Em outras palavras, se uma mulher de 5 pés e um homem de 7 pés tiverem uma VCI de 1,9 cm, esses dois pacientes serão excluídos da triagem VExUS adicional para congestão venosa. No entanto, isso está em desacordo com outras práticas ecocardiográficas que incorporaram cada vez mais a indexação à área de superfície corporal para normalizar as medidas ultrassonográficas do tamanho corporal30.
Quinto, o protocolo VExUS provavelmente encontrará problemas em casos de hipertensão intra-abdominal (IAH). Na HIA, os pacientes provavelmente apresentam uma VCI pequena (<2,0 cm), pois a alta pressão intra-abdominal pode comprimir extrinsecamente o vaso31. Isso significa que a maioria dos pacientes com HIA será automaticamente excluída de uma avaliação adicional do VExUS assim que um pequeno tamanho de VCI for detectado. No entanto, a HIA pode ser causada por congestão venosa, e essa congestão não seria detectada pelo VExUS devido à exclusão automática de pacientes com pequeno calibre de VCI. Além disso, os pacientes com HIA, em geral, são provavelmente candidatos ruins para VExUS. Isso ocorre porque, na HIA, há compressão extrínseca de todas as veias intra-abdominais, e as formas de onda Doppler dessas veias refletirão um equilíbrio entre compressão extrínseca e congestão intramural, dificultando a interpretação das formas de onda Doppler apenas para congestão.
Direções futuras
A iteração atual do protocolo VExUS pode evoluir com o tempo por vários caminhos. Primeiro, o protocolo VExUS atual inclui apenas uma única medição ântero-posterior da VCI obtida a partir de uma visão de eixo longo da VCI subxifóide. No entanto, essa visão única pode ser enganosa, e há evidências de que uma estimativa mais robusta da pressão do átrio direito pode ser obtida adicionando uma incidência de eixo curto da VCI para medir o índice de esfericidade da VCI: razão entre os diâmetros lateral-medial e ântero-posterior da VCI32. Em segundo lugar, o protocolo VExUS atual mede apenas o diâmetro máximo da VCI e não leva em consideração a colapsabilidade da VCI. Portanto, o protocolo VExUS atualmente exclui pacientes com uma VCI de < = 2 cm de diâmetro que, no entanto, têm CIVs não dobráveis. Por outro lado, o protocolo VExUS atual trata pacientes com VCI grande (>2 cm) e dobrável como tendo algum grau de congestão venosa. Pesquisas futuras são necessárias para determinar se a colapsibilidade da VCI deve ser usada como critério de triagem para o exame VExUS. Terceiro, as formas de onda da veia femoral podem ser úteis para aqueles com dificuldade em prender a respiração. O fluxo Doppler da veia femoral (FVD) deve ser contínuo em casos normais, mas à medida que a congestão venosa aumenta, o fluxo se torna cada vez mais pulsátil, levando a interrupções significativas do fluxo. A FVD pode emergir como uma expansão útil do protocolo VExUS atual para permitir a utilidade desse exame em uma proporção maior de pacientes33. Em quarto lugar, há evidências de que existem dados semelhantes sobre a congestão venosa fornecidos por ambas as medidas da veia jugular interna e da VCI34. Estudos futuros devem examinar se os parâmetros da veia jugular podem substituir a VCI no protocolo VExUS em situações em que a VCI é difícil de visualizar.
É provável que o protocolo VExUS evolua à medida que a tecnologia de ultrassom integra amplamente mais funcionalidades, especialmente aprendizado de máquina (ML) e inteligência artificial (IA)35. A integração de ML/IA no hardware e software de ultrassom deve ser capaz de automatizar muitos aspectos do protocolo VExUS que atualmente são trabalhosos. Por exemplo, algumas máquinas existentes já são capazes de medir a colapsabilidade da VCI automaticamente e devem, em princípio, um dia também ser capazes de medir a esfericidade da VCI.
Além disso, seria altamente benéfico para as máquinas de ultrassom oferecer tecnologia de bloqueio de eletrocardiograma virtual assistida por IA, já que muitas máquinas de ultrassom no local de atendimento atualmente não possuem cabos físicos de eletrocardiograma. Isso ajudaria muito os médicos a interpretar os padrões de fluxo na veia hepática na ausência de recursos de bloqueio de eletrocardiograma.
Finalmente, a inteligência artificial que obtém o rastreamento Doppler de onda pulsada de um vaso alvo automaticamente pode ajudar a achatar a curva de aprendizado já bastante íngreme que existe para o VExUS36. Essa tecnologia já existe para estimativa do débito cardíaco obtendo a medição automática da integral do tempo de velocidade da via de saída do VE (LVOT VTI), portanto, expandi-la para os vasos hepáticos, portais e intrarrenais não está além das possibilidades neste estágio da tecnologia de ultrassom.
Em resumo, a avaliação do circuito hemodinâmico com POCUS é vital no manejo de pacientes agudamente enfermos37. No entanto, devido à falta de treinamento padronizado em aquisição e interpretação de imagens, o VExUS permanece subutilizado. Esta revisão apresenta uma estrutura para aquisição e interpretação de imagens do exame VExUS de um grupo de médicos abrangendo uma variedade de especialidades. Por sua vez, este protocolo pode ser usado para ensinar e aprender VExUS para melhorar a capacidade dos médicos de avaliar a congestão venosa e monitorar seu tratamento ao longo do tempo.
Divulgações
YSB relata ter recebido honorários da Sociedade Americana de Anestesiologistas pelo trabalho do Conselho Editorial em Ultrassom Point-of-Care e de OpenAnesthesia.org pela criação de conteúdo educacional relacionado ao POCUS. Os demais autores não têm divulgações.
Agradecimentos
Nenhum.
Materiais
| Name | Company | Catalog Number | Comments |
| 5500P Ultrasound System | Philips | HC795143 | Used to obtain a subset of the Figures and Videos |
| Affiniti 70 Ultrasound System | Philips | HC795210 | Used to obtain a subset of the Figures and Videos |
| Curvilinear Transducer (C1-5-D) | GE | 5409287-R | 1-5 MHz, also called the abdominal probe |
| Curvilinear Transducer (C5-1) | Philips | HC989605412041 | 2-5 MHz, also called the abdominal probe |
| Curvilinear Transducer (C5-1) | SonoSite | https://www.sonosite.com/products/ultrasound-transducers/c5-1 | 1-5 MHz, also called the abdominal probe |
| Curvilinear Transducer (C5-2s) | Mindray | https://lysis.cc/products/mindray-c5-2s | 1-5 MHz, also called the abdominal probe |
| Edge 1 Ultrasound Machine | SonoSite | Used to obtain a subset of the Figures and Videos | |
| Handheld Probe (Butterfly iQ3) | Butterfly | https://www.butterflynetwork.com/iq3?srsltid=AfmBOorvY6WqHGbdeWW gtefztEJa8pt_xbwSOc6hQuB2s-Kb0wRlsCLR | Used to obtain a subset of the Figures and Videos |
| LOGIQ P9 Ultrasound System | GE | H42752LS | Used to obtain a subset of the Figures and Videos |
| Lumify Handheld Ultrasound | Philips | Used to obtain a subset of the Figures and Videos | |
| Phased-Array Transducer (3Sc-D) | GE | https://services.gehealthcare.in/gehcstorefront/p/5863286 | 1-5 MHz, also called the cardiac probe |
| Phased-Array Transducer (P4-2s) | Mindray | https://lysis.cc/products/mindray-p4-2s | 1-5 MHz, also called the cardiac probe |
| Phased-Array Transducer (P5-1) | SonoSite | https://www.sonosite.com/in/products/ultrasound-transducers/p5-1 | 1-5 MHz, also called the cardiac probe |
| Phased-Array Transducer (S4-1) | Philips | HC989605389271 | 1-5 MHz, also called the cardiac probe |
| TE7 Max Ultrasound System | Mindray | https://www.mindray.com/na/products/ultrasound/point-of-care/te-series/te-7-max-portable-ultrasound-machine/ | Used to obtain a subset of the Figures and Videos |
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoExplore Mais Artigos
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados