Method Article
新しいミニオープン経椎間孔腰椎椎体間固定術
要約
このプロトコルは、術中の失血を大幅に減らすことができる新しいミニオープンTLIFを導入し、回復を促進して低侵襲の結果を達成します。
要約
経椎間孔腰椎椎体間固定術(TLIF)は、さまざまな脊椎の病状、特に変性疾患を管理するための効果的で人気のある外科的処置です。TLIFの登場以来、外科医は低侵襲技術を追求してきました。現在、TLIFは、開腹手術、低侵襲手術、または経皮的内視鏡検査による経椎間孔アプローチを通じて実施できます。この研究では、ミニオープン TLIF と呼ばれる経皮的椎弓根スクリューを使用した修正オープン TLIF の詳細な説明を提供します。目的は、この手順の実現可能性とその予備的な結果を提示することです。2021年1月から施術が行われており、選択基準を満たす患者数は300人を超えています。収集されるデータには、手術時間、失血、歩行時間、ヘマトクリット値、周術期合併症が含まれます。臨床症状は、術後1週間、3ヶ月、12ヶ月で評価されます。腰痛と脚痛のビジュアルアナログスケール(VAS)スコアとオスウェストリー障害指数(ODI)が評価されます。磁気共鳴画像法は、術前と術後 12 か月に実施され、傍脊髄筋の断面積を測定します。腰椎椎体間固定率は、CTスキャンを使用して評価されます。この手順は、臨床診療で最も一般的な腰椎変性疾患に適用できます。現在収集されているデータによると、シングルレベルの平均手術時間は102.3分、マルチレベルの手術の平均時間は130.2分でした。術中失血は、シングルレベル手術で平均62.5 mL、マルチレベル手術で108.3 mLでした。VASおよびODIスコアは、術後に有意な改善を示し(p < 0.001)、臨床的に重要な差は最小限に抑えられました。傍脊髄筋萎縮率は、症候性側で2.5%、無症候性側で1.2%でした。断面積の変化と萎縮率は統計的に有意ではありません(p > 0.05)。MO-TLIFは、特にマルチレベルの症例で、筋肉の損傷を最小限に抑え、手術時間を短縮して、腰椎変性疾患の治療に効果的かつ実現可能です。
概要
腰椎変性疾患(LDD)は高齢者に多くみられ、腰椎椎間板ヘルニアや腰椎管狭窄症を呈することが多く、慢性的な腰痛や神経症状として現れます1。1980 年代に導入されて以来、経椎間孔腰椎椎体間固定術 (TLIF) は進化し、腰椎変性疾患を治療するための最も古典的で確立された外科的処置の 1 つであり続けています2。2002年、Foleyらは低侵襲手術による経椎間孔腰椎椎体間固定術(MIS-TLIF)3,4,5を導入しました。2012年、Osmanらは、腰椎固定術6,7にシングルチャンネル内視鏡を使用したことを報告しました。2018年、Kim氏とChoi氏は片側バイポータル内視鏡検査(UBE)を導入し、TLIFの手術に応用することに成功し、バイポータル内視鏡TLIF(BE-TLIF)と名付けました8。
近年、MIS-TLIFとPE-TLIFが徐々に採用されたことで、従来の手術と比較して、臨床転帰と患者の満足度が大幅に向上しています9。一部の学者は、内視鏡技術が最終的には開腹手術に取って代わると信じているとさえ信じています。しかし、従来の開腹手術も継続的に改善され、侵襲性が低くなっており、修正されたTLIFが広く受け入れられている開腹手術として浮上しています10。修正されたTLIFには、棘突起に沿って腰椎筋膜を切開し、棘突起に付着した筋肉と靭帯、および骨膜の下の椎弓板を細心の注意を払って剥離し、広範な解剖や長期の引っ込みなしに椎弓根を露出させることが含まれます。この技術は、Wiltseアプローチ11と比較して、同様の低侵襲結果を達成します。
これに関連して、この研究は革新的に提案します 経皮的椎弓根スクリューによって支援された低侵襲アプローチ、ミニオープンTLIF(MO-TLIF)のさらなる進歩。多くの研究は、後腰椎手術がしばしば術後傍脊髄筋萎縮を引き起こすと報告しており、これはおそらく手術中の背中の筋肉の長期収縮に関連しており、これは腰痛(LBP)と神経根症状に関連しています12,13,14。Mengiardi らは、多裂筋への脂肪浸潤の増加がしばしば慢性的な腰痛を引き起こすことを発見し7、Hyun らは腰椎神経根症と筋除神経萎縮との関連を示唆しました12。他の研究では、傍脊髄筋萎縮症は腰椎変性疾患の症状の発生と悪化と密接に関連していることが示されています15。傍脊髄筋の量と機能は、腰椎と骨盤の矢状バランスを維持する上で重要な役割を果たし、術後の腰椎の安定性に不可欠です16。したがって、傍脊髄筋への影響は、脊椎固定術の外科的アプローチと技術を選択する際の重要な考慮事項であり、前方または低侵襲の後方アプローチが筋肉の混乱を軽減します17。
この研究では、MO-TLIF で治療された単一レベルおよびマルチレベルの腰椎変性症の患者における傍脊髄筋の短期臨床効果と変化を前向きに分析します ( 表 1 に示すように、平均年齢 54.8 ± 17.5 歳の男性 47 人女性)。手術の有効性、失血、固定結果、疼痛および機能スコア、および傍脊髄筋の破壊を評価し、これらの転帰を同じ期間に修正TLIFを受けた患者と比較した。この比較は、腰椎変性疾患の治療における MO-TLIF の利点、特に傍脊髄筋への影響を調査することを目的としています。
プロトコル
この研究は、ヘルシンキ宣言の原則に沿って実施されました。東呉大学第二附属病院の倫理委員会によって承認が与えられました(No.JD-LK2023045-I01)です。インフォームドコンセントは、研究に含まれるすべての個々の参加者から得られました。記事内のすべての画像は、人間の研究参加者のインフォームドコンセントを得ています。
1. 包含基準と除外基準
- 次の選択基準を使用してください: 臨床的に診断された シングルレベルまたはマルチレベルの腰椎椎間板ヘルニア、腰椎狭窄症、腰椎不安定性、またはグレード I または II 腰椎すべり症;-持続性の腰痛および/または脚の痛み、しびれ、または3か月間保存的治療に反応しなかった脱力感。
- 次の除外基準を使用してください: 再手術;脊柱側弯症、強直性脊椎炎、新たな脊椎骨折、脊髄腫瘍、またはその他の悪性腫瘍の存在;グレードIII以上の腰椎すべり症;凝固障害のある患者。
2.外科的処置
- 術前準備
- 全身麻酔下で手術を受けるすべての患者を、放射線透過性の脊椎手術台にうつ伏せに置きます。胸部と骨盤部の下に適切なサイズのサポートパッドまたはクッションを配置して、胸部と骨盤をそれぞれ持ち上げます。サポートの高さと角度を微調整して、体間の露出を最大化し、腹部が自由に垂れ下がるようにして、下大静脈の圧迫を防ぎます。
注:一般的に、10°から15°の前方腰椎前弯症と適切な骨盤傾斜は、最高の椎間腔露出を達成するために最適であると考えられています。手術中の微調整は、望ましい曝露と患者の安全性のバランスをとるために重要です。 - まず、L5-S1 セグメントの識別から始めます。標準的な前後図に基づいて C アーム透視法の下でローカリゼーション ガイドを利用して、病変セグメントと患者の体上の椎弓根の表面投影を決定します。
- マーカーペンを使用して、正中線の外科的切開、椎弓根の表面突起、および椎弓根突起の横縁にある1cmの切開をマークします。
- 3つの別々のアプリケーションでヨードフォアで手術部位を消毒し、消毒剤を計画された切開部から少なくとも15cm延長して、適切な消毒マージンを作成します。術前のマーキングを汚したり、取り除いたりしないように注意してください。
- 切開部位の周囲に4つの滅菌ドレープを配置します。手術野の頭側端と尾側端の両方に外科用ドレープを塗布します。手術部位を大きな滅菌ドレープで覆い、所定の位置に固定します。
- 全身麻酔下で手術を受けるすべての患者を、放射線透過性の脊椎手術台にうつ伏せに置きます。胸部と骨盤部の下に適切なサイズのサポートパッドまたはクッションを配置して、胸部と骨盤をそれぞれ持ち上げます。サポートの高さと角度を微調整して、体間の露出を最大化し、腹部が自由に垂れ下がるようにして、下大静脈の圧迫を防ぎます。
- 手術アクセスチャネルの確立
- #3ブレードで腰のマークされた線に沿って10cmの縦方向に切開します(図1)。皮膚、皮下組織、胸腰筋膜を高周波エレクトロトームで順番に切り取ります。
- 棘突起に沿って傍脊髄筋を剥離し、影響を受けた棘突起、椎弓板、および高周波エレクトロトームで椎間関節の一部を露出させます。椎弓状開創器を下部椎骨の上面の外縁に配置して手術野を露出させ、通常は5分以内にアプローチチャネルを確立します。
- 減圧
- 超音波ボーンナイフまたは通常のボーンナイフを使用して、上関節下突起と下棘上突起の一部を取り除きます。腹側靭帯の一部を取り除き、硬膜と神経根を露出させます。その間、背側靭帯と硬膜外脂肪を保存して、正常な脊柱管の解剖学的構造への混乱を最小限に抑えます。
- 両側減圧または対側狭窄が必要な場合は、放射線透過性の脊椎手術台を反対側に傾けます。棘突起の基部を取り除き、反対側のくぼみに達するまで肥大性靭帯を切除します。このアプローチにより、270°の徹底的な減圧が達成されます。
- 神経根リトラクターで神経根と硬膜嚢を引っ込めて、手術領域を露出させます。#11メスで線維性輪を切開します。ケリソンで髄核を切除し、骨ロンジャーで端板軟骨をこすり落とし、骨の終板を露出させます。椎間板ノミで椎間腔を順次拡張し、通常の生理食塩水で洗い流して止血を達成します。
- 骨ロンジャーを使用して切除された関節突起と椎弓板の一部をトリミングし、約 2 mm2 のサイズの骨片を作成します。これらの骨移植片の一部をケージに詰め、残りの断片を椎間腔に配置します。ケージを椎間腔の中央に配置します。
- 超音波ボーンナイフまたは通常のボーンナイフを使用して、上関節下突起と下棘上突起の一部を取り除きます。腹側靭帯の一部を取り除き、硬膜と神経根を露出させます。その間、背側靭帯と硬膜外脂肪を保存して、正常な脊柱管の解剖学的構造への混乱を最小限に抑えます。
- 切開を閉じる
- 椎間固定装置の位置が適切であることを、横方向および前後方向の透視法によって確認します。ニューラルストリッパーを使用して硬膜嚢と神経根をプローブし、可動性が良好で、圧迫がなく、脊柱管の狭窄がないことを確認します。
- 生理食塩水で椎間腔を洗い流します。3-0吸収性縫合糸を使用して、ロック技術で筋膜層を閉じ、脂肪層に対して連続縫合を行います。好みや臨床要件に応じて、ステープルまたは縫合糸のいずれかを使用して皮膚を縫合します。この手順では、ドレナージを定期的に配置する必要はありません。
- 内部固定留置と閉鎖切開
- 目的の椎間腔の上下の椎骨の椎弓根の投影部位に 1 cm の切開を行います (マーカーは術前に作成されています)。
- 椎弓根の侵害や周囲の神経への損傷を避けるために、Cアーム透視法の下で次の手順を実行します。鋭利なトロカール針を皮膚に挿入して、茎にアクセスします。計画されたエントリーポイントに針を正確に配置してください。
- 正しい針の配置後、小径のリーマーを使用して椎弓根チャネルを徐々に拡大し、椎弓根スクリューに十分なスペースを確保します。専用のガイドシステムを使用して、椎弓根ネジとコネクティングロッドをリーマチャネルに挿入し、ネジキャップを締めます。切開部を生理食塩水で洗浄し、止血を徹底的に行います。
- 3-0吸収性縫合糸を使用して、切開部を層ごとに閉じ、ドレッシングで覆います。術後に下肢の活動を確認してください。
注:マルチレベル手術の場合、後部正中線切開は2つのセグメントで約4 cm、3つのセグメントで約5 cmです(図2)。外科的アプローチチャネルは、同じ方法を使用して確立でき、椎弓板開創器の位置を変更するだけで複数の椎間腔を減圧できます。マルチレベルの切開部をわずかに伸ばすと、手術スペースが広くなり、手術がより便利になり、外傷や出血を大幅に増加させることなく、より良い露出を提供できます。
3. 臨床評価
- 術前、術中、術後 1 週間、術後 3 か月、術後 12 か月で次のデータを収集します。手術時間、失血、術後歩行時間、フォローアップ時間、合併症、および腰椎および下肢の痛みに広く利用されているビジュアルアナログスケール(VAS)およびオスウェストリー障害指数(ODI)スコアを記録します18。
- 目盛り付き吸引バッグを使用して、手術中の目に見える失血を測定します。手術中に使用される生理食塩水などの液体の量を差し引きます。さらに、血液に浸したガーゼの重さを量ることにより、ガーゼが吸収する血液量を推定します。
- 術前および術後ヘマトクリット(Hct)を使用して失血を計算します。Nadler 式19 を使用して、患者の推定血液量 (EBV) を決定します。
EBV(mL)=[k1×高さ(m)3 +k2×体重(kg)+k3]×1000]
男性の場合:k1=0.3669、k2=0.03219、k3=0.6041。女性の場合: k1=0.3561, k2=0.03308, k3=0.1833. - 続いて、総失血量(TBL)をグロス式20を使用して計算します
TBL(mL)=EBV(mL)×(HctPre−HctPost)/HctAve
ここで、HctPre は術前ヘマトクリット値、HctPost は術後 2 日目に測定されたヘマトクリット値、HctAve は HctPre と HctPost の平均値です。 - 側方 X 線撮影とコンピューター断層撮影 (CT) を使用して、椎間固定術を評価します 21。術前および術後 1 年間に磁気共鳴画像法 (MRI) を実行して、病変セグメントの傍脊髄筋の断面積 (CSA) をエミュレートします。ImageJ22 による脂肪浸潤の特性を計算します(図3)。
4. 統計解析
- 対応のあるサンプルの t 検定により、手術前後の VAS スコアと ODI スコアを比較します。手術前後の手術セグメントでMRI T2WIで測定した断面積を比較します。すべての統計分析はSPSSを使用して実行されました。データは平均±標準偏差として表され、p < 0.05は有意であると考えられました。
結果
シングルレベル手術(n = 50)の平均手術時間は102.3分(範囲75-160分)、マルチレベル手術(n = 46)で130.2分(範囲112-185分)であった。シングルレベル手順の平均術中失血は 62.5 mL (範囲 35-125 mL) であり、マルチレベル手順では 108.3 mL でした (表 2)。両側の傍脊髄筋の術前および術後の断面積 (CSA) および脂肪浸潤 (FI) レベルを 表 3 に示します。
術前では、減圧側のCSAは2088.4±226.7mm2、対側では2081.8±238.6mm2であり、有意差は見られませんでした。術後1年で、減圧側のCSAは2077.9±225.5mm2、反対側のCSAは2076.1±235.5mm2でした。減圧側の萎縮率は2.5%、反対側の萎縮率は1.2%で、統計学的に有意な差はなかった(p > 0.05)。
減圧側の脂肪浸潤率は術前が22.14%±9.21%、術後が22.09%±9.04%であった。反対側では、脂肪浸潤率は術前が21.78%±8.71%、術後が22.20%±9.19%でした。CSAの比較には、術前と術後の両方で同じ側、または減圧側と反対側の間で統計的に有意な差はありませんでした。傍脊髄筋の破壊に関する詳細なデータは、 表3 および 表4に示されています。
これらの結果は、MO-TLIFの術中出血が従来のオープンTLIFよりも低く、BE-TLIFと同等であることを示しています。手術時間はBE-TLIFよりも大幅に短く、従来のオープンTLIFと似ています。さらに、これまでに400件以上の手術を成功裏に完了したことから、MO-TLIFは筋肉の侵襲性を大幅に低下させ、対側に比べて減圧側の筋肉損傷がほとんど増加していないことを示しました。

図1:単一レベル病変に対するMO-TLIFの手順(A-B) 椎弓根の椎間腔と突起は、赤十字で示されているように、Cアーム透視法で決定されました。次に、2 つの椎間スペースの間の棘突起に沿った外科的切開をマークし、椎弓根の外側 1.5 cm に経皮的椎弓根スクリューの穿刺点をマークします。(C-I)減圧過程における術野の模式図(神経根は赤い実線で囲まれています)。(J) 単一レベルの病変に対する中央の 3 cm の切開。(K-M)経皮的スクリュー留置のプロセス。(N)治癒後の切開。この図の拡大版を表示するには、ここをクリックしてください。
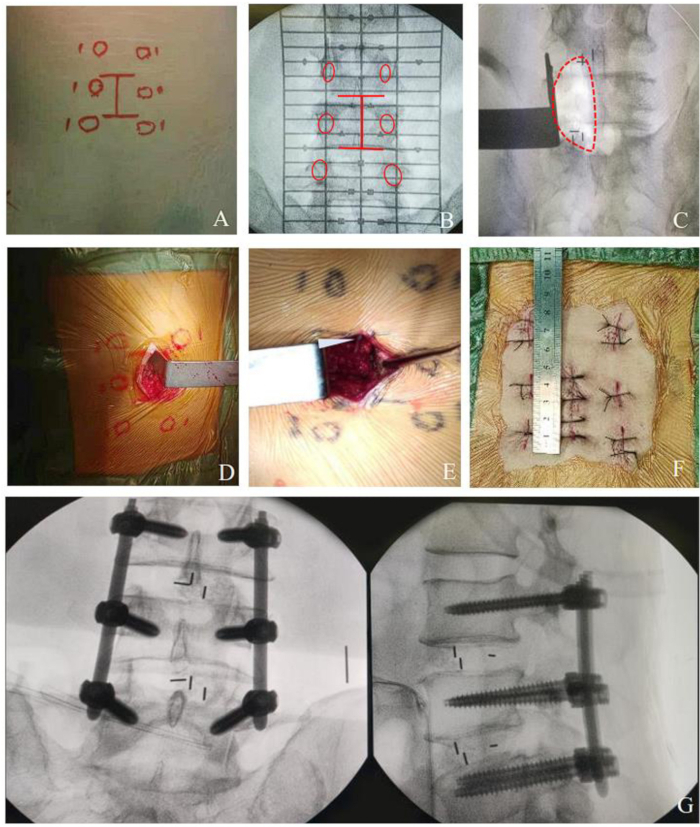
図2:マルチレベル病変に対するMO-TLIFの手順(A-B)皮膚上のマルチレベルマークライン。(C-E)マルチレベル減圧の手術野。(F) ツーセグメント手術でMO-TLIFの約4cmを切開した術後写真。(G) MO-TLIFが完成したときの写真で、ペディクルのネジとケージが所定の位置に位置している。この図の拡大版を表示するには、ここをクリックしてください。

図3:術前および術後の脂肪浸潤と傍脊髄筋の断面積 (A-B) 赤い線で囲まれた傍脊髄筋の術前および術後の断面積。(C-D)術前および術後の傍脊髄筋の脂肪浸潤、ImageJによる特性の計算は、黄色の線で囲まれていました。 この図の拡大版を表示するには、ここをクリックしてください。
| 特性 | 価値観 |
| 平均年齢(年) | 54.8 ± 17.5 |
| 性別 (M/F) | 47/49 |
| 診断 | |
| 腰椎すべり症 | 21 |
| 分節性不安定性を伴う腰椎椎間板ヘルニア | 45 |
| 分節性不安定性を伴う腰椎椎孔狭窄症 | 30 |
| BMIの | 23.9 ± 2.8 |
| オペレーションレベル | |
| シングルレベル | |
| L3-4 | 5 |
| L4-5 | 24 |
| L5-S1 | 21 |
| マルチレベル | |
| L3-5 | 18 |
| L4-S1 | 24 |
| L3-S1 | 4 |
| フォローアップ期間(月) | 13.2 ± 2.1 |
表1:患者の人口統計学的特性。
| メトリック | シングルレベル | マルチレベル |
| 術前ヘマトクリット値(%) | 41.6 ± 4.8 | 42.7 ± 7.1 |
| 術後ヘマトクリット値(%) | 38.5 ± 3.4 | 38.8 ± 6.8 |
| 術中失血(mL) | 62.5 ± 28.2 | 108.3 ± 31.2 |
| 推定総失血量(mL) | 213.9±124.8 | 282.8±155.9 |
| 動作時間(分) | 102.3 ± 17.2 | 130.2 ± 18.3 |
| 術後歩行時間(日) | 1.7 ± 0.4 | 2.0 ± 0.5 |
表2:周術期データ。
| 横 | CSA(ミリメートル2) | FI税率(%) |
| 術前 | ||
| 減圧側 | 2088年4月±226年7月 | 22.14 ± 9.21 |
| 対側 | 2081.8 ± 238.6 | 9月22日±9月04日 |
| 術後 | ||
| 減圧側 | 2077年9月±225年5月 | 21.78 ± 8.71 |
| 対側 | 2076年1月±235年5月 | 22.20 ± 9.19 |
表3:術前および術後の傍脊髄筋CSAと脂肪浸潤。
| 平均±SD(mm2) | p 値 | |
| 術前減圧側 - 術前対側 | 6.59±36.65 | 0.081 |
| 術前減圧側 - 術後減圧側 | 10.51±59.68 | 0.088 |
| 術前対側 - 術後対側 | 5.77±30.84 | 0.07 |
| 術後対側 - 術後減圧側 | 1.85±80.48 | 0.822 |
表4:効果的な傍脊髄筋の比較。 すべての統計分析は、対応のあるサンプルのt検定を使用して実行されました。
ディスカッション
過去10年間で、MIS-TLIF、PE-TLIF、およびBE-TLIFは、従来の開腹手術の代替手段となり、外傷、失血、および術後の回復の面で利点を提供しています23。一部の学者は、内視鏡補助腰椎固定術が最終的に開腹手術に取って代わると信じています。しかし、私たちの研究は、開腹TLIF手術が低侵襲技術の面でも大きな進歩を遂げたことを示しています。従来のオープンプロシージャのシンプルさと幅広い適用性を維持しながら、内視鏡的低侵襲技術と同様の臨床結果と低侵襲効果を達成しています。
術前に、椎弓根の突起、穿刺針の入口点、ターゲットセグメントの椎間スペース、および外科的切開をマークします。ただし、減圧する前に、透視法でセグメントを再度確認することをお勧めします。これは、解剖中の角度のわずかな変化でさえ、手術中に2つのそのようなケースに遭遇したため、セグメントエラーにつながる可能性があるためです。解剖後、超音波骨メスを使用して骨切り術を行い、脊柱管を露出させます。脊柱管を扱うときは、瘢痕の癒着を減らすために亜層靭帯を部分的に保持し、神経を圧迫する過度に厚い部分のみを取り除くことをお勧めします。対側中央管減圧が必要な場合は、手術床の角度を調整して棘突起根骨の一部を切除し、反対側で減圧を達成することができます。両側の横方向の陥凹減圧術には、両側の解剖が必要になる場合があります。減圧中は、安全上の理由から、既存のルートを完全に露出させる必要はありません。フックを使用して神経根の周囲をプローブすることができ、十分なスペースがあれば、広範な操作は必要ありません。減圧と固定が完了したら、中央の小さな切開部を閉じ、経皮的椎弓根スクリューを配置できるため、傍脊髄筋の収縮時間を短縮できます。ケージの選択に関しては、MO-TLIFは、従来のオープンTLIFと同じサイズのフュージョンケージを使用でき、小型または拡張可能なケージを必要とせず、ディスクの高さを回復し、ケージの沈下リスクを減らすのに役立ちます24。メタアナリシスは、ストレートケージがバナナ形状のケージよりも端板のより大きな面積を占めるため、圧力のより良い分布を作り出し、それが沈下率の低下に寄与する可能性があることを示唆した25。この研究では、追跡期間中にケージの沈下が見つかったのは1例だけでした。また、MO-TLIFは、対側へのオーバーザトップ減圧も実現できるため、両側減圧術(ULBD)のための片側椎弓切開術に適しています。これにより、脊柱管面積が効果的に増加しますが、椎間板の高さ、腰椎角度、および脊柱管領域の改善を測定するには、さらなる統計分析が必要です。
中央切開部のサイズが小さいため、内固定の交換が必要な再手術には適していません。ただし、このアプローチは他のほとんどのケースで引き続き適用できます。例えば、4つのセグメントを含む手術では、中央に小さな切開部を2つ使用し、各切開部で2つのセグメントの減圧を処理できます。
MO-TLIF技術は、直接視覚化して、またはルーペや顕微鏡などの視覚ツールの助けを借りて実行できます。この研究では、マルチレベルMO-TLIFを受けた患者は、平均手術時間が108.3分、平均失血が130.2mLという良好な結果を示しました。限られた骨膜下解離術と最小限の筋肉の収縮は、傍脊髄筋を保護する可能性があり、内視鏡支援腰椎固定術と同様の臨床結果と筋肉への影響をもたらします。
近い将来、内視鏡的または管状技術が開腹手術アプローチに完全に取って代わるわけではないかもしれません。MO-TLIFは、マルチレベル手術の利便性、手術時間の短縮、スムーズな学習曲線、特殊な器具の不要、水資源の保全など、開腹手術のユニークな利点を維持しながら、低侵襲の開腹手術を行うことができます。Zhang らの研究によると、PE-TLIF の手術時間は 202 ± 31.4 分で、失血は 73 ± 26.4 mL で、MIS-TLIF の術中失血 (192 ± 18.9 分、129 ± 31.7 mL) よりも大幅に短いことが示されています26。対照的に、Xueらによる研究では、PE-TLIFの手術時間(140.3±35.6分)はMIS-TLIF(170.±654.8分)よりも短く、PE-TLIF(65.6±15.3mL)の術中出血はMIS-TLIF(140.5±21.5mL)よりも少ないことがわかりました27。手術時間の違いは、外科医の習熟度に関連している可能性があります。メタアナリシスによると、PE-TLIF の平均手術時間は 155 分で、平均術中失血は 101.1 mL であるのに対し、MIS-TLIF の平均手術時間は 181.1 分、術中失血は 174 mL28,29 です。
シングルレベル MO-TLIF (64.5 ± 30.2 mL) の術中失血は、PE-TLIF と同等で、MIS-TLIF よりも優れており、操作時間が大幅に短縮されています (102.3 ± 17.2 分)。MO-TLIFは、3cmのシングルレベル切開部を近位または遠位に1cm延長することで、マルチレベル手術に有利です。このアプローチにより、切開部の延長を最小限に抑え、失血と手術時間をわずかに増加させるだけで減圧手術が可能になります。
結論として、低侵襲内視鏡技術には明確な利点がありますが、MO-TLIFのような低侵襲開術の継続的な進化は、脊椎手術における関連性と有効性を維持しながら、独自の利点を提供し続けています。
開示事項
著者には、開示すべき利益相反はありません。
謝辞
本研究は、2021年に中国国家自然科学基金会(プロジェクト番号:82474251)から、2024年に蘇州衛生委員会の科学技術プロジェクト(プロジェクト番号:LCZX202307)から資金提供を受けました。
資料
| Name | Company | Catalog Number | Comments |
| Absorbable sutures | Suzhou Jiahe | VT401L | |
| Blade | KYUAN | T00100 | |
| C-arm fluoroscopy | Siemens | Siremobile Compact L | |
| High frequency electrotome | Zhejiang Huatong | 20162010692 | |
| Iodophor | Likang High-tech | 31005102 | |
| Lumbar fusion cage | Shandong Weigao | GJXT310417 | |
| Premier posterior spine minimally invasive nail rod system | Shandong Weigao | GJXT310417 | |
| Suture | MERSILK | SA86G | |
| Ultrasonic bone knife | SMTP Technology | XD860A |
参考文献
- Souslian, F. G., Patel, P. D. Review and analysis of modern lumbar spinal fusion techniques. Brit J Neurosurg. 38, 61-67 (2024).
- Mobbs, R. J., Phan, K., Malham, G., Seex, K., Rao, P. J. Lumbar interbody fusion: Techniques, indications and comparison of interbody fusion options including plif, tlif, mi-tlif, olif/atp, llif and alif. J Spine Surg. 1 (1), 2-18 (2015).
- Foley, K. T., Gupta, S. K., Justis, J. R., Sherman, M. C. Percutaneous pedicle screw fixation of the lumbar spine. Neurosurg Focus. 10 (4), E10(2001).
- Zhao, J., Zhang, F., Chen, X., Yao, Y. Posterior interbody fusion using a diagonal cage with unilateral transpedicular screw fixation for lumbar stenosis. J Clin Neurosci. 18 (3), 324-328 (2011).
- Foley, K. T., Lefkowitz, M. A. Advances in minimally invasive spine surgery. Clin Neurosurg. 49, 499-517 (2002).
- Kambin, P. Arthroscopic microdiscectomy. Arthroscopy. 8 (3), 287-295 (1992).
- Osman, S. G. Endoscopic transforaminal decompression, interbody fusion, and percutaneous pedicle screw implantation of the lumbar spine: A case series report. Int J Spine Surg. 6, 157-166 (2012).
- Kim, J. E., Choi, D. J. Biportal endoscopic transforaminal lumbar interbody fusion with arthroscopy. Clin Orthop Surg. 10 (2), 248-252 (2018).
- Derman, P. B., Albert, T. J. Interbody fusion techniques in the surgical management of degenerative lumbar spondylolisthesis. Curr Rev Musculoskelet Med. 10 (4), 530-538 (2017).
- Meng, F. J., et al. Comparison research of mMO-TLIF via midline approach versus MIS-TLIF via Wiltse approach for thoracolumbar surgery. Orthop J China. 28, 118-122 (2020).
- Li, S. W., et al. Comparison of mMO-TLIF via midline incision versus MIS-TLIF via Wiltse approach in lumbar degenerative disease. Indian J Orthop. 58, 1278-1287 (2024).
- Anand, N., Hamilton, J. F., Perri, B., Miraliakbar, H., Goldstein, T. Cantilever tlif with structural allograft and rhbmp2 for correction and maintenance of segmental sagittal lordosis: Long-term clinical, radiographic, and functional outcome. Spine. 31 (20), E748-E753 (2006).
- Shafaq, N., et al. Asymmetric degeneration of paravertebral muscles in patients with degenerative lumbar scoliosis. Spine. 37 (16), 1398-1406 (2012).
- Laasonen, E. M. Atrophy of sacrospinal muscle groups in patients with chronic, diffusely radiating lumbar back pain. Neuroradiology. 26 (1), 9-13 (1984).
- Hira, K., et al. Relationship of sagittal spinal alignment with low back pain and physical performance in the general population. Sci Rep. 11 (1), 20604(2021).
- Hiyama, A., et al. The correlation analysis between sagittal alignment and cross-sectional area of paraspinal muscle in patients with lumbar spinal stenosis and degenerative spondylolisthesis. BMC Musculoskelet Disord. 20 (1), 352(2019).
- Singh, K., et al. A perioperative cost analysis comparing single-level minimally invasive and open transforaminal lumbar interbody fusion. Spine J. 14 (8), 1694-1701 (2014).
- Phan, K., Rao, P. J., Kam, A. C., Mobbs, R. J. Minimally invasive versus open transforaminal lumbar interbody fusion for treatment of degenerative lumbar disease: systematic review and meta-analysis. Eur Spine J. 24 (5), 1017-1030 (2015).
- Nadler, S. B., Hidalgo, J. H., Bloch, T. Prediction of blood volume in normal human adults. Surgery. 51 (2), 224-232 (1962).
- Gross, J. B. Estimating allowable blood loss: corrected for dilution. Anesthesiology. 58 (3), 277-280 (1983).
- Bridwell, K. H., Lenke, L. G., Mcenery, K. W., Baldus, C., Blanke, K. Anterior fresh frozen structural allografts in the thoracic and lumbar spine. Spine. 20 (12), 1410-1418 (1995).
- Jacob, K. C., et al. The effect of the severity of preoperative disability on patient-reported outcomes and patient satisfaction following minimally invasive transforaminal lumbar interbody fusion. World Neurosurg. 159, E334-E346 (2022).
- Ba, Z., et al. Percutaneous endoscopical transforaminal approach versus plf to treat the single-level adjacent segment disease after plf/plif: 1-2 years follow-up. Int J Surg. 42, 22-26 (2017).
- Zhang, H., et al. Percutaneous endoscopic transforaminal lumbar interbody fusion: Technique note and comparison of early outcomes with minimally invasive transforaminal lumbar interbody fusion for lumbar spondylolisthesis. Int J Gen Med. 14, 549-558 (2021).
- Amer, S., Gaby, K., Jean, T., Khalil, K., Mohammad, D. Transforaminal lumbar interbody fusion using banana-shaped and cages: meta-analysis of and outcomes. Eur Spine J. 32, 3158-3166 (2023).
- Xue, Y. D., Diao, W. B., Ma, C., Li, J. Lumbar degenerative disease treated by percutaneous endoscopic transforaminal lumbar interbody fusion or minimally invasive surgery-transforaminal lumbar interbody fusion: A case-matched comparative study. J Orthop Surg Res. 16 (1), 696(2021).
- Zhu, L., et al. Comparison of clinical outcomes and complications between percutaneous endoscopic and minimally invasive transforaminal lumbar interbody fusion for degenerative lumbar disease: A systematic review and meta-analysis. Pain Physician. 24 (6), 441-452 (2021).
- Song, Y. F., et al. Percutaneous endoscopic versus minimally invasive transforaminal lumbar interbody fusion for lumbar degenerative diseases: A meta-analysis. Wideochir Inne Tech Maloinwazyjne. 17 (4), 591-600 (2022).
- Aoki, Y., et al. Influence of pelvic incidence-lumbar lordosis mismatch on surgical outcomes of short-segment transforaminal lumbar interbody fusion. BMC Musculoskelet Disord. 16, 213(2015).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved