Method Article
Vordere zervikale Hybrid-Dekompressions- und Fusionschirurgie zur Behandlung der mehrstufigen zervikalen spondylotischen Myelopathie
In diesem Artikel
Zusammenfassung
In dieser Arbeit wird eine hybride Operationstechnik beschrieben, die eine anteriore zervikale Diskektomie und Fusion mit einer anterioren zervikalen Korpektomie und Fusion kombiniert, um Patienten mit mehrstufiger zervikaler spondylotischer Myelopathie zu behandeln.
Zusammenfassung
Die zervikale spondylotische Myelopathie (CSM) ist eine häufige Erkrankung, die aus einem Bandscheibenvorfall, einer Ossifikation des hinteren Längsbandes und anderen pathologischen Veränderungen resultiert, die eine Kompression des Rückenmarks verursachen. Die CSM schreitet schleichend fort mit leichtem Taubheitsgefühl der oberen Gliedmaßen, das die Patienten tendenziell ignorieren. Wenn sich der Zustand verschlimmert, kann es bei den Patienten zu einem Hinken, einer eingeschränkten Feinmotorik und schließlich zu einem Verlust der täglichen Aktivität kommen. Konservative Behandlungen wie Physiotherapie und Medikamente sind bei CSM häufig unwirksam. Sobald eine Operation als erforderlich erachtet wird, ist eine Dekompressionsoperation die beste Option. Bisher wurden sowohl die anteriore zervikale Diskektomie und Fusion (ACDF) als auch die anteriore zervikale Corpektomie und Fusion (ACCF) häufig zur Behandlung von CSM eingesetzt. Darüber hinaus wurde eine Art hybrides Verfahren, das ACDF mit ACCF kombiniert, zur Behandlung einiger CSM-Fälle eingesetzt und erzielte zufriedenstellende Ergebnisse. Daher zielt diese Studie darauf ab, diese hybride Operationstechnik vorzustellen und sie auf der Grundlage ihres Patientenerfolgs zu befürworten.
Einleitung
Die zervikale spondylotische Myelopathie (CSM) ist eine häufige Ursache für eine Funktionsstörung des zervikalen Nerven. Sie ist gekennzeichnet durch eine erworbene Stenose des zervikalen Spinalkanals, eine osteoarthritische Degeneration oder Bandaberrationen der Spinalwirbelsäule1. Aufgrund der pathologischen Merkmale der Krankheit sind konservative Behandlungen bei der Beseitigung der zunehmenden Kompression unwirksam, und ein sofortiger chirurgischer Eingriff ist erforderlich. In der klinischen Praxis ist die anteriore zervikale Diskektomie und Fusion (ACDF) in der Regel die erste Option für die einstufige CSM2. Trotz der Vielzahl der verfügbaren Verfahren bleibt das beste Verfahren für die mehrstufige zervikale spondylotische Myelopathie (MCSM) umstritten.
Bei MCSM kommt die typische Kompression des Rückenmarks von der ventralen Seite, und diese Kompression verursacht Symptome einer zentralen und peripheren Nervenverletzung. Gebärmutterhalsoperationen sind in der Regel erforderlich, um MCSM zu behandeln. Es gibt zwei gängige chirurgische Ansätze: anteriore und hintere Operationen. Der anteriore Zugang umfasst die ACDF, die anteriore zervikale Korpektomie und Fusion (ACCF) und die anteriore zervikale Hybrid-Dekompressions- und Fusionschirurgie (ACHDF, die Kombination aus ACDF und ACCF). Diese anterioren Operationen eignen sich für MCSM mit ventraler Kompression des Rückenmarks. Zu den Vorteilen von ACHDF als hybride Operationstechnik gehören die Beibehaltung der vorderen und mittleren Säulen der Halswirbelsäule bei gleichzeitiger Gewährleistung eines möglichst hohen Dekompressionsaufwands und die Möglichkeit, dass die Chirurgen ihre Operationsstrategie individuell anpassen können. In dieser Studie wollen wir die ACHDF-Technik vorstellen, die ACDF und ACCF zur Behandlung von MCSM kombiniert.
Präsentation des Falles
Eine 50-jährige Patientin, die seit 1,5 Jahren über Nackenschmerzen und seit 7 Monaten über Taubheitsgefühle in den linken Gliedmaßen klagte, wurde in die Abteilung für Wirbelsäulenchirurgie des Dritten Krankenhauses der Medizinischen Universität Hebei eingeliefert. Es wurde die Zustimmung der Patientin eingeholt, ihre Krankengeschichte in dieser Studie zu verwenden. Die Hauptsymptome dieses Patienten wurden durch tägliche Aktivitäten verschlimmert und durch Ruhe gelindert und standen in keinem Zusammenhang mit Temperaturschwankungen. Die Patientin hatte sich in einer örtlichen Klinik konservativen Behandlungen unterzogen, darunter eine Transfusionstherapie und Akupunktur, jedoch ohne erfolgreiche Linderung ihrer Beschwerden. Die körperliche Untersuchung ergab eine verminderte Kraft des linken Bizeps und Trizeps (Grad 3) und der Muskelgruppen der linken unteren Extremität (Grad 4) sowie verminderte Bizeps- und Trizepssehnenreflexe. Das Hoffmann-Zeichen und das Babinski-Zeichen waren beide negativ.
Diagnose, Beurteilung und Planung
Die Patientin wurde zur Vorbereitung auf die Operation zervikalen Röntgenaufnahmen, CT-Scans, MRTs und Labortests unterzogen. Die radiologischen Untersuchungen ergaben eine Begradigung der physiologischen Krümmung der Halswirbelsäule, Bandscheibenvorfälle und eine Rückenmarkskompression. Die visuelle Analogskala (VAS) der Patientin betrug 5 und ihr zervikaler Japanese Orthopaedic Association Score (JOA) 7. Die zervikale spondylotische Myelopathie wurde anhand der Symptome einer verminderten Muskelkraft, verminderter Sehnenreflexe und Taubheitsgefühl der Gliedmaßen diagnostiziert. Da der Patient keine Anzeichen einer peripheren Nervenkompression zeigte, wurde eine zervikale spondylotische Radikulopathie ausgeschlossen. Darüber hinaus wurden Schmerzen durch Muskelzerrungen und rheumatische Erkrankungen ausgeschlossen, da es keinen offensichtlichen Zusammenhang zwischen den Schmerzsymptomen und Temperaturveränderungen bei der Patientin gab 3,4.
Da die konservative Behandlung unwirksam war, wurde dem Patienten eine chirurgische Behandlung empfohlen. Zur Behandlung der Erkrankung wurde eine ACHDF-Operation gewählt, da im Röntgenbild und CT des Patienten im Segment C6/7 ein Osteophyt zu beobachten war (Abbildung 1A, B, gelber Pfeil). Währenddessen konnte in der MRT in C6/7 ein schwacher Signalschatten beobachtet werden, der posterior hervorstand und auf den Duralsack drückte (Abbildung 1C, gelber Pfeil). Die sagittale CT-Bildgebung zeigte Osteophyten, die um ~5,7 mm aus dem hinteren Rand des Wirbelkörpers herausragten und das Rückenmark nicht nur auf Bandscheibenhöhe, sondern auch hinter dem Halswirbelkörper in C6 und C7 zusammendrückten. Bei C5/6 konnte ein Bandscheibenvorfall beobachtet werden, während C4/5 einen relativ leichten Bandscheibenvorfall erlitt. In Übereinstimmung mit den Empfehlungen des Wirbelsäulenkomitees5 der WFNS wurden zur Behandlung der Erkrankung eine C6-Korpektomie und eine C4/5-Diskektomie durchgeführt. Die Nackenschmerzen und das Taubheitsgefühl der Patientin verbesserten sich nach der Operation, und obwohl die körperliche Untersuchung keine signifikante Wiederherstellung der Muskelkraft zeigte, berichtete die Patientin über eine Verbesserung ihrer eigenen Wahrnehmung ihrer Muskelkraft. Es wurden keine größeren postoperativen Komplikationen beobachtet.
Protokoll
Das Protokoll wurde genehmigt und folgte den Richtlinien der Ethikkommission des Dritten Krankenhauses der Medizinischen Universität Hebei. Die Einverständniserklärung der Patienten wurde eingeholt, um sie und die im Rahmen dieser Studie generierten Daten einzubeziehen.
1. Präoperative Vorbereitung
- Wenden Sie die folgenden Einschlusskriterien an.
- Stellen Sie sicher, dass die radiologische Untersuchung drei oder mehr Krankheitsstufen anzeigt.
- Stellen Sie sicher, dass die Symptome durch krankhafte Veränderungen der Halswirbel unter Ausschluss anderer systemischer Erkrankungen verursacht werden.
- Achten Sie auf Hypertonie, Hyperreflexie, positive pathologische Anzeichen oder Symptome einer Verletzung der oberen Motoneuronen.
- Wenden Sie die folgenden Ausschlusskriterien an.
- Ausschließen Sie diejenigen, bei denen eine zervikale spondylotische Radikulopathie diagnostiziert wurde.
- Schließen Sie Patientinnen aus, die sich einer Gebärmutterhalsoperation unterzogen haben oder in der Vergangenheit Gebärmutterhalsverletzungen erlitten haben.
- Schließen Sie Patientinnen mit einem Gebärmutterhalstumor oder einer Entzündung aus.
- Patienten mit schwerer Ossifikation des hinteren Längsbandes ausschließen.
- Nach der Vollnarkose und der trachealen Intubation legen Sie den Patienten in Rückenlage auf den Operationstisch.
- Legen Sie ein zylindrisches Kissen auf den Nacken des Patienten, um die Halswirbelsäule in einer Hyperextensionsposition zu halten.
- Desinfizieren Sie den Operationsbereich mit Jod und Alkohol und legen Sie dann die sterilen Tücher über den Patienten.
2. Exposition der Läsionen
- Machen Sie einen rechten Quer- oder Längsschnitt (je nach Präferenz des Chirurgen), der auf den Fusionssegmenten zentriert ist (Lokalisation gemäß den Markern der Körperoberfläche).
- Verwenden Sie ein Skalpell, um die Haut zu schneiden, und verwenden Sie ein Elektrokoagulationselektrotom, um das Unterhautgewebe zu isolieren und die Platysma myoides zu durchtrennen (schneiden Sie den Omohyoid-Muskel, wenn der Operationsumfang groß ist und der Muskel nicht genäht werden muss).
- Bestimmen Sie mit dem Finger den Karotispuls und die Position der Halsschlagaderscheide. Führen Sie eine stumpfe Dissektion des Muskels medial zur Halsschlagaderscheide bis zur prävertebralen Faszie durch.
- Verwenden Sie einen Periostablöser, um den Muskel entlang der Ansatzpunkte zu trennen. Verwenden Sie einen Kropfretraktor, um die Schilddrüsen- und Tracheoösophagusstrukturen auf die linke Seite des Patienten zu ziehen.
- Verwenden Sie ein Elektrokoagulationselektrotom, um die prävertebrale Faszie zu durchtrennen und den Wirbelkörper freizulegen. Verwenden Sie dann einen Gebärmutterhalsspreizer, um den Zwischenwirbelraum zu erweitern.
3. Dekompression
- ACDF-Chirurgie
- Schneiden Sie mit einem Skalpell die erforderliche Menge des Anulus fibrosus ab. Verwenden Sie dann eine Kürette und eine Nucleus pulposus-Klemme, um den Nucleus pulposus zu entfernen, bis die Dura freiliegt. Verwenden Sie ein Laminektomie-Rongeur, um die Endplatten und den hyperplastischen Knochen zu entfernen.
- Verwenden Sie einen Nervendissektor, um nach einer möglichen Kompression zu suchen, und verwenden Sie ihn, um einen Teil des hinteren Wirbelkörperrandes zu entfernen, um eine Dekompression durchzuführen.
- Setzen Sie einen mit autologem Knochen gefüllten interkorporellen Fusionskäfig in der richtigen Größe in den Zwischenwirbelraum ein.
- ACCF-Chirurgie
- Verwenden Sie eine Rongeurzange, um den Wirbelkörper zu entfernen, der sich zwischen zwei erkrankten Bandscheiben befindet. Verwenden Sie eine Kürette und eine Nucleus pulposus-Klemme, um die beiden angepassten Scheiben und Endplatten zu entfernen, ähnlich wie in Schritt 3.1.1.
- Nachdem die Dura freigelegt wurde, verwenden Sie den Nervendissektor, um nach einer möglichen Kompression zu suchen. Verwenden Sie Gelatineschwämme oder flüssige Gelatine, begleitet von Gehirnwattestücken, um die Blutung zu stoppen.
- Setzen Sie einen mit autologem Knochen gefüllten Titan-Netzkäfig in der richtigen Größe in den Raum zwischen den beiden Wirbeln ein.
4. Fixierung der Titanplatte
- Wählen Sie eine Titanplatte mit einer geeigneten Länge, um das chirurgische Segment abzudecken. Implantieren Sie sechs Schrauben in die Wirbel, um die Titanplatte zu fixieren.
5. Den Schnitt schließen
- Verwenden Sie Kochsalzlösung, um den Operationsbereich zu spülen und mit bipolarer Elektrokoagulation eine Blutstillung auszulösen. Füllen Sie den Hohlraum mit Gelatineschwämmen und führen Sie einen Drainageschlauch ein.
- Verwenden Sie eine unterbrochene Naht, um die oberflächliche Faszie und die Haut zu schließen (Nahtmaterial der Größe 2-0).
HINWEIS: Die Nahtmethode kann je nach Vorliebe des Bedieners oder auf Wunsch des Patienten gewählt werden.
6. Nachsorge
- Messen Sie jeden Tag den Blutverlust durch die Drainageflasche. Wenn der tägliche Blutverlust weniger als 50 ml beträgt, kann der Drainageschlauch entfernt werden.
- Lassen Sie den Patienten am Tag nach der Operation mit einer getrennten Kragenstütze gehen. Raten Sie dem Patienten, die Bandage 1,5 Monate lang zu tragen.
Ergebnisse
Die CT- und MRT-Untersuchungen zeigten einen Bandscheibenvorfall in den zervikalen Segmenten C3-C7 und eine Ossifikation in C6-C7 (Abbildung 1). Obwohl C3-C4 pathologische Veränderungen aufwies, wurde keine Rückenmarkskompression beobachtet. Daher wurde C4-C7 als chirurgisches Segment gewählt. Der postoperative VAS-Score sank von 5 vor der Operation auf 3 nach 3 Monaten und 1 nach 20 Monaten. Der JAA-Score stieg von 7 vor der Operation auf 8 nach 3 Monaten und 12 nach 20 Monaten. Die Nackenschmerzen traten nur auf, wenn der Patient den Kopf längere Zeit gebeugt hatte; Die Taubheit und der Verlust der Muskelkraft in den Gliedmaßen waren immer noch vorhanden, waren aber im Vergleich zu den Werten vor der Operation in der letzten Nachuntersuchung besser. Eine postoperative Röntgenaufnahme ergab keine signifikanten implantatbedingten Komplikationen (Abbildung 1)6.
In einer früheren Studie haben wir die klinischen Ergebnisse zwischen Multilevel-ACDF und ACHDFverglichen 6. Die Ergebnisse zeigten, dass die ACHDF in Bezug auf das intraoperative Trauma, das anhand des Krankenhausaufenthalts, der Operationszeit und des intraoperativen Blutverlusts beurteilt wurde, mit der ACDF-Operation vergleichbar war, sowie in Bezug auf bildgebende Parameter, einschließlich des Cobb-Winkels und der Höhe der vorderen Säule. Mit Ausnahme der langfristigen Aufrechterhaltung der Höhe der vorderen Säule auf Fusionsebene hatte die mehrstufige ACDF-Operation im Vergleich zur ACHDF-Operation bessere Ergebnisse in Bezug auf die stabile Höhe der vorderen Wirbelsäule, obwohl dieser Unterschied die VAS- oder JAA-Werte der Patienten nicht beeinflusste (Tabelle 1 und Tabelle 2)6.
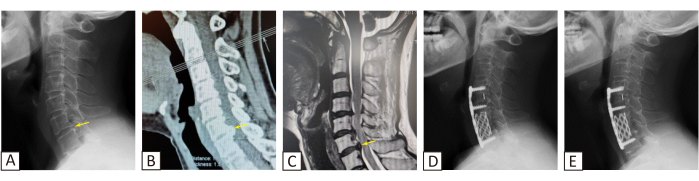
Abbildung 1: Prä- und postoperative Bildgebung. Die (A) präoperativen Röntgen-, (B) CT- und (C) MRT- und postoperativen Röntgenbilder des Patienten nach (D) 3 Monaten und (E) 20 Monaten. Diese Abbildung wurde von Tian et al.6 modifiziert. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
| ACDF (n=43) | ACHDF (n=23) | Z-Wert | P-Wert | |
| Krankenhausaufenthalt (Tage) | 12.11 (± 4.02) | 13.65 (± 3.27) | - | 0.121 |
| Betriebszeit (min) | 133,63 (± 34,22) | 136,09 (± 41,40) | - | 0.797 |
| Blutverlust (ml) | 200 (IQR=200) | 200 (IQR=200) | -0.314 | 0.754 |
| VAS (vor der Inbetriebnahme) | 2 (IQR=4) | 3 (IQR=3) | -0.979 | 0.328 |
| LZ (letzte Nachuntersuchung) | 1 (IQR=2)* | 1 (IQR=2)* | -0.17 | 0.865 |
| JOA (vor der Operation) | 8 (IQR=2) | 8 (IQR=2) | -0.868 | 0.385 |
| JOA (letzte Nachuntersuchung) | 14 (IQR=1)* | 13 (IQR=2)* | -1.749 | 0.08 |
| Verbesserungsrate (%) | 62,50 (IQR=14,44) | 50,00 (IQR=25,56) | -1.619 | 0.105 |
Tabelle 1: Der Vergleich der Dauer des Krankenhausaufenthalts (Tage), der Operationszeit (min), des Blutverlusts (ml), des VAS-Scores, des JAA-Scores und der Verbesserungsrate (%) der beiden Gruppen mit ACDF und ACHDF. Diese Tabelle wurde von Tian et al.6 modifiziert. * Signifikanter Unterschied zwischen der Voroperation und der letzten Nachuntersuchung in derselben Gruppe. Abkürzungen: ACDF = anteriore zervikale Diskektomie und Fusionschirurgie; ACHDF = anteriore zervikale hybride Dekompressions- und Fusionschirurgie (die Kombination von ACDF und ACCF); VAS = visuelle Analogskala; JOA = Japanische Orthopädische Vereinigung; IQR = Interquartilsbereiche.
| ACDF (n=43) | ACHDF (n=23) | P-Wert | |
| Cobb (vor der Operation) | 8,67 ± 9,54 | 10.09 ± 10.86 Uhr | 0.587 |
| Cobb (3 Monate) | 12.53 ± 5.95∫ | 12,87 ± 6,92∫ | 0.838 |
| Cobb (letzte Nachuntersuchung) | 11,58 ± 5,89*∫∫ | 11.48 ± 6.73∫∫ | 0.949 |
| Höhe (vor dem Betrieb) | 76,96 ± 9,72 | 73.10 ± 8.62 | 0.116 |
| Höhe (3 Monate) | 80,89 ± 9,26∫ | 76.56 ± 7.30 Uhr∫ | 0.057 |
| Höhe (letzte Nachverfolgung) | 79,85 ± 9,20*∫∫ | 75,27 ± 7,41*∫∫ | 0.044 |
Tabelle 2: Vergleich des Cobb-Winkels (Grad) und der Höhe der vorderen Säule (mm) der beiden Gruppen mit ACDF und ACHDF. Diese Tabelle wurde von Tian et al. geändert6 * Signifikanter Unterschied zwischen der Voroperation und der letzten Nachuntersuchung in derselben Gruppe; ∫ signifikanter Unterschied zwischen der Voroperation und der 3-monatigen Nachbeobachtung in derselben Gruppe; ∫∫ signifikanter Unterschied zwischen der 3-monatigen Nachbeobachtung und der letzten Nachbeobachtung in derselben Gruppe. Abkürzungen: ACDF = anteriore zervikale Diskektomie und Fusionschirurgie; ACHDF = anteriore zervikale hybride Dekompressions- und Fusionschirurgie (die Kombination von ACDF und ACCF).
Diskussion
Die mehrstufige zervikale spondylotische Myelopathie ist eine Krankheit, die mehrere Bandscheiben betrifft. Dies erhöht den Schweregrad der Erkrankung, erschwert die Erlangung einer guten Prognose und erschwert die Bestimmung des verantwortlichen Segments als bei einer einstufigen CSM. Klinisch wird der mJAA-Score häufig zur Bewertung von CSM verwendet. Ein mJAA-Score ≤ 11 wird im Allgemeinen als schwerwiegend angesehen, 12-14 ist moderat und 15-17 ist mild; Mittelschwere und schwere CSM erfordern eine sofortige chirurgische Behandlung, während Patienten, die als leicht eingestuft wurden, eine nicht-operative Behandlung in Anspruch nehmenkönnen 1. Ärzte sollten auch über den Zusammenhang zwischen Bildgebung und Anzeichen und Symptomen nachdenken. Wenn in der Bildgebung nur eine Rückenmarkskompression beobachtet wird, aber keine Symptome vorliegen, sollte ein chirurgischer Eingriff mit Vorsicht durchgeführt werden. Die gebräuchlichsten anterioren Ansätze für MSCM sind ACDF, ACCF und ACHDF.
Die mehrstufige ACDF wird bevorzugt, wenn die Patienten eine minimale retrovertebrale Erkrankung haben; Wenn jedoch eine signifikante retrovertebrale Erkrankung beobachtet wird, werden ACCF und ACHDF empfohlen7. Obwohl ACCF das chirurgische Sehvermögen verbessern und eine vollständigere Dekompression ermöglichen kann, haben Studien gezeigt, dass die mehrstufige ACCF aufgrund der umfangreichen Schädigung der Halswirbelsäulenstruktur keinen Vorteil bei der Behandlung von MCSM 8,9,10 hat. Die beiden anderen Techniken zeigen eine ähnliche Wirksamkeit8. ACHDF ist eine Technik, die ACDF und ACCF kombiniert. ACDF wird zur Behandlung kleinerer Läsionen eingesetzt, die nur die Bandscheibe betreffen, während ACCF zur Behandlung von Läsionen eingesetzt wird, die den hinteren Rand des Wirbelkörpers betreffen, was zu einer ausgedehnteren Dekompression führt. Der Vorteil der ACHDF ist die Kombination aus einem leichten Trauma aus der ACDF und einer vollständigen Dekompression aus der ACCF, die eine patientenspezifische Behandlung ermöglicht.
Einer früheren Studie zufolge sind eine schlechte lokale Kyphosekorrektur, fortgeschrittenes Alter, eine längere Dauer der Symptome und ein größerer T1-Steigungswinkel mit einer schlechten Prognose verbunden11. Wenn die dorsale Kompression des Rückenmarks ausgeprägt ist oder eine generalisierte Spinalkanalstenose bei MCSM vorliegt, wie z. B. eine Ossifikation des hinteren Längsbandes, ist eine Dekompression von der ventralen Seite riskant. Dies kann zu Komplikationen wie iatrogenen Nervenschäden und Liquoraustritt führen. In diesen Fällen sind die Laminoplastik und die Laminotomie12 - die beiden prominenten Operationen am hinteren Zugang, die den Bogensehneneffekt nutzen, um den Spinalkanal zu erweitern - die sicherere Wahl. Neurologische, Gefäß- oder Speiseröhrenverletzungen können auftreten, wenn die Chirurgen die chirurgische Anatomie nicht gründlich kennen, und implantatbedingte Komplikationen wie Implantatverschiebungen und Fusionsversagen können auch aufgrund einer ungeeigneten Auswahl der Implantate auftreten. Daher sollten sich Chirurgen der mechanischen Eigenschaften der Implantate bewusst sein und Titanplatten und -schrauben in geeigneter Größe wählen, um Komplikationen zu vermeiden5.
Die Schritte zur Entfernung der Bandscheibe bei dieser Operation müssen mit Vorsicht durchgeführt werden. Bei der Annäherung an das hintere Längsband müssen zusätzliche Vorsichtsmaßnahmen getroffen werden, um eine Verletzung der Dura zu vermeiden. Bei der Entfernung des hinteren Längsbandes kann es zu einer Kapillarblutung kommen, und die Verwendung einer bipolaren Gerinnungszange sollte aufgrund des Risikos einer Nervenschädigung vermieden werden. Die Kompression mit Gelatineschwämmen und Gehirnwattestücken ist eine gute Möglichkeit, den Verlust von Liquor cerebrospinalis zu stoppen oder zu behandeln. Ein weiterer kritischer Faktor ist die Fokussierung auf die Wiederherstellung der zervikalen Krümmung, die ein wichtiger Indikator für die postoperative Wirksamkeit ist13,14. Eine leichte Konvexität der Halswirbelsäule polstert das Rückenmark ab und ist auch ein Schutzfaktor gegen axiale Symptome15. Es ist wichtig, die präoperative Position, das Ausmaß der Distraktion des Zwischenwirbelraums und die Auswahl eines interkorporalen Fusionskäfigs und eines Titankäfigs in geeigneter Größe zu berücksichtigen. Bei der Formulierung dieser Strategien sollten Chirurgen auch berücksichtigen, dass manche Menschen physiologisch gerade Stacheln oder kyphotische Stacheln16,17 haben, abhängig von Geschlecht, Alter, Region und anderen Faktoren.
Der Hybridbetrieb weist im Vergleich zu ACDF einige Einschränkungen auf. ACDF hat bessere Langzeitergebnisse in Bezug auf die Wiederherstellung der Höhe der vorderen Wirbelsäule6. Aufgrund der Unterschiede in Spannweite und Härte zwischen dem Titankäfig und dem interkorporellen Fusionskäfig wird der spongiöse Knochen bei der ACCF stärker unter Druck gesetzt als bei der ACDF. Eine Vergleichsstudie untersuchte die Unterschiede zwischen der interkorporalen Fusion von Titan und Polyetheretherketon (PEEK) und entdeckte, dass Titan- und PEEK-Käfige ähnliche Fusionsraten aufwiesen, Titan jedoch eine höhere Setzungsrate aufwies18. Eine Finite-Elemente-Studie verglich die biomechanischen Eigenschaften von ACDF, ACCF und ACHDF bei MCSM und stellte fest, dass die ACCF-Gruppe die höchste Belastung für die Bandscheibe aufwies. Im Gegensatz dazu wies ACDF ohne Titanplattenfixierung die geringste Belastungauf 19. Um dieses Problem auszuräumen, haben sich die Forscher darauf konzentriert, das Material und die Form des Titankäfigs 20,21,22,23 anzupassen, mit positiven Ergebnissen. Aufgrund der Empfindlichkeit des Rückenmarks sind nicht alle Patienten Kandidaten für einen anterioren Zugang.
Posteriore Zugänge wie Laminoplastik und Labotomie können das Spinalkanalvolumen vor allem durch indirekte Dekompression vergrößern und dazu beitragen, Rückenmarksverletzungen durch die Entfernung von Läsionen zu vermeiden, um ähnliche Prognosen zu erreichen24. Daher können bei Patienten mit hinteren Längsbändern mit posterioren Zugängen bessere Ergebnisse erzielt werden25. Die meisten Patienten können mit dem anterioren oder posterioren Zugang allein gute Ergebnisse erzielen, aber einige Patienten können Restsymptome haben, die auf eine unvollständige intraoperative Dekompression zurückzuführen sein können. Daher kann bei Patienten mit komplexer MCSM ein kombinierter anteriorer und posteriorer Zugang zu einer weitgehenden Dekompression führen und die Unzulänglichkeit der alleinigen Verwendung des anterioren oder posterioren Zugangs kompensieren. Kombinierte anteriore und posteriore Zugänge sollten in Betracht gezogen werden, wenn die zervikale Spondylose des Rückenmarks mit einer schweren oder fixierten Kyphose oder mit schwerer Osteoporose kombiniert ist oder wenn die Stabilität durch eine multisegmentale Beteiligung beeinträchtigt wird26. Bei Patienten mit schwerer zervikaler Ossifikation des hinteren Längsbandes bieten die anterior kontrollierbare Antedisplacement- und Fusionschirurgie im Vergleich zur Laminoplastik einzigartige Vorteile27 . Diese Studie demonstriert eine hybride Operationstechnik, die ACDF und ACCF zur Behandlung von MCSM kombiniert. Diese Hybridtechnik besitzt die Vorteile sowohl des ACDF- als auch des ACCF-Verfahrens und kann daher effektiv zur Behandlung von MCSM eingesetzt werden und zufriedenstellende Ergebnisse erzielen.
Offenlegungen
Die Autoren haben keine Interessenkonflikte offenzulegen.
Danksagungen
Nichts.
Materialien
| Name | Company | Catalog Number | Comments |
| Adhesive | Biatain | 3420 | 12.5 x 12.5 cm |
| Bipolar electrocoagulation tweezers | Juan'en Medical Devices Co.Ltd | BZN-Q-B-S | 1.2 x 190 mm |
| Bone wax | ETHICON | W810T | 2.5 g |
| High frequency active electrodes | ZhongBangTianCheng | GD-BZ | GD-BZ-J1 |
| interbody fusion cage | WEGO | 900200013 | 5 x 16 x 13 mm |
| Laminectomy rongeur | Qingniu | 2051.03 | 220 x 1.5 x 130° |
| Laminectomy rongeur | Qingniu | 2054.03 | 220 x 3.0 x 130° |
| Pituitary rongeur | Qingniu | 2028.01 | 220 x 3.0 mm |
| Pituitary rongeur | Qingniu | 2028.02 | 220 x 3.0 mm |
| self-tapping screw | WEGO | 700054012 | 4.0 x 12 mm |
| spreader | WEGO | 818-021 | - |
| Surgical drainage catheter set | BAINUS MEDICAL | SY-Fr16-C | 100-400 mL |
| Surgical film | 3L | SP4530 | 45 x 30 cm |
| titanium plate | WEGO | 700000057 | 57.5 mm |
| Titanium cage | WEGO | 9051028 | 10 x 28 mm |
Referenzen
- Badhiwala, J. H., et al. Degenerative cervical myelopathy - Update and future directions. Nature Reviews Neurology. 16 (2), 108-124 (2020).
- Carrier, C. S., Bono, C. M., Lebl, D. R. Evidence-based analysis of adjacent segment degeneration and disease after ACDF: A systematic review. Spine Journal. 13 (10), 1370-1378 (2013).
- Farbu, E. H., et al. Working in a cold environment, feeling cold at work and chronic pain: A cross-sectional analysis of the Tromso Study. BMJ Open. 9 (11), e031248 (2019).
- Azzouzi, H., Ichchou, L. Seasonal and weather effects on rheumatoid arthritis: Myth or reality. Pain Research and Management. 2020, 5763080 (2020).
- Deora, H., et al. Anterior surgical techniques for cervical spondylotic myelopathy: WFNS Spine Committee recommendations. Neurospine. 16 (3), 408-420 (2019).
- Tian, X., et al. Treatment of three-level cervical spondylotic myelopathy using ACDF or a combination of ACDF and ACCF. Frontiers in Surgery. 9, 1021643 (2022).
- Wilson, J. R., et al. State of the art in degenerative cervical myelopathy: An update on current clinical evidence. Neurosurgery. 80, S33-S45 (2017).
- Badhiwala, J. H., et al. A comparison of the perioperative outcomes of anterior surgical techniques for the treatment of multilevel degenerative cervical myelopathy. Journal of Neurosurgery. Spine. , (2020).
- Katz, A. D., Mancini, N., Karukonda, T., Cote, M., Moss, I. L. Comparative and predictor analysis of 30-day readmission, reoperation, and morbidity in patients undergoing multilevel ACDF versus single and multilevel ACCF using the ACS-NSQIP dataset. Spine. 44 (23), E1379-E1387 (2019).
- Wang, T., et al. Anterior cervical discectomy and fusion versus anterior cervical corpectomy and fusion in multilevel cervical spondylotic myelopathy: A meta-analysis. Medicine. 95 (49), e5437 (2016).
- Cheng, X. J., Jin, L., Wang, X., Zhang, W., Shen, Y. Predictors of poor outcome in cervical spondylotic myelopathy patients underwent anterior hybrid approach: Focusing on change of local kyphosis. Journal of Orthopaedic Surgery and Research. 15 (1), 369 (2020).
- Huang, M., Gao, X., Cheng, J., Han, J., Liu, J. Laminoplasty versus laminectomy and fusion for multilevel cervical compressive myelopathy: A meta-analysis. Medicine. 95 (23), e03588 (2016).
- Xia, C., Shi, F., Chen, C., Lv, J., Chen, Q. Clinical efficacy and safety of anterior cervical decompression versus segmental fusion and posterior expansive canal plasty in the treatment of multilevel cervical spondylotic myelopathy. Journal of Healthcare Engineering. 2022, 7696209 (2022).
- Goto, S., Kita, T. Long-term follow-up evaluation of surgery for ossification of the posterior longitudinal ligament. Spine. 20 (20), 2247-2256 (1995).
- Wang, L. F., Dong, Z., Miao, D. C., Shen, Y., Wang, F. Risk factor analysis of axial symptoms after single-segment anterior cervical discectomy and fusion: A retrospective study of 113 patients. Journal of International Medical Research. 47 (12), 6100-6108 (2019).
- Been, E., Shefi, S., Soudack, M. Cervical lordosis: The effect of age and gender. Spine Journal. 17 (6), 880-888 (2017).
- Yu, M., et al. Analysis of cervical and global spine alignment under Roussouly sagittal classification in Chinese cervical spondylotic patients and asymptomatic subjects. European Spine Journal. 24 (6), 1265-1273 (2015).
- Seaman, S., Kerezoudis, P., Bydon, M., Torner, J. C., Hitchon, P. W. Titanium vs. polyetheretherketone (PEEK) interbody fusion: Meta-analysis and review of the literature. Journal of Clinical Neuroscience. 44, 23-29 (2017).
- Li, Z., Liu, H., Yang, M., Zhang, W. A biomechanical analysis of four anterior cervical techniques to treating multilevel cervical spondylotic myelopathy: A finite element study. BMC Musculoskeletal Disorders. 22 (1), 278 (2021).
- vanden Brink, W., Lamerigts, N. Complete osseointegration of a retrieved 3-D printed porous titanium cervical cage. Frontiers in Surgery. 7, 526020 (2020).
- Wang, Y., et al. A novel anatomic titanium mesh cage for reducing the subsidence rate after anterior cervical corpectomy: A finite element study. Scientific Reports. 11 (1), 15399 (2021).
- Zhang, T., Guo, Y., Zhang, D., Zhao, R., Hu, N. Titanium cage in comparison with nano-hydroxyapatite bone graft substitutes in cervical reconstruction. Journal of Biomedical Nanotechnology. 17 (7), 1448-1452 (2021).
- Lu, T., et al. Construction of a new cervical anatomically adaptive titanium mesh cage based on measurements of cervical geometry: A morphological and cadaveric study. Experimental and Therapeutic Medicine. 22 (5), 1256 (2021).
- Hitchon, P. W., et al. Anterior and posterior approaches for cervical myelopathy: Clinical and radiographic outcomes. Spine. 44 (9), 615-623 (2019).
- Sun, Y., Li, L., Zhao, J., Gu, R. Comparison between anterior approaches and posterior approaches for the treatment of multilevel cervical spondylotic myelopathy: A meta-analysis. Clinical Neurology and Neurosurgery. 134, 28-36 (2015).
- Cervical Spondylotic Myelopathy: Surgical Treatment Options. Orthoinfo Available from: https://orthoinfo.aaos.org/en/treatment/cervical-spondylotic-myelopathysurgical-treatment-options/ (2022)
- Kong, Q. J., et al. Anterior controllable antedisplacement and fusion (ACAF) vs posterior laminoplasty for multilevel severe cervical ossification of the posterior longitudinal ligament: Retrospective study based on a two-year follow-up. Orthopaedic Surgery. 13 (2), 474-483 (2021).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenWeitere Artikel entdecken
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten