Method Article
产前 delta-9-四氢大麻酚暴露的临床前模型评估其对神经发育结果的影响
摘要
随着立法限制的变化,导致大麻素产品的可及性增加,开发模型来研究这些暴露的影响至关重要,尤其是在怀孕期间。已经开发了一种通过自愿摄入适度接触产前大麻素的临床前模型,从而能够进行更深入的调查。
摘要
随着美国越来越多的州将娱乐性大麻(大麻素)合法化,产前大麻素暴露 (PCE) 变得越来越频繁。怀孕期间食用大麻素产品与各种异常结果有关,尽管历史研究是在这些产品的效力比当前产品低约 300% 的时期进行的。鉴于大麻素的使用不断增加,了解 PCE 可能对胎儿神经发育和随后的婴儿和儿童发育产生的潜在影响至关重要。以前的研究表明,PCE 会对后代的学习和记忆、行为技能、睡眠和注意力产生负面影响。本研究的目的是在临床前模型中,通过在怀孕期间自愿摄入 delta-9-四氢大麻酚 (THC),大麻素产品的精神活性成分来概括 PCE。本文概述了在整个妊娠期间实现中度 PCE 的程序。在这个模型中,对照组食用普通迷你巧克力/花生酱饼干,而 PCE 组食用混合到花生酱中的四氢大麻酚与迷你巧克力饼干。这种方法可以进一步研究 PCE 对发育结果的影响。
引言
随着产前大麻素产品使用率的增加1,这可能是受到美国大麻素产品日益合法化的影响,需要研究以更好地了解它们对胎儿发育的影响。Delta-9-四氢大麻酚 (THC) 是大麻素产品的精神活性成分,很容易穿过胎盘并与内源性内源性大麻素系统相互作用 2,3。内源性大麻素系统在神经发育中起着关键作用,可能是发生发育改变的途径。怀孕期间使用大麻素与出生体重减轻4 和早产风险增加有关 5,6。其他发育异常,例如一生中的社交行为和执行功能缺陷,也有报道 7,8,9。
随着时间的推移,大麻素效力和一般人群使用模式的变化凸显了对产前暴露对胎儿发育的潜在影响进行详细研究的必要性。怀孕期间使用大麻素产品的人数正在增加,因为这些产品通常被认为可以缓解抑郁、压力、疼痛、睡眠障碍和恶心等症状10,11。Dickson 等人12 进行了一项研究,调查了科罗拉多州 400 家大麻药房关于孕早期使用的建议,发现大约一半的药房 (50.5%) 向孕妇推荐食用。人们通常认为食物可以避免与吸烟相关的危害和健康风险13,14,这导致许多孕妇食用食物。
食物通过胃肠道系统输送大麻素,在那里 THC 被吸收到血液中,并通过门静脉运输到肝脏进行第一过代谢。在肝脏中,酶羟基化 THC 以产生 11-羟基四氢大麻酚 (11-OH-THC),这是一种高效的精神活性代谢物,很容易穿过血脑屏障15。虽然食物的初始精神作用需要更长的时间(30-90 分钟),但由此产生的“高”持续时间更长,在摄入后 2-4 小时达到峰值16,17。THC 在大鼠中的药代动力学半衰期为 1.3-7.3 小时18,19。
鉴于怀孕期间利用率的增加以及缺乏关于其对胎儿神经发育影响的数据,开发了怀孕期间自愿摄入 THC 的临床前模型,与报道的典型人类使用(口服以减轻恶心)更紧密地保持一致,以进一步描述对神经发育结果的影响。
研究方案
此处描述的所有程序均已获得新墨西哥大学健康科学中心 (UNM HSC) 机构动物护理和使用委员会 (IACUC) 的批准。所有实验均按照 ARRIVE 指南进行。Long-Evans (Blue Spruce, HsdBlu: LE) 大鼠购自商业来源。使用的雄性是经过验证的成年种鼠,到达时为 12 周龄,育种方案开始时为 15-16 周龄。雌性重 125-150 克,抵达时年龄约为 6-7 周龄。在繁殖时,雌性大约有 9-10 周大。确保所有潜在的母鼠都没有怀孕史至关重要。至少留出一周的时间来适应设施和新的住房环境。该协议的第一部分涉及孕前大麻素的消费,而第二部分则侧重于怀孕期间大麻素的暴露。 材料表中提供了所用动物、试剂和设备的详细信息。实验设计如图 1 所示。
1. 孕前接触大麻素
- 住房和维护
- 将动物单独饲养在标准大鼠静态微型隔离器笼子中,垫料在 22 °C 下,以反向 12 小时光照/黑暗时间表(每天 21:00 至 09:00 开灯)。
- 在整个研究过程中随意提供辐照食物(见材料表)和自来水。
- 材料和化学品制备
- 获取所有必需的材料和化学品(如 材料表中提供)。
- 将研究级 THC 保存在含有 10 mg/mL 或 20 mg/mL THC 溶解在乙醇中的小瓶中。
注意:使用适当的个人防护设备 (PPE),因为 THC 对皮肤有刺激性和吸入危险。将 THC 固定在钢柜中,因为它被美国卫生与公众服务部和美国食品和药物管理局归类为附表 I 受控物质。
- 基线测量
- 获得每只雌性大鼠的基线体重。
- 如有必要,请在此处暂停实验 1-2 周。
- 制备注入 THC 的饼干
- 每天 14:00 给药前 30 分钟准备饼干,以保持一致的喂食时间。
- 将迷你巧克力饼干分开,在奶油中加入大约半茶匙花生酱。
- 在组装饼干之前,将所需剂量的 THC(前 2 天 1.5 mg/kg,然后 3 mg/kg,持续 7 天)与花生酱混合。
- 消费评估
- 提供纯花生酱/迷你巧克力饼干 2-4 天,直到达到一致的食用量。从笼子中取出水,并在每天 14:00 用镊子给每只大鼠服用零食。
- 观察直到零食完全食用。如有必要,请去除残留物。
注意:以 1.5 mg/kg 的剂量施用 THC,持续 2 天,然后施用 3 mg/kg,持续 7 天。对于不立即食用的大鼠,将零食在笼子中放置长达 2 小时。 - 仅继续与表现出一致食用零食的大鼠。从实验中删除那些摄取不一致的 Segment。
- 评估怀孕前 2 周的食用量。
- PCE 后小组分配
- 将持续摄入的大鼠随机分配到普通(对照)或 THC 注入 (PCE) 饼干组。
- 在繁殖前至少允许 4 天没有饼干,以确保 THC 从他们的系统中清除。
2. 怀孕(产前)大麻素暴露
- 繁殖和怀孕确认
- 称量雌性以获得起始体重,然后将它们放入与经过验证的雄性饲养员(雄性是 THC 幼稚)一起的笼子中。
- 确保雌性大鼠在此期间不吃饼干。
- 通过阴道栓的存在来确认怀孕,阴道栓通常发生在交配后 24 小时。
- 称量雌鼠并将其放回家笼中。这被定义为妊娠日 (GD) 1。
- 怀孕期间输注 THC
- 在怀孕期间,每天 14:00 从 GD 1 开始提供原味或注入 THC 的 (3 mg/kg) 饼干。
- 继续这种方案,直到注意到母鼠正在筑巢等待分娩,此时停止 THC 暴露。
- 监测产妇体重增加
- 每周两次称量大鼠坝以评估产妇体重增加。
注意:新重量还用于计算饼干中应包含多少 THC,并根据母带的重量根据需要调整剂量。
- 每周两次称量大鼠坝以评估产妇体重增加。
- 停止接触 THC 和出生证明
- 当大坝在预期交货时间附近筑巢时,停止 THC 暴露程序。
- 后代出生后,记录活幼崽的数量。
- 将出生日期指定为出生后日 (P) 0。
- 断奶和后代的饲养
- 在出生后 (P) 23 断奶。
- 根据性别将断奶的后代与同窝伴侣分组。
- 水坝的安乐死
- 一旦窝产仔猪断奶,按照机构批准的方案对母鼠实施安乐死。
3. 术后步骤
- 后代住房和监测
- 确保所有后代都保存在适当的住房条件下,确保适当的温度、光线和通风。
- 定期监测幼犬是否有任何健康或发育问题,例如体重异常或发育迟缓。
- 基线评估
- 如果需要,在开始对后代进行实验之前,评估基线测量值,例如体重、反射或其他相关发育参数。
- 实验组分配
- 将幼崽随机分配到实验组,以尽量减少测试中的任何偏差。
- 将每个实验使用的幼崽数量限制为每窝 1-2 只幼崽,以减少潜在的窝产影响。
结果
为了建立 THC 的自愿消费,对许多零食进行了试验,以确定哪些零食对大鼠来说是可口的,并且会快速、持续地食用。
最初,试验了含和不含 THC 的无糖草莓味明胶块(1 立方毫升大小)。增加草莓糖浆调味剂的量,并以三种不同的浓度 (2 mg/kg/剂、3 mg/kg/剂和 5 mg/kg/剂) 试验 THC。大鼠没有始终如一地食用方块,并且被注意到在较高的 THC 浓度下迅速停止食用。众所周知,老鼠可以拒绝带有苦味或酸味的食物,这引起了人们对这种模式可能不适合自愿食用的担忧。
在咨询了机构兽医后,试验了各种其他零食,包括花生酱或奶酪饼干、花生酱迷你巧克力饼干、花生酱奶酪饼干和鱼形奶酪饼干,所有这些都是从亚马逊获得的。雌性大鼠始终食用加花生酱的迷你巧克力饼干,通常在获得款待后的 10-30 分钟内。然后将 THC 添加到带有花生酱的迷你巧克力饼干中,对照组和 THC 暴露组之间食用日常零食的母猪的百分比相似(分别为 67% 和 62%;p = 0.14)。
然后按照方案中的描述,坝子暴露于 THC,孕前和产前接触大麻素。育种前将母猪随机分配到对照组或 PCE 组 (THC 暴露量为 3 mg/kg/剂量)。两组之间的窝产仔数和产妇体重增加相似。对照组和 PCE 之间的死亡率 (从出生到 P2 的死亡率百分比) 和出生体重接近显着性 (分别为 0% vs. 0.04%, p = 0.06 和 6.25 g vs. 5.96 g,p = 0.07)。PCE 组的死亡率呈较高趋势,而 PCE 组的后代出生体重呈较低趋势(表 1 和 图 2),这与人类文献一致20。

图 1:实验设计。 母猪在繁殖前每天自愿摄入注入 THC 的饼干,以确保摄入量一致。不食用饼干的 dams 被排除在实验之外。其余的母鸡被随机分配在怀孕期间食用原味或注入 THC 的 (3 mg/kg) 饼干。分娩正常,幼仔在出生后第 23 天 (P) 断奶。 请单击此处查看此图的较大版本。
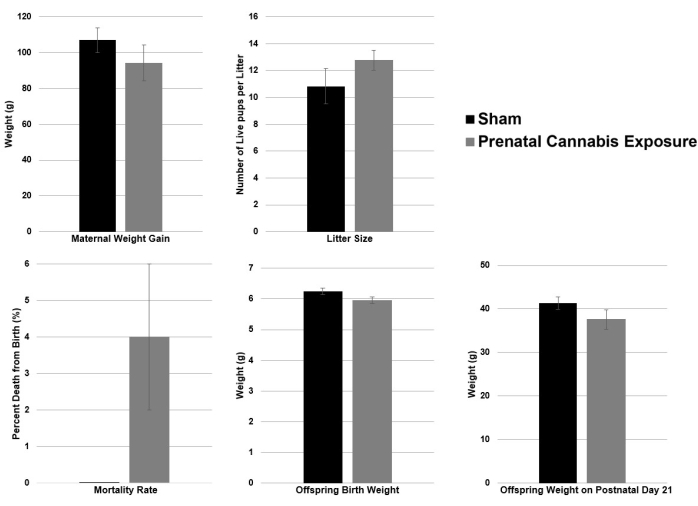
图 2:PCE 模型的母系和后代特征的图形表示。 该图提供了 PCE 模型中母体和后代特征的图形表示。 请单击此处查看此图的较大版本。
| 假 (n = 6 dams) | PCE (n = 4 dams) | p 值* | |
| 产妇体重增加 (g) | 107.00 ± 6.83 | 94.25 ± 10.03 | 0.48 |
| 窝产仔数(活仔数/窝数) | 10.83 ± 1.31 | 12.75 ± 0.74 | 0.22 |
| 死亡率(从出生到 P2 的死亡百分比) | 0.00 ± 0.00 | 0.04 ± 0.02 | 0.06 |
| 后代出生体重 (g) | 6.25 ± 0.11 | 5.96 ± 0.10 | 0.07 |
| 出生后第 21 天的后代体重 (g) | 41,31 ± 1,40 | 37,61 ± 2,22 | 0.17 |
| *P 值是使用学生的 t 检验计算的 | |||
表 1:PCE 模型的母系和后代特征。 通过妊娠日 (GD) 22 的母亲体重增加以克为单位进行测量,组间差异不显著 (p = 0.48)。该表还包括平均窝产仔数、死亡率(从出生到 P2 的死亡百分比)、每窝后代的出生体重以及 P21 的体重。所有数据均显示为平均值±平均值 (SEM) 的标准误差;*p 值是使用学生 t 检验计算的。
讨论
此处概述的 PCE 范式涉及怀孕的鼠坝自愿食用 THC。这是第一项在临床前模型中通过自愿摄入对怀孕大鼠dams进行THC给药的研究。两组大鼠都食用相同的大鼠食物,最大限度地减少了组间营养和热量摄入的潜在差异。动物模型具有控制 PCE 的时间和剂量用于研究目的的优势。
评估怀孕前消费以确定在消费方案的后续阶段以所需水平消耗 THC 的大鼠。这种方法确保所有雌性大鼠在怀孕前都有摄入 THC 的经历,更准确地反映了人类行为5,其中个体通常在怀孕前使用 THC。在这个模型中,PCE 发生在整个妊娠发育过程中,大致对应于人类妊娠的前两个三个月。有证据表明,大麻素的使用在妊娠早期最常见,在妊娠中期减少,在孕晚期进一步下降1。
内源性大麻素受体直到妊娠 5-6 周才在胎儿中表达21。在此期间之前的暴露可能不会直接影响胎儿的大脑发育,尽管通过胎盘中内源性大麻素受体表达的间接影响仍然是可能的22。因此,专注于神经发育结果的研究人员将需要考虑与感兴趣的特定结果相关的暴露时间。
该方案的一个关键步骤是能够经常测量 THC 水平,以确保消费达到目标血清水平。正在进行的实验正在测量整个怀孕期间的血清水平,以确保尽管怀孕期间发生代谢变化,但仍能保持稳定的水平。
我们考虑了其他口服给药技术,例如口服管饲法。然而,该模型的目标是尽可能保持临床相关性。管饲法给药可诱导大鼠显着应激,导致血压升高、血浆皮质酮水平升高和其他不良反应23,24。因此,我们选择自愿摄入以尽量减少任何意外的副作用。
这项研究的局限性包括确保一致的食用和在准备零食时需要谨慎,因为准备过程中 THC 剂量的不准确可能会影响结果。虽然个体大鼠的新陈代谢可能不同,但考虑到临床相关性的愿望,这也是一个优势。
总体而言,自愿摄入以产生适度 THC 暴露的临床前模型是可行的。该模型开发将允许对神经发育结果以及其他感兴趣的领域进行进一步深入研究。未来的研究将有助于越来越多的关于 PCE 对胎儿发育影响的文献。
披露声明
作者没有需要披露的利益冲突。
致谢
感谢美国国家药物滥用研究所 (NIDA) 药物供应计划的慷慨供应 THC。由新墨西哥大学儿科研究分配委员会拨款和新生儿学部支持。
材料
| Name | Company | Catalog Number | Comments |
| 5L0D PicoLab Laboratory Rodent Diet, irradiated | Purina LabDiet | 5L0D | |
| Cellulose/paper bedding BioFresh Comfort Bedding | BioFresh Vet | NA | https://biofreshvet.com/products/ |
| Digital Kitchen Scale | Etekcity | EK4150 | |
| Female rats, 125-150 g | Inotiv | 14005F | |
| Long-Evans rats (Blue Spruce, HsdBlu: LE) | Inotiv | 14016M | |
| N10 Rodent Plastic Cage Bottoms | Ancare | N10PLF | |
| N10 Rodent Wire Lids | Ancare | N10SS | |
| Narrow Pattern Forceps | Fine Science tools (FST) | 11002-14 | |
| OREO mini chocolate Sandwich cookies, Go Paks, 12-3.5 oz cups | Amazon | B0198TUO7W | |
| proven adult breeder males | Inotiv | 14016M | |
| Rat static polysulfone microisolator cages (R20): | |||
| Research Grade THC (only available with a DEA license, Schedule I drug) | NIDA | NA | https://nida.nih.gov/research/research-data-measures-resources/nida-drug-supply-program |
| SKIPPY Creamy Peanut Butter spread | Amazon | B0C75KZ28C | |
| THC Consumption Supplies: |
参考文献
- Volkow, N. D., Han, B., Compton, W. M., McCance-Katz, E. F. Self-reported medical and nonmedical cannabis use among pregnant women in the United States. JAMA. 322 (2), 167-169 (2019).
- de Salas-Quiroga, A., et al. Prenatal exposure to cannabinoids evokes long-lasting functional alterations by targeting CB1 receptors on developing cortical neurons. Proc Natl Acad Sci USA. 112 (44), 13693-13698 (2015).
- Baglot, S. L., et al. Maternal-fetal transmission of delta-9-tetrahydrocannabinol (THC) and its metabolites following inhalation and injection exposure during pregnancy in rats. J Neurosci Res. 100 (3), 713-730 (2022).
- Ryan, S. A., Ammerman, S. D., O'Connor, M. E. Committee on Substance Use and Prevention; Section on Breastfeeding. Marijuana use during pregnancy and breastfeeding: implications for neonatal and childhood outcomes. Pediatrics. 142 (3), e20181889(2018).
- Corsi, D. J., et al. Association between self-reported prenatal cannabis use and maternal, perinatal, and neonatal outcomes. JAMA. 322 (2), 145-152 (2019).
- Duko, B., Dachew, B. A., Pereira, G., Alati, R. The effect of prenatal cannabis exposure on offspring preterm birth: a cumulative meta-analysis. Addiction. 118 (4), 607-619 (2023).
- Scheyer, A. F., Melis, M., Trezza, V., Manzoni, O. J. J. Trends in Neurosciences. Trends Neurosci. 42 (12), 871-884 (2019).
- Nashed, M. G., Hardy, D. B., Laviolette, S. R. Prenatal Cannabinoid Exposure: Emerging Evidence of Physiological and Neuropsychiatric Abnormalities. Front Psychiatry. 11, 624275(2021).
- Lin, A., et al. Prenatal cannabinoid exposure: why expecting individuals should take a pregnancy pause from using cannabinoid products. Front Pediatr. 11, 1278227(2023).
- Chang, J. C., et al. Beliefs and attitudes regarding prenatal marijuana use: perspectives of pregnant women who report use. Drug Alcohol Depend. 196, 14-20 (2019).
- Young-Wolff, K. C., et al. Trends in cannabis polysubstance use during early pregnancy among patients in a large health care system in Northern California. JAMA Netw Open. 5 (6), e2215418(2022).
- Dickson, B., et al. Recommendations from cannabis dispensaries about first-trimester cannabis use. Obstet Gynecol. 131 (6), 1031-1038 (2018).
- Murphy, F., et al. Baby boomers and cannabis delivery systems. J Drug Issues. 45 (3), 293-313 (2015).
- Barrus, D. G., et al. Tasty THC: Promises and challenges of cannabis edibles. Methods Rep, RTI Press. , 1-22 (2016).
- Mura, P., Kintz, P., Dumestre, V., Raul, S., Hauet, T. THC can be detected in brain while absent in blood. J Anal Toxicol. 29 (8), 842-843 (2005).
- Grotenhermen, F. Pharmacokinetics and pharmacodynamics of cannabinoids. Clin Pharmacol Ther. 42 (4), 327-360 (2003).
- Thompson, R., DeJong, K., Lo, J. Marijuana Use in Pregnancy: A Review. Obstet Gynecol Surv. 74 (7), 415-428 (2019).
- Ravula, A., et al. Pharmacokinetic and pharmacodynamic characterization of tetrahydrocannabinol-induced cannabinoid dependence after chronic passive cannabis smoke exposure in rats. Cannabis Cannabinoid Res. 4 (4), 240-254 (2019).
- Zgair, A., et al. Dietary fats and pharmaceutical lipid excipients increase systemic exposure to orally administered cannabis and cannabis-based medicines. Am J Transl Res. 8 (8), 3448-3459 (2016).
- Mulligan, M. K., Hamre, K. M. Influence of prenatal cannabinoid exposure on early development and beyond. Adv Drug Alcohol Res. 3, 10981(2023).
- Paul, S. E., et al. Associations between prenatal cannabis exposure and childhood outcomes: Results from the ABCD study. JAMA Psychiatry. 78 (1), 64-76 (2021).
- Fügedi, G., et al. Increased placental expression of cannabinoid receptor 1 in preeclampsia: An observational study. BMC Pregnancy Childbirth. 14, 395(2014).
- Walker, M. K., et al. A less stressful alternative to oral gavage for pharmacological and toxicological studies in mice. Toxicol Appl Pharmacol. 260 (1), 65-69 (2012).
- Brown, A. P., Dinger, N., Levine, B. S. Stress produced by gavage administration in the rat. Contemp Top Lab Anim Sci. 39 (1), 17-21 (2000).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。