Method Article
Peri-implantitis tedavisinde kullanılan mekanik yöntemlerin implant yüzey dekontaminasyonu ve pürüzlülüğü üzerine etkileri
Bu Makalede
Özet
Mevcut protokol, klinik karar vermeye katkıda bulunmak için in vitro implant yüzey dekontaminasyonu ve pürüzlülük araştırmaları için kullanılabilecek mürekkep boyamaya dayalı deneysel bir modeli tanımlamaktadır.
Özet
Dental implant yüzeylerinin dekontamine edilmesi için çeşitli mekanik yöntemler çeşitli başarılarla önerilmiştir. Bu in vitro çalışma, eritritol tozu, bir polieter-eter-keton (PEEK) ultrasonik uç ve titanyum küretler (TIT) ile bir hava aşındırma (AA) sisteminin dekontaminasyon verimliliğini ve bunların taramalı elektron mikroskobu (SEM) kullanılarak implant yüzey topografisi üzerindeki etkilerini değerlendirdi. Toplam 60 implant kalıcı kırmızı mürekkeple boyandı ve 3D baskılı Sınıf 1A ve Sınıf 1B peri-implantitis defektlerine yerleştirildi, defekt tipine ve tedavi protokolüne göre altı grup (grup başına n = 10) oluşturuldu. Ek olarak, bir pozitif ve bir negatif kontrol implantı kullanıldı. Eritritol tozu, PEEK ultrasonik uçlar ve titanyum küretler Class 1A defektlerde 2 dk, Class 1B defektlerde 3 dakika süreyle uygulandı. Kalıntı kırmızı mürekkep alanları dijital yazılımlarla ölçüldü ve implant yüzey değişiklikleri SEM ve EDS kullanılarak analiz edildi. Yöntemlerin hiçbiri tam dekontaminasyon sağlamadı. Bununla birlikte, eritritol tozu önemli ölçüde en etkili olanıydı ve %24 ± %6'lık bir kalıntı mürekkep oranı bıraktı (p < 0.001). PEEK ultrasonik uçlar %41 ± %4 mürekkep kalıntısı ile sonuçlanırken, titanyum küretler %55 ± %3 bıraktı. Tüm yöntemler arasında anlamlı farklılıklar gözlendi. Sınıf 1A ve Sınıf 1B defektler arasında dekontaminasyon etkinliği açısından anlamlı bir fark bulunmadı. SEM analizi, eritritol tozu ve PEEK uçları ile minimum yüzey hasarı gösterirken, titanyum küretler orta ila ciddi hasara neden oldu. Hem dekontaminasyon verimliliğine hem de yüzey korumasına dayalı olarak, eritritol tozu ve PEEK uçlar peri-implantitis tedavisi için güvenli ve etkili seçeneklerdir, titanyum küretler ise daha az etkilidir ve önemli yüzey hasarına neden olur. Bu bulgular peri-implantitis tedavi planlamasında klinisyenlere yardımcı olabilir.
Giriş
Dental implant tedavisi, dünya çapında eksik dişlerin yerine konması için en yaygın ve tercih edilen protokoldür. Uzun süreli takip çalışmaları, tam veya kısmi dişsizlik tedavisinde implant destekli restorasyonların kullanılmasının sağkalım açısından öngörülebilir sonuçlar ve yüksek başarı oranları sağladığını göstermiştir. Bununla birlikte, implantların cerrahi olarak yerleştirilmesi ve restorasyonunu takiben sert ve yumuşak dokuları etkileyen çeşitli komplikasyonlar ortaya çıkabilir1. 2017 yılında, Periodontal ve Peri-implant Hastalıkların ve Durumların Sınıflandırılması Dünya Çalıştayı, peri-implant dokuları etkileyen hastalıklar için tanımlar ve ayırıcı tanılar getirmiştir2. Bu tanıma göre, peri-implantitis, sondalama ve/veya süpürasyon sırasında kanama, artmış sondalama derinlikleri ve/veya peri-implant mukozadaki mukozal kenarın durgunluğu ve destekleyici kemiğin radyografik kaybı dahil olmak üzere klinik inflamasyon belirtileri ile karakterize geri dönüşümsüz bir patolojik durumdur2. Peri-implant hastalıkların etiyolojisi çok faktörlüdür ve bazı bireyler bu duruma diğerlerinden daha duyarlıdır. Bireylerin spesifik yatkınlıkları, implant çevresi hastalık gelişme riskini artırabilir ve bu da implant kaybına yol açabilir. Peri-implant hastalıkların etiyolojisinde rol oynayan diğer faktörler ise hastaya bağlı faktörler (sigara, sistemik hastalıklar, periodontal hastalık öyküsü, ağız hijyeni); keratinize mukozanın durumu, implant bölgesindeki kemik ve yumuşak dokuların miktarı ve kalitesi; implant ve çevresindeki dokular üzerindeki kuvvetler; implant yerleştirilmesi sırasında karşılaşılan komplikasyonlar; cerrahi ve protetik tedavileri yapan hekimin deneyim ve becerisi2. Buna ek olarak, yakın zamanda yeni bir risk değerlendirmesi ve tedavi konsepti olan İmplant Hastalığı Risk Değerlendirme Aracı (IDRA)3 tanıtılmıştır. Bu araç, her biri peri-implantitis ile belgelenmiş bir ilişkiye sahip sekiz parametreden oluşan fonksiyonel bir diyagram olarak geliştirilmiştir. Sekizgenin vektörleri, periodontitis öyküsü, sondalamada kanama olan implant ve diş bölgelerinin yüzdesi (BoP), sondalama cebi derinliği 5 mm'≥ olan diş/implant sayısı, periodontal kemik kaybı oranı (hastanın yaşına göre radyografiler), periodontite yatkınlık, destekleyici periodontal tedavi (SPT) sıklığı ve protezin tasarımıdır.
Son sistematik derlemeler, peri-implantitis prevalansının hasta düzeyinde %19.53 ve implant düzeyinde %12.53 olduğunu göstermiştir3. Dünya çapında her yıl yaklaşık 5 milyondan fazla implant yerleştirildiği ve pazar büyüklüğünün 4 milyar USD'yi aştığı göz önüne alındığında, peri-implantitis popülasyon için önemli bir sağlık sorununu temsil etmektedir. Tedavi edilmezse, peri-implantitis, etkilenen implantın ve implant destekli protezin kaybıyla sonuçlanır ve hem diş hekimi hem de hasta için büyük bir sıkıntıya neden olur.
Peri-implant hastalıkların tedavisi cerrahi olmayan ve cerrahi yaklaşımlar olarak ikiye ayrılabilir. Periodontitis4'ün tedavisinde uç noktaların başarısı için makul bir beklenti olmasına rağmen, peri-implantitis tedavisi için karşılaştırılabilir kanıtlar hala azdır. Bu nedenle, peri-implantitisin aşamalı bir yaklaşım ve cerrahi olmayan tedavisinin mantığı, tedavi invazivliğini artırmadan önce nispeten basit yaklaşımlarla biyofilm ve inflamasyon kontrolünün denenmesi ve daha iyi biyofilm ve risk faktörü kontrolü sağlandığında cerrahi adımın gerçekleştirilmesidir. Bu, OH talimatları ve motivasyonu, risk faktörü kontrolü, biyofilm tutucu faktörlerin kontrolü ve protez bileşenlerinin değerlendirilmesi, supramarjinal ve submarjinal enstrümantasyon ve gerektiğinde eşlik eden periodontal tedavi dahil olmak üzere protez temizliği/çıkarılması/modifikasyonunu içerir. Bu nedenle, cerrahi olmayan tedavi her zaman ilk adım olmalıdır5. Erken peri-implantitis için risk faktörlerinin azaltılması ve cerrahi olmayan tedavi yeterli olabilir, ancak kemik kaybından sonra derin ceplerde biyofilmin tamamen çıkarılması genellikle zordur. Cerrahi olmayan tedaviden sonra yeniden değerlendirme aşamasında, kalıcı cep derinlikleri (≥ 6 mm) ve sondalama kanaması (BoP) peri-implantitisin potansiyel ilerlemesini gösterir. Bu belirtiler varsa cerrahi girişimler önerilir6. Peri-implantitisin cerrahi tedavisi (i) açık flep debridmanını, (ii) rezektif flep cerrahisini, (iii) implant çevresi kemik defektlerinin rekonstrüktif yaklaşımlarla tedavisini, (iv) implant yüzeyi dekontaminasyonu için ek yöntemleri ve (v) lokal/sistemik antibiyotiklerin yardımcı kullanımınıiçerir 7.
Peri-implantitisin en önemli etiyolojik faktörü implant yüzeyinde kolonize olan patojenik biyofilmdir6. Bu biyofilmin uzaklaştırılması, mekanik, kimyasal ve lazer dekontaminasyon yöntemlerini içeren tüm tedavi protokollerinin ana prensibi ve hedefidir7.
Mekanik debridmanda plastik, karbon ve titanyum küretler, plastik ve metal uçlu ultrasonik cihazlar, titanyum fırçalar ve çeşitli tozlara sahip hava aşındırıcı (AA) sistemler kullanılır. Biyofilmin tamamen ortadan kaldırılması zor olsa da, bu tedaviler klinik faydalar sağlar. Antiseptikler 8,antibiyotikler 9 ve rezektif ve rejeneratif cerrahi10 ile veya antiseptiklerolmadan mekanik debridman protokolleri dahil olmak üzere çeşitli klinik müdahaleler, değişen derecelerde klinik başarı ile kullanılmıştır. Bununla birlikte, implant yüzeyinin kimyasal ve fiziksel özelliklerinde de değişikliklere neden olurlar ve muhtemelen yeni kemik oluşumunu ve yeniden osseointegrasyonu zorlaştırırlar.
Mekanik yöntemler arasında, farklı toz bileşimleri kullanan AA prosedürleri en iyi temizleme etkinliğini göstermiştir 11,12,13. Bununla birlikte, artık parçacıkların varlığı yüzey topografyasını değiştirebilir ve biyouyumluluğu azaltabilir14. Glisin, ardından sodyum bikarbonat, AA sistemlerinde en çok kullanılan tozdur8. Son zamanlarda, eritritol (14 μm) gibi daha küçük hava aşındırıcı partiküller, azaltılmış yüzey hasarı ile etkili dekontaminasyon için ilgi görmeye başlamıştır9. Çelik uçlara göre daha az yüzey hasarına neden olan titanyum ve plastik küretler biyofilm dekontaminasyonunda etkilidir15. Poli-eter-eter-ketondan (PEEK) yapılan ultrasonik kazıyıcı uçlar ayrıca minimum yüzey hasarı ile bakteri yükünü azaltır10. Dekontaminasyon yöntemleri, implant yüzeylerinin yüksek pürüzlülüğünü dikkate almalı ve önemli yüzey hasarına neden olmadan bakteriyel biyofilmi uzaklaştırmayı amaçlamalıdır. Kapsamlı in vitro, in vivo ve klinik araştırmalar yapılmış olmasına rağmen, bugüne kadar peri-implantitis tedavisi için hala bir fikir birliği ve altın standart bir protokol yoktur. Çok sayıda dental implanta bağlı olarak peri-implant hastalıklarının artan prevalansı, kontamine yüzeylerin tedavisinde kanıta dayalı, öngörülebilir bir yaklaşım gerektirmektedir. Bu çalışmanın amacı, hava aşındırıcı (AA) sistemler, PEEK ultrasonik uçlar ve titanyum küretler gibi farklı dekontaminasyon yöntemlerinin implant yüzeyi dekontaminasyonundaki etkinliğini değerlendirmek ve SEM analizi ile implant yüzey pürüzlülüğü üzerindeki etkilerini değerlendirmektir.
Protokol
Çalışma protokolü, Akdeniz Üniversitesi, Antalya, Türkiye etik kurulu (TBAEK-363) tarafından onaylanmıştır. Bu çalışma Akdeniz Üniversitesi Araştırma Fonu tarafından desteklenmiştir (Proje no: TDH-2024-6676). Çalışmada, 4,2 mm x 11 mm boyutlarında, yaka üzerinde 1,7 mm ölçülerinde bir mikro diş tasarımına sahip vida şeklinde bir diş implantı (PrimeTaper EV İmplant) kullanıldı. İyi tanımlanmış OsseoSpeed yüzeyini elde etmek için kumlama ve seyreltilmiş hidroflorik asit ile asitle aşındırma ile yüzey hazırlığı.
1. Deneysel peri-implantitis modellerinin hazırlanması
NOT: Üç dekontaminasyon mekanik arıtma yöntemi (hava aşındırıcı (AA), polietereterketon (PEEK) ultrasonik ve titanyum küretler; Malzeme Tablosu) iki farklı peri-implantitis defektinde tip11 (Sınıf 1A ve Sınıf 1B) analiz edildi. Bu nedenle, altı deney grubu vardı (Şekil 1). Biri pozitif diğeri negatif kontrol implantı olmak üzere toplam 62 implant kullanıldı. İlk olarak Sharhmann ve ark.16 tarafından geliştirilen bu in vitro çalışma deseni, literatürde çeşitli araştırmacılar 12,13,14,15,16,17,18 tarafından değiştirilmiştir (Şekil 2). Gruplar arasında biyofilm giderme etkinliğinde %10'luk bir fark olduğu varsayılarak örneklem büyüklüğü G*power, etki büyüklüğü 0.50, tip I hata %5 ve %80 güce sahip altı grup için 60 (her grup için 10) olarak belirlenmiştir.

Şekil 1: Deney gruplarının akış şeması. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
- Eğitim mandibular fantom modelinden bir birinci azı dişini çıkarın. Plastik dişler bu fantom modele vidalarla sabitlenir. İlk azı dişi sökün ve ipliği soketten çıkarın. Düz bir alveolar sırt oluşturmak için soketi kaplayacak şekilde yumuşak silikon malzemeyi kalıplayarak soketi doldurun.
NOT: Tam dişsiz bir bölgeye yerleştirilen bir implantın simülasyonu oluşturulmuştur. - Dijital bir tasarım oluşturmak için hazırlanan modeli bir laboratuvar tarayıcısında tarayın.
- Dijital olarak 3D Sınıf 1A ve Sınıf 1B11 peri-implantitis kemik defektleri oluşturun. Exocad yazılım programını açın. Taranan model dosyasını yükleyin. Ardından Tasarım'a tıklayın ve Uzman Modu'nu seçin. Ağı Düzenle seçeneğiyle düzensiz alanları kaldırın. Ardından sağ tıklayın ve bilgisayardaki ilgili klasör üzerinde Taramayı Dosya Olarak Kaydet'i seçin.
- Mesh Ekle/Kaldır seçeneğini > Araçlar'ı seçin, Wax Taraması> Dosya Yükle'yi seçin ve klasöre yeni kaydedilen dosyayı seçin. Bundan sonra, sağdaki Sihirbaz Modu'nu tıklayın.
- Ortaya çıkan yeni STL modelinde, diş soketinde bir kusur simülasyonu oluşturun. Bunu yapmak için sol taraftaki Ekle/Kaldır'a tıklayın. Oval Şekil Fırça Boyutu'nu seçin. Daha sonra, shift ve sol tıklamayı aynı anda kullanarak model üzerinde kusuru oluşturun. İmplantın bukkal yüzeyinde Class 1A defektler için defektin uzunluğunu 5 mm ve genişliğini 4,2 mm (implantın çapına karşılık gelir) ve Class 1B defektler için 5-5-5 mm olarak ayarlayınız.
- Kusurun yatay genişliğini daraltmak için, sol taraftaki Anatomi'ye tıklayarak ve defektin vestibüler genişliğini içe doğru daraltarak Cusps'u seçin. Ardından, sahneyi sağ tıklayın ve bir dosya olarak kaydedin.
- Son bir model oluşturmak için programı yeniden başlatın ve kaydedilen klasörü yeniden yükleyin. Ardından sağdaki Sihirbaz Modu ve Model Hizalama seçeneğini seçin. Sol tarafta bulunan model türünü Digital Waxup Model (Dijital Waxup Modeli) olarak seçin. Soldaki model tasarımı bölümüne ulaşana kadar birkaç kez İleri'ye tıklayın. Tam Model seçeneğini belirleyin ve iki kez İleri'ye tıklayın. Model dosyası tamamlandıktan sonra Explorer ile açın ve yazdırmaya hazırdır.
- Tasarlanan modelin STL dosyalarını 3D yazıcıya iletin. Oluşturulan dijital modelleri bir model reçinesi kullanarak yazdırın.
- Deneysel modelleri %96 etanolde 5-10 dakika durulayın. Temizleme işleminden sonra modelleri ışık yayan kürleme cihazına yerleştirin ve üreticinin talimatlarına uygun olarak doz ayarında 5 dakika boyunca ışıkla kürleyin.
NOT: İmplant delme için uygun, yüksek çekme, eğilme ve basınç dayanımına sahip bir reçine modeli kullanın. Basılı modeli, üreticinin talimatlarına göre alkol bazlı solüsyonlarla temizleyin ve yeterince ışıkla sertleştirildiğinden emin olun.
2. İmplantların boyanması
- Test implantlarını viskoz suya dayanıklı kırmızı mürekkebe batırın. 15 saniye boyunca implant yüzeyinin tüm parçalarının tamamen ve homojen bir şekilde mürekkeple kaplandığından emin olun. El teması olmadan sürücü el aletlerini veya baskı direklerini kullanarak implantları steril kaptan çıkarın.
NOT: Bu boyama, fotoğraf analizi için optik olarak görünür bir biyofilm vekilini simüle edecektir. - Mürekkebin eşit bir şekilde dağılmasını sağlamak için lekeli implantları bir diş ünitesi hava şırıngası ile havayla kurutun. Lekeli implantları oda sıcaklığında 24 saat daha kurutun. İmplantları el teması olmadan el aletleriyle izole bir şekilde kurutun.
3. Lekeli implantların yerleştirilmesi
- Bir dental fizyoloji dispenserinin ayarlarını aşağıdaki gibi yapın: 800 rpm, tuzlu sulama olmadan 40 N tork.
- 11 mm uzunluğunda ve 4,2 mm genişliğindeki implantları yerleştirmek için deneysel modeller üzerinde cerrahi implant matkapları ile implant yuvasını oluşturun. Her iki tip kusuru olan modeller için aynı implant soketini hazırlayın (Sınıf 1A ve 1B kusurlu modeller).
- Birincil stabiliteyi elde etmek için implant matkaplarını üreticinin talimatlarına göre sırayla kullanın. Delindikten sonra kalan kalıntıları hava-su şırıngasıyla temizleyin, ardından implantları yerleştirin. İmplantların mikro hareketini önlemek ve modellerde mikro çatlakları önlemek için deneysel peri-implantitis modellerini çalışma platformunda bir kelepçe ile stabilize edin.
- İmplantları bir taşıyıcı el aleti ile yuvalara yerleştirin. Bukkal yüzeyde 5 mm açıkta kalan alan bırakın. İmplantların, modelin lingual kemik tepesi üzerinde aynı seviyede daldırıldığından emin olun. Lekeli implant yüzeyine dokunmaktan kaçının.
4. İmplantların dekontaminasyonu
- İmplantları deneysel 1A ve 1B kusur modellerinden çıkarmadan gruplar halinde dekontamine etmeye başlayın.
- Hava aşındırıcı sistem: Cihazı 14 μm eritritol tozu ile su sulama ile tam güce ayarlayın. Cihazın ucunu implant yüzeyinden 2-3 mm uzakta tutun ve tozu açıkta kalan peri-implantitis defektine eşit şekilde uygulayın. Çalışma süresini 2A kusurlar için 1 dakika ve 3B kusurlar için 1 dakika ile sınırlayın.
- Polietereterketon (PEEK) ultrasonik uç: Cihazı maksimum su sulaması ile 8 güce (%80) ayarlayın. PEEK el aletini ultrasonik kullanıma uygun bir şekilde tutun. İmplant yüzeyinde doğrusal ve paralel hareketlerle dekontaminasyon gerçekleştirin. PEEK ucunu tasarımının izin verdiği kadar iplikler arasına uygulayın. Çalışma süresini 2A kusurlar için 1 dakika ve 3B kusurlar için 1 dakika ile sınırlayın.
- Titanyum küretler: 1A defektler için 2 dk ve 1B defektler için 3 dk boyunca 5 mm açıkta kalan implant yüzeyine yaklaşık 0,75 N'luk bir kuvvetle implant yüzeyine 60°-90°'de sabit basınçla ardışık kontaklar uygulayın.
- Dekontaminasyondan sonra, el teması olmadan sürücü parçasını kullanarak implantı çıkarın. Dekontaminasyondan sonra modeller deforme olursa, yedek modellere geçin. Deneysel peri-implantitis modellerini çalışma platformunda bir kelepçe ile stabilize edin.
NOT: Tüm yöntemler tek bir araştırmacı tarafından kalibre edilmeli ve uygulanmalıdır.
5. Fotoğrafik görüntüleme
- Uyumlu bir implant sürücü parçası ile implantları modelden çıkarın. Yüzeydeki gevşemiş parçacıkları/kalıntıları gidermek için implantları 20 saniye havayla kurutun.
- İmplant yüzeyindeki ipliklerin apikal ve koronal kısımlarını değerlendirmek için düz görünümler, 30° apikal görünümler ve 30° koronal görünümler çekmek için implantları özel olarak tasarlanmış akrilik fotoğraf modellerine yerleştirin.
- Fotoğraf makinesini bir tripoda yerleştirin ve fotoğraf makinesi ayarlarını standart hale getirin (mesafe 15 cm, ISO 160, diyafram f/16, pozlama süresi 1/250 sn). Odanın yeterince aydınlatıldığından emin olun. Kamerayı bir tripod ile sabitlemek gerekir.
- Dijital fotoğrafları bir flaşla RAW formatında çekin. Sınıf 1A kusurları için toplam 90 bukkal fotoğraf (bir düz, bir 30° apikal ve her implant yüzeyi için bir 30°koronal) ve Sınıf 1B kusurları için 270 fotoğraf (düz, 30° apikal ve her implant için her bukkal, mesiyal ve distal yüzeyden 30°koronal) elde edin. Daha fazla görüntü analizi için tüm dijital fotoğraf dosyalarını bir sabit diske kaydedin.
6. Görüntü analizi
- Tüm analizleri dijital görüntü yazılımı (ImageJ) üzerinde gerçekleştirin. Analizden önce, görüntüde sadece implantın göründüğünden emin olmak için bir Photoshop programı (Photoroom) kullanarak fotoğrafların arka planını siyah yapın. Uygulamayı açın ve ardından galerideki her bir resmi ekleyin. Görüntüden arka planı kaldırın ve seçeneklerden Siyah Arka Plan'ı seçin.
- Görüntüyü ImageJ'ye sürükleyip bırakın. İmplantın 5 mm koronal kısmını kaplayacak şekilde görüntüye bir kare çizin. Ardından standardizasyon için Görüntü > Kırp'ı tıklayın. Her görüntü için aynı işlemi tekrarlayın.
- Görüntü ˃ Tür ˃ 8 bit'e tıklayarak görüntüleri 8 bit formatına dönüştürün ve alan hesaplamaları için Görüntü ˃ Ayarla ˃ Eşik'e tıklayarak eşikleri ayarlayın.
- Analiz Et ˃ Ölç ˃ Alanı'na tıklayarak tüm implant yüzey alanını ve kırmızı renk kalıntı alanını hesaplayın.
- Elde edilen piksel alanını bir elektronik tablo dosyasına kaydedin. Ham görüntü verilerini kaydetmek için ayrı bir elektronik tablo dosyası oluşturun.
- Kırmızı renk kalıntılarının yüzdesini elde etmek için, kırmızı görüntülenen alanı 100 ile çarpın ve toplam implant yüzey alanına bölün.
7. SEM analizi
- Analiz gününe kadar tüm implantları steril kutularında saklayınız.
- SEM analizinden önce, her tedavi grubundan rastgele bir temsili numune seçin. Her gruptan seçilen örneklere ek olarak, bir steril implant ekleyin ve sadece implant tamamen mürekkeple kaplıdır. Böylece SEM analizi için toplam sekiz implant numunesi hazırlayın.
- SEM analizinden önce implant yüzeyindeki mikro tozu çıkarmak için bir gaz tabancası kullanarak 20 saniye boyunca nitrojen gazı püskürtün.
NOT: Cihazın ileri teknolojiye sahip olması nedeniyle ek bir altın kaplama uygulanmamıştır. - Her bir implantı, bukkal düz yüzeyin el dekontaminasyonu olmadan analizine izin verecek şekilde iletken karbon yapışkan disklerle SEM saplamalarına monte edin. Grupların karışıklığını önlemek için bunları numaraya göre sıralayın.
- Alete yerleştirilen implantlardan bir alan seçin ve farklı büyütme oranlarında görüntüler yakalayın. İmplant yüzeylerinin farklı bölgeleri (mesial veya distal) için aynı işlemi tekrarlayın. Ortalama 12 mm çalışma mesafesi ile 10-30 kV'da çalışan bir SEM cihazı kullanan görüntüler için 100x, 1000x ve 5000x büyütme kullanın.
NOT: SEM analizi sırasında standardizasyonu sağlamak için her implant için yaka bölgesinden ikinci mikro iplikçik ve vücuttan ikinci makro iplikçik seçilmiştir. Bazı görüntüler için, karşılaştırma için görüntüleme sırasında element analizi (EDS) yapılması önerilir.

Şekil 2: Çalışmanın akış şeması. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
8. İstatistiksel analiz
- Kategorik değişkenleri sayılar ve yüzdeler ve sürekli değişkenleri ortalama ve standart sapma olarak ifade edin. Shapiro-Wilk testi ile sürekli değişkenler için dağılımın normalliğini onaylayın.
- Kusur grupları arasındaki sürekli değişkenlerin karşılaştırılması için Student t-testini kullanın. İkiden fazla grubun karşılaştırılması için, istatistiksel hipotezlerin gerçekleşip gerçekleşmediğine bağlı olarak tek yönlü varyans analizi veya Kruskal Wallis testi kullanın.
- Normal dağılımlı veriler için, varyansların homojenliği ile ilgili olarak, grupların çoklu karşılaştırmaları için Tukey testlerini kullanın. Normal olmayan dağılımlı veriler için, grupların çoklu karşılaştırmaları için Bonferroni tarafından ayarlanmış Mann-Whitney U testini kullanın. Tüm istatistiksel analizler IBM SPSS 20 programı kullanılarak yapılmıştır. Tüm testler için istatistiksel anlamlılık düzeyi 0.05 olarak kabul edildi.
Sonuçlar
İmplant yüzeylerinin dekontaminasyonunu analiz etmek için burada açıklanan deneysel protokol, çeşitli tedavi prosedürleri arasında önemli farklılıklar ortaya koymuştur. Ek olarak, tedavi sonrası SEM protokolü de implant yüzeylerinde çalışma grupları arasında değişen derecelerde önemli değişiklikler gösterdi.
Dekontaminasyon sonrası implant düzeyinde karşılaştırmalar (Toplam implant ortalamaları)
İmplant düzeyinde karşılaştırmalar, her bir implantın genel ortalamaları (Sınıf 1A defektlerinde bukkal yüzeylerin ölçüm ortalamaları ve Sınıf 1B defektlerinde bukkal, mezial ve distal yüzey ölçüm ortalamaları) karşılaştırılarak gerçekleştirildi. Buna göre en etkili dekontaminasyon 1A defektlerde AA ile elde edildi (0.19 ± 0.02) (p < 0.001). Bu grubu AA-1B (0.29 ± 0.04), PI-1B (0.38 ± 0.04) ve PI-1A (0.43 ± 0.03) izledi. En az dekontaminasyon TIT-1A (0.53 ± 0.03) ve TIT-1B (0.56 ± 0.03) gruplarında tespit edildi. Titanyum küret grupları arasında anlamlı fark bulunmazken (1A-1B), diğer tüm grupların ikili karşılaştırmaları istatistiksel olarak anlamlıdır (p < 0.001; Tablo 1; Şekil 3).
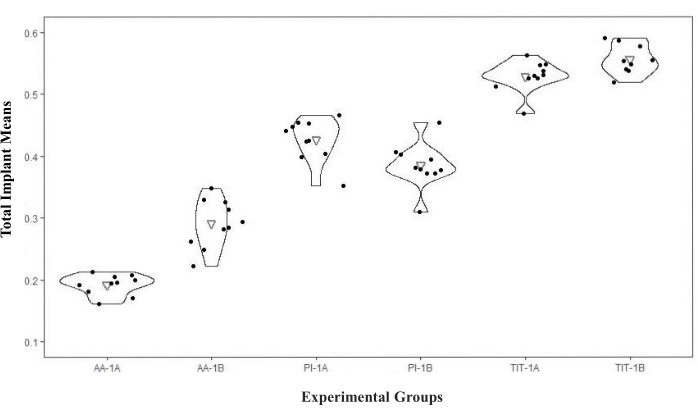
Şekil 3: Deney gruplarının keman grafiği ve toplam implant ortalamaları. Kısaltmalar: AA = Hava Aşındırıcı, PI = PEEK ucu, TIT = Titanyum küret. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
Dekontaminasyon sonrası implant yüzey seviyesi karşılaştırmaları
İmplant düzeyindeki karşılaştırmalara benzer şekilde, hava aşındırıcı (AA), PI ve TIT ile karşılaştırıldığında tüm numunelerin (1A + 1B) bukkal yüzeylerinde istatistiksel olarak en etkili dekontaminasyonu sağlamıştır (p < 0.001). Bukkal yüzeylerde PI ile TİT'e göre daha iyi dekontaminasyon sağlanırken (p < 0.001), TIT 1A ve 1B bukkal grupları arasında fark saptanmadı.
1B defektlerinin mezial yüzeylerinde en etkili dekontaminasyon PI ve TİT ile karşılaştırıldığında AA ile sağlandı ve tüm gruplar arasındaki fark istatistiksel olarak anlamlıydı (p < 0.001). AA ve PI protokollerinin 1B defektlerinin distal yüzeyleri üzerinde benzer şekilde etkili olduğu bulundu (p ˃ 0.05) ve her iki grubun da TİT grubuna göre daha etkili olduğu gözlendi (p < 0.001; Tablo 1).
Dekontaminasyon sonrası tedavi protokolü düzeyinde karşılaştırmalar
Defekt gruplarından bağımsız olarak, tedavi protokolü karşılaştırmaları, AA'nın (0.24 ± 0.06) implant yüzeyi dekontaminasyonunda PI ve TIT'e kıyasla istatistiksel olarak anlamlı derecede daha etkili olduğunu gösterdi (p < 0.001). Ek olarak, PI ölçümleri (0.41 ± 0.04) TIT'den (0.55 ± 0.03; p < 0.001; Tablo 1).
Dekontaminasyon sonrası kusur seviyesi karşılaştırmaları
Tedavi protokollerinden bağımsız olarak, defekt tipi karşılaştırmaları, Sınıf 1A ve Sınıf 1B peri-implantitis defekt tiplerinin benzer dekontaminasyon etkinliği ile sonuçlandığını gösterdi (p ˃ 0.388). Öte yandan, Sınıf 1B defektlerde tedavi protokollerinin etkinliğinin bukkal yüzeylerde (0.34 ± 0.17) distal yüzeylere göre istatistiksel olarak daha iyi olduğu gözlendi (p ˃ 0.388; Tablo 1).
Tablo 1: Kalan mürekkep yüzdesi ve dekontaminasyon sonuçlarının tedavi gruplarına ve kusur tiplerine göre karşılaştırılması. Bu Tabloyu indirmek için lütfen buraya tıklayın.
Dekontaminasyon sonrası fotografik analiz açılarının karşılaştırılması
Frontal 90° (F-90°), apikal 30° (A-30°) ve koronal 30° (C-30°) fotoğraflarının ölçümleri karşılaştırıldığında, A-30° ile C-30° arasında gruplar arasında fark tespit edilemedi. AA grubunda bukkal yüzeylerin C-30° ve F-90° fotoğraf örneklerinde, PI grubunda A-30° ve C-30° fotoğraf örneklerinde ve TİT grubunda bukkal ve mezial F-90° fotoğraf örneklerinde daha etkili dekontaminasyon kaydedildi (Tablo 2).
Tablo 2: Kalan mürekkep yüzdesi ve dekontaminasyon sonuçlarının fotoğraf açılarına göre karşılaştırılması. Bu Tabloyu indirmek için lütfen buraya tıklayın.
Dekontaminasyon sonrası SEM sonuçları ve EDS analizi
Temsili örneklerin SEM analizi, tüm tedavi modalitelerinin implant yüzeyini etkilediğini gösterdi. AA tedavisi, defekt grubundan bağımsız olarak, bukkal bölgelerdeki hem mikro iplik hem de makro iplik yapılarında ihmal edilebilir değişikliklere neden oldu (Şekil 4, Şekil 5). Bununla birlikte, 1B defekt grubunun mezial ve distal bölgelerinde, bukkal alana kıyasla ipliklerin altında daha fazla mürekkep kalıntısı bulundu (Şekil 5). Ek olarak, 1B kusur grubunun bukkal mikro iplik bölgesinde bir toz partikülü gözlendi (Şekil 6). Plastik/karbon PEEK ultrasonik uç, kusur grubundan bağımsız olarak, AA yöntemine kıyasla bukkal bölgedeki topografik yapının hafif ila orta derecede düzleşmesine neden oldu. Ayrıca, PEEK grubunda, özellikle mikro iplikler arasında kalan mürekkep kalıntıları nedeniyle, pürüzlü yapıdan farklı, daha bulanık ve delikli bir görünüm gözlenmiştir (Şekil 4, Şekil 5). Bununla birlikte, PEEK tedavisi, 1B defekt grubunun mezial ve distal bölgelerinde 1000x ve 5000x büyütmelerde AA'ya benzer sonuçlar vermiştir (Şekil 5). Ek olarak, PEEK grubunda herhangi bir yabancı cisim bulunamadı. Öte yandan, titanyum küretler diğer yöntemlere kıyasla yüzeyde büyük değişikliklere neden oldu. 1A defekt grubunda, kötü dekontaminasyon nedeniyle bukkal alandaki mikro iplik yapısında pürüzlü yapı ayırt edilememiştir (Şekil 4). Diğer bölgelerde düzleşme ve uzunlamasına/yatay çizikler tespit edildi (Şekil 4, Şekil 5). 1B defekt grubunun mezial ve distal bölgelerinde pürüzlü yapı kaybolmuş ve çizik sayısı artmıştır (Şekil 5). Ek olarak, steril referans implantın bir element analizi (EDS) yapıldı ve %99.2 titanyum içeriği ortaya çıktı (Şekil 7). Diğer gruplardaki kayda değer yapılar (kara delikler) ve tamamen mürekkeple kaplı işlenmemiş implant yüzeyi üzerinde de element analizi yapıldı ve muhtemelen mürekkebin buharlaşması nedeniyle bu alanlarda karbon baskın bir sonuç gösterdi (Şekil 8 A-C).

Şekil 4: Sınıf 1A defekt grubuna ait implant örneklerinin SEM görüntüleri. (A) 1A bukkal defektin mikro ipliğinin 100x, 1000x, 5000x büyütmeli görüntüleri. (B) 1A bukkal kusurun makro ipliğinin 100x, 1000x, 5000x büyütmeli görüntüleri. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 5: Sınıf 1B defekt grubuna ait implant örneklerinin SEM görüntüleri. (A) 1B bukkal defektin mikro ipliğinin 100x, 1000x, 5000x büyütme oranındaki görüntüler. (B) 1B bukkal kusurun makro ipliğinin 100x, 1000x ve 5000x büyütme oranındaki görüntüler. (C) 1B kusurunun mesiyal bölgesinin 100x, 1000x, 5000x büyütme görüntüleri. (D) 1B defektinin distal bölgesinin 100x, 1000x, 5000x büyütme oranındaki görüntüler. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 6: İmplant yaka bölgesinde tanınan eritritol tozu partikülü görüntüsü. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 7: Steril ve tedavi edilmemiş referans implant numunesinin EDS analizi. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 8: EDS analizi. (A) Mürekkep kaplı işlenmemiş bir implant numunesinin EDS analizi. (B) PEEK grubundan (grup 4) alınan implant örneğinin EDS analizi. (C) Titanyum küretten alınan implant örneğinin EDS analizi. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
Tartışmalar
Peri-implant hastalığından etkilenen dental implantların in vitro yüzey analizi metodolojisi, implantın pürüzlü yüzeylerinde meydana gelen patojenik mekanizmaların enflamatuar ve bakteriyel doğası nedeniyle her zaman zor olmuştur. Numune materyali seçimi, yüzeydeki biyofilmi taklit etme, peri-implantitis defekt tipinin seçilmesi, in vitro prosedürler sırasında klinik koşulların temsil edilmesi, dekontaminasyon prosedürlerinin varyasyonları ve dekontaminasyon miktarını belirleme yöntemleri ve prosedürlerin implant yüzeyinin pürüzlülüğü üzerindeki etkileri çeşitli endişeleri içerir. Her implant markası, metal türü (titanyum, zirkonyum), yüzey pürüzlülüğü özellikleri, yüzey serbest enerjisi, ıslanabilirlik, iplik derinliği, genişliği ve uzunlukları gibi benzersiz yüzey özelliklerine sahiptir ve bunların tümü dekontaminasyon protokollerinin etkinliği üzerinde doğrudan bir etkiye sahiptir. Bu endişenin üstesinden gelmek için, bazı çalışmalarda implantlar yerine lekeli veya kontamine diskler kullanılmıştır. Bununla birlikte, bakteriyel biyofilmi düz bir yüzeyden (disk) vida tipi bir özelliğe (implant) karşı çıkarma yeteneği, gerçek klinik durumu ortaya çıkarmayacaktır16,20. Literatürde farklı implant markalarının dekontaminasyon etkinliği değerlendirilmiş olmasına rağmen21 bu çalışmada standart ve üst düzey özelliklere sahip implantlar kullanılmıştır.
Bu çalışmada kullanılan kalıcı mürekkep modeli, implantlar 13,14,15,16,17,19,22 üzerindeki biyofilmi taklit etmek için en yaygın yöntemdir. Bununla birlikte, mürekkep kullanmak, operatör tarafından kolayca görülebildiği için önyargıyı temsil edebilir ve bu da klinik koşullarla çelişir. Ek olarak, bu simüle edilmiş biyofilm, implant yüzeyine doğal biyofilmlerle aynı şekilde yapışmaz ve kalsifiye edilmez, bu da fiziksel debridmanı gerçek klinik ortamlardan daha kolay hale getirir. İmplant yüzeyinin yapay diş taşı23 ile kaplanması bunun için bir çözüm olabilir, ancak tek tip ve eşit bir diş taşı kalınlığı elde etmek yine de bir sınırlama olabilir. Birkaç çalışmada doğrudan canlı periodontal patojenik bakteriler kullanılmıştır in vivo24 veya in vitro titanyum yüzeyinin in vitro 25 kontaminasyonu. Peri-implantitis kompleks bir multibakteriyel hastalık olduğundan, yüzeyde mono-bakteri biyofilmleri veya multi-bakteri biyofilmlerinin kullanılması dekontaminasyon prosedürlerinin sonuçlarını etkileyebilir26. Ayrıca, bakterilerin farklı implant yüzey materyallerine (zirkonya, titanyum) yapışma afinitesi, yüzey pürüzlülüğü ve yüzeysiz enerji nedeniyle farklılık gösterebilir26. Bu sınırlamalar dahilinde, mürekkep boyama yöntemi, mürekkep kalıntılarının doğrudan dijital olarak ölçülmesi ve dekontaminasyon yöntemleri arasında kantitatif karşılaştırmaların sağlanması gibi çeşitli avantajlar sağlar.
Peri-implantitis defekt tipinin tipi ve defekt duvarlarının varlığının mekanik debridman protokollerinin etkisini etkilediği bildirilmiştir 15,18,27. Daha önceki in vitro çalışmalarda çeşitli açılanmalara sahip suprakrestal veya çevresel defektler kullanılmıştır15,28. Bu kusur modelleriyle ilgili temel sorun, enstrümantasyon sırasında implant yüzeyine erişimin tüm alanlarda aynı olmasıdır; Ancak, bu klinik kusurları yansıtmaz. Bu çalışmada peri-implantitis defektlerinin en sık görülen tipleri olan Sınıf 1A ve Sınıf 1B intraosseöz defektler18 kullanıldı. Ek olarak, mevcut çalışmada, klinik olarak protez üst yapının çıkarıldığı ve peri-implantitis defektlerinin doğrudan görüşü için mukoperiosteal fleplerin yükseltildiği EFP kılavuzları5 tarafından önerildiği gibi cerrahi ortamlar simüle edildi.
İmplant yüzeyi dekontaminasyon protokollerinin başarısı, implant ipliklerinin pürüzlü iç yüzeylerine erişim yeteneklerine bağlıdır. Bugüne kadar, çeşitli derecelerde başarı ile çeşitli dekontaminasyon yöntemleri araştırılmıştır. Bunlar arasında hava aşındırıcı sistemler, titanyum fırçalar ve küretlerin en etkili tedavi protokolleri olduğu bildirilmiştir8. Bununla birlikte, tüm bu tedaviler, doku ve oksit tabakası kalınlığındaki değişiklikler gibi implant yüzey pürüzlülüğünde değişikliklere neden olur. Bu mikro-topografik değişikliklerin sonunda olumsuz klinik etkileri olabilir. Bu nedenle, implant yüzeyleri için en uygun dekontaminasyon yöntemi henüz belirlenmemiştir. Spesifik defekt tipi ve çene modeli simülasyonu nedeniyle mevcut sonuçların önceki çalışmalarla doğrudan karşılaştırılması mümkün olmasa da, intraosseöz bileşendeki benzerlikler not edilebilir. Bu çalışmanın bulguları literatür ile uyumlu olup, AA'nın implant yüzeyine 90° açıyla dik olarak uygulandığı bukkal yüzeylerde daha etkili olduğunu, intraosseöz komponentin açılı uygulama gerektirdiği mesial ve distal yüzeylerde etkinliğinin azaldığını göstermektedir 14,16,17,29. Ek olarak, bu, Petersilka tarafından 201130'da tarif edilen ve basınçlı toz ve su prensibi ile çalışan AA'nın yüzeylere uygulandığında ortaya çıkan sekme etkisi ile açıklanabilir.
AA prosedürlerinde kullanılan toz tipinin etkinliği birçok çalışmada araştırılmıştır. Glisin, bugüne kadar klinik ve in vitro araştırmalarda en yaygın kullanılan toz iken, diğer türler arasında sodyum bikarbonat, kalsiyum bikarbonat, trikalsiyum fosfat ve eritritol7 bulunur. Bununla birlikte, daha büyük partikül boyutlarına sahip tozların, implant yüzeyinde daha etkili bir dekontaminasyon sağlarken, aynı zamanda makro yapısal değişiklikler ve artan çizikler gibi daha fazla yüzey değişikliklerine neden olduğu gözlemlenmiştir 13,31. Pujarern ve ark.9 tarafından yakın zamanda yapılan bir in vitro çalışma, implant yüzeylerindeki eritritol ve sodyum bikarbonat tozları arasında biyofilm dekontaminasyon etkinliğinde bir fark göstermedi. Ayrıca, daha küçük parçacıkların hava-su karışımında daha kolay çözündüğü, yüzey hasarı riskini azalttığı ve daha büyük parçacıklara kıyasla dar diş boşluklarına nüfuz etmeyi kolaylaştırdığı bildirilmiştir13. Hava abrasiv sistemlerin, implant yüzeylerinden biyofilm uzaklaştırmada etkili bir yöntem olması, minimal yüzey hasarına neden olması, yumuşak doku travmasını azaltması ve ameliyat sonrası hasta morbiditesinin düşük olması gibi avantajlarına rağmen, bazı sınırlamalara dikkat edilmelidir. Bunlar, kalsifiye birikintilerin veya iyi yapışmış bakteri birikimlerinin32 çıkarılmasındaki zorlukları, posterior ve lingual/palatal bölgelerde uygun açıların elde edilmesinde zorluk ve işlem sırasında basınçlı hava nedeniyle deri altı amfizem riskiniiçerir 33. Bu nedenle, hava aşındırıcı sistemlerin rutin kullanımını desteklemek için daha fazla kanıt gereklidir5.
Hava aşındırıcı toz sistemlerinin kullanılamadığı durumlarda, titanyum fırçalar, metal küretler veya ultrasonik uçlar gibi alternatifler tercih edilebilir veya yardımcı tedavi olarak gerekli olabilir21. Bununla birlikte, mekanik dekontaminasyon için kullanılan metalik aletler, titanyum yüzeyi çizerek daha pürüzlü bir yüzey oluşturabilir ve potansiyel olarak mikrobiyal yapışmayı ve plak birikimini teşvik edebilir. Bu nedenle, Teflon, plastik ve PEEK kaplı aletler gibi alternatifler kullanılmalı ve daha fazla araştırılmalıdır. Bu çalışmada, implant yüzeyleri için özel olarak tasarlanmış, yakın zamanda geliştirilen bir ultrasonik PEEK / karbon ucun etkinliği değerlendirildi. Metodolojimizle tutarlı son çalışmalarda, sonik ve ultrasonik PEEK plastik uçların yanı sıra hava aşındırıcı toz sistemleri, farklı implant yüzeylerinde en iyi sonuçları elde etmiştir12,34. Mevcut çalışmada kullanılan PI MAX ucu, %30 karbon içermesi ve daha ince, daha esnek bir tasarıma sahip olması bakımından üreticinin önceki PEEK ucundan farklıdır. Bu yeni tasarımla ilgili mevcut sınırlı veriler, mevcut çalışmada en çok çalışılan iki yöntemle (hava aşındırması ve titanyum küretler) karşılaştırılmasının önemini vurgulamaktadır.
Günümüzde yaygın olarak kullanılan ve periodontal tedavilerde mekanik debridman için altın standart olarak kabul edilen metalik küretler de dental implantlar çevresinde yaygın olarak kullanılmaktadır. Birçok üretici, implant yüzeyine zarar vermeden biyofilm ve diğer kalıntıları gidermek için özel olarak tasarlanmış titanyum küretler geliştirmiştir35. İn vitro simülasyonlar, tekrarlanan mekanik enstrümantasyonun implant yüzey pürüzlülüğünde kümülatif değişikliklere yol açmadığı sonucuna varmıştır36. Bununla birlikte, bazı durumlarda, titanyum küretler sertleşmiş veya mineralize tortuların giderilmesinde sınırlı etkinliğe sahip olabilir. Ek olarak, manuel titanyum küretlerle temizlik yapmak zaman alıcı olabilir ve operatörün beceri düzeyine37 bağlı olarak değişkenliğe tabi olabilir. Mevcut kanıtlara dayanarak, implant mikro ve makroskopik tasarımlarının yüksek heterojenliği nedeniyle bu çalışmaların bulgularını klinik uygulamaya dönüştürmek zordur.
Yerleştirilen çok sayıda dental implant nedeniyle peri-implant hastalık prevalansının artması, kontamine yüzeyleri tedavi etmek için kanıta dayalı verilerle desteklenen öngörülebilir bir yaklaşım gerektirmektedir. Dekontaminasyon yöntemleri, en yaygın olarak kullanılan implant yüzeylerinin osseointegrasyonu destekleyen yüksek derecede pürüzlülük sergilediğini ve bakteriyel biyofilmin miktarının belirlenmesi ve ardından ortadan kaldırılmasının önemli yüzey hasarına neden olmadan standartlaştırılması gerektiğini dikkate almalıdır8. Dental materyallerin nano topografyasını ve implant yüzeylerinin pürüzlülüğünü değerlendirmek için kullanılan en yaygın in vitro yöntemler, kantitatif analiz için mekanik ve 3D optik (temaslı ve temassız) profilometri ve kalitatif değerlendirme için taramalı elektron mikroskobudur (SEM) 12,38,40. İmplantların yüzey pürüzlülüğünün ölçülmesinin ve araştırılmasının karmaşıklığı, kesin bir görünür model olmaksızın boşlukların ve kusurların varlığından kaynaklanmaktadır41.
Mevcut çalışmanın SEM bulguları, AA işleminin hafif yüzey değişikliklerine neden olduğu 17,31 önceki bulgularla uyumluyken, titanyum küretler23 ile yüzey topografyasında önemli bir düzleşme gözlenmiştir. SEM, daha büyük bir alan derinliği ve daha fazla büyütme ile daha geniş bir görüş alanı kullanarak dinamik bir aralık sağlar. Topografik doku ve malzeme kontrastı gibi yüzey detayları nanometre çözünürlüğe kadar değerlendirilebilir. Ancak SEM tek başına kantitatif bir teknik değildir ve profilometrinin en yaygın yöntem olduğu diğer kantitatif tekniklerle birleştirildiğinde daha güvenilir veriler elde edilebilir. Son zamanlarda, doğrudan SEM kantitatif ölçümleri için 3D stereo-fotogrametri42 ve yenilikçi yapay zeka tabanlı görüntü analiz yazılımı43 kullanılmıştır.
Sonuç olarak, bulgular, sınırlılıklar dahilinde, klinik uygulamalar için dekontaminasyon yönteminin seçiminin peri-implantitis tedavisinin nihai hedefine dayalı olarak belirlenmesi gerektiğini göstermektedir. Bu doğrultuda, hava aşındırıcı eritritol toz sistemi, rejeneratif tedavilerde implant yüzeyi için daha nazik bir seçenek gibi görünüp daha etkin erişilebilirlik ve dekontaminasyon sağlarken, implant çevresi yumuşak doku granülasyonlarının debridmanı için ve implant yüzeyinin ağız ortamına açıkta bırakıldığı rezektif tedavilerde yüzeyi düzleştiren titanyum küretler önerilebilir. Ultrasonik PEEK uçlar, implant ipliği tepeleri ve pürüzsüz transmukozal yüzeyler üzerindeki kalsifiye birikintilerin giderilmesi için de önerilir. Mevcut dekontaminasyon yöntemlerinin tek başına kullanılması yerine birlikte kullanılması en etkili yaklaşımı temsil edebilir.
Açıklamalar
Yazarların açıklanacak herhangi bir çıkar çatışması yoktur.
Teşekkürler
Çalışmada kullanılan implantlar Dentsply Sirona tarafından desteklenmiştir.
Malzemeler
| Name | Company | Catalog Number | Comments |
| 3D Printer | DentaFab, Istanbul, Turkey | To produce experimental periimplantitis defects | |
| 3D Printing Resin | Alias, Istanbul,Turkey | To produce experimental periimplantitis models | |
| 3D Scanner | DOF Inc. EDGE, Seoul ,Republic of Korea | Used to scan the dental phantom model | |
| Air Abrasive system | AIRFLOW Plus PowderE.M.S., Electro Medical Systems S.A., Nyon, Switzerland | Used to decontaminate implant surface | |
| CAD/CAM Software | Exocad 3.2 Elefsina | To produce experimental periimplantitis defects | |
| Camera | Canon EOS 70D, Japan | In order to obtain photographic records of implants | |
| Dental implant | DS PrimeTaper, Dentsply Sirona, Hanau, Germany | ||
| Light-Curing Unit | Solidilite V, Japan | Used to curing experimental models in laboratory | |
| Permanent ink | Edding, Germany | Used to stain the implant surface for mimicking biofilm | |
| Physiodispenser | Dentsply Sirona, Hanau, Germany | To place the implants in the experimental models | |
| SEM Device | FEI QUANTA FEG 250 FEI Technologies Inc. (Oregon, United States | Used to analyze topograhic changes on the implant surface | |
| Surgical implant set | Dentsply Sirona, Hanau, Germany | To place the implants in the experimental models | |
| Titanium Currette | Langer ½ Titanium Currette, Hu-Friedy, Chicago, IL, USA | Used to decontaminate implant surface | |
| Ultrasonic PEEK Tip | PI-MAX Implant Scaler, E.M.S., Electro Medical Systems S.A., Nyon, Switzerland | Used to decontaminate implant surface |
Referanslar
- Buser, D., et al. 10-year survival and success rates of 511 titanium implants with a sandblasted and acid-etched surface: A retrospective study in 303 partially edentulous patients. Clin Implant Dent Relat Res. 14 (6), 839-851 (2012).
- Berglundh, T., et al. Peri-implant diseases and conditions: Consensus report of workgroup 4 of the 2017 World workshop on the classification of periodontal and peri-implant diseases and conditions. J Clin Periodontol. 45, S286-S291 (2018).
- Diaz, P., Gonzalo, E., Villagra, L. J. G., Miegimolle, B., Suarez, M. J. What is the prevalence of peri-implantitis? A systematic review and meta-analysis. BMC Oral Health. 22 (1), 1-13 (2022).
- Herrera, D., et al. Prevention and treatment of peri-implant diseases—The EFP S3 level clinical practice guideline. J Clin Periodontol. 50 (S26), 4-76 (2023).
- Heitz-Mayfield, L., Mombelli, A. The therapy of peri-implantitis: a systematic review. Int J Oral Maxillofac Implants. 29 Suppl, 325-345 (2014).
- Heitz-Mayfield, L. J. A., Heitz, F., Lang, N. P. Implant disease risk assessment IDRA–a tool for preventing peri-implant disease. Clin Oral Implants Res. 31 (4), 397-403 (2020).
- Monje, A., Cha, J. K. Strategies for implant surface decontamination in peri-implantitis therapy. Int J Oral Implantol. 15 (3), 213-248 (2022).
- Francis, S., Iaculli, F., Perrotti, V., Piattelli, A., Quaranta, A. Titanium surface decontamination: A systematic review of in vitro comparative studies. Int J Oral Maxillofac Implants. 37 (1), 76-84 (2022).
- Pujarern, P., et al. Efficacy of biofilm removal on the dental implant surface by sodium bicarbonate and erythritol powder airflow system. Eur J Dent. 18 (4), 1022-1029 (2024).
- Polizzi, E., D’orto, B., Tomasi, S., Tetè, G. A micromorphological/microbiological pilot study assessing three methods for the maintenance of the implant patient. Clin Exp Dent Res. 7 (2), 156-162 (2021).
- Monje, A., et al. Morphology and severity of peri-implantitis bone defects. Clin Implant Dent Relat Res. 21 (4), 635-643 (2019).
- Khan, S. N., Koldsland, O. C., Tiainen, H., Hjortsjö, C. Anatomical three-dimensional model with peri-implant defect for in vitro assessment of dental implant decontamination. Clin Exp Dent Res. 10 (1), e841-e848 (2024).
- Matsubara, V. H., et al. Cleaning potential of different air abrasive powders and their impact on implant surface roughness. Clin Implant Dent Relat Res. 22 (1), 96-104 (2020).
- Ronay, V., Merlini, A., Attin, T., Schmidlin, P. R., Sahrmann, P. In vitro cleaning potential of three implant debridement methods. Simulation of the non-surgical approach. Clin Oral Implants Res. 28 (2), 151-155 (2017).
- Sahrmann, P., et al. In vitro cleaning potential of three different implant debridement methods. Clin Oral Implants Res. 26 (3), 314-319 (2015).
- Hart, I., Wells, C., Tsigarida, A., Bezerra, B. Effectiveness of mechanical and chemical decontamination methods for the treatment of dental implant surfaces affected by peri-implantitis: A systematic review and meta-analysis. Clin Exp Dent Res. 10 (1), e839-e844 (2024).
- Korello, K., Eickholz, P., Zuhr, O., Ratka, C., Petsos, H. In vitro efficacy of non-surgical and surgical implant surface decontamination methods in three different defect configurations in the presence or absence of a suprastructure. Clin Implant Dent Relat Res. 25 (3), 549-563 (2023).
- Luengo, F., et al. In vitro effect of different implant decontamination methods in three intraosseous defect configurations. Clin Oral Implants Res. 33 (11), 1087-1097 (2022).
- Keim, D., et al. In vitro efficacy of three different implant surface decontamination methods in three different defect configurations. Clin Oral Implants Res. 30 (6), 550-558 (2019).
- Al-Hashedi, A. A., Laurenti, M., Benhamou, V., Tamimi, F. Decontamination of titanium implants using physical methods. Clin Oral Implants Res. 28 (8), 1013-1021 (2017).
- Sanz-Martín, I., et al. Significance of implant design on the efficacy of different peri-implantitis decontamination protocols. Clin Oral Investig. 25 (6), 3589-3597 (2021).
- Mensi, M. Comparison between four different implant surface debridement methods: an in vitro experimental study. Minerva Stomatol. 69 (5), 286-294 (2020).
- Sirinirund, B., Garaicoa-Pazmino, C., Wang, H. L. Effects of mechanical instrumentation with commercially available instruments used in supportive peri-implant therapy: An in vitro study. Int J Oral Maxillofac Implants. 34 (6), 1370-1378 (2019).
- Wiessner, A., et al. In vivo biofilm formation on novel PEEK, titanium, and zirconia implant abutment materials. Int J Mol Sci. 24 (2), 1779 (2023).
- Cai, Z., et al. Disinfect Porphyromonas gingivalis biofilm on titanium surface with combined application of chlorhexidine and antimicrobial photodynamic therapy. Photochem Photobiol. 95 (3), 839-845 (2019).
- Azizi, B., et al. Antimicrobial efficacy of photodynamic therapy and light-activated disinfection on contaminated zirconia implants: An in vitro study. Photodiagnosis Photodyn Ther. 21, 328-333 (2018).
- Sahrmann, V., et al. In vitro cleaning potential of three different implant debridement methods. Clin Oral Impl Res. 26 (3), 314-319 (2015).
- Tuchscheerer, V., et al. In vitro surgical and non-surgical air-polishing efficacy for implant surface decontamination in three different defect configurations. Clin Oral Investig. 25 (4), 1743-1754 (2021).
- Iatrou, P., et al. In vitro efficacy of three different nonsurgical implant surface decontamination methods in three different defect configurations. Int J Oral Maxillofac Implants. 36 (2), 271-280 (2021).
- Petersilka, G. J. Subgingival air-polishing in the treatment of periodontal biofilm infections. Periodontol 2000. 55 (1), 124-142 (2011).
- Giffi, R., et al. The efficacy of different implant surface decontamination methods using spectrophotometric analysis: an in vitro study. J Periodontal Implant Sci. 53 (4), 295 (2023).
- Laleman, I., et al. Subgingival debridement: end point, methods and how often. Periodontol 2000. 75 (1), 189-204 (2017).
- Regidor, E., Derks, J., Ortiz-Vigón, A. The use of air abrasive devices for implant surface decontamination. Perio Clinica. 27 (2), 23-38 (2023).
- Khan, S. N., et al. The decontamination effect of an oscillating chitosan brush compared with an ultrasonic PEEK-tip: An in study using a dynamic biofilm model. Clin Oral Implants Res. 36 (1), 73-81 (2025).
- Louropoulou, A., Slot, D. E., van der Weijden, F. The effects of mechanical instruments on contaminated titanium dental implant surfaces: a systematic review. Clin Oral Implants Res. 25 (10), 1149-1160 (2014).
- Lang, M. S., Cerutis, R., Miyamoto, T., Nunn, E. Cell attachment following instrumentation with titanium and plastic instruments, diode laser, and titanium brush on titanium, titanium-zirconium, and zirconia surfaces. Int J Oral M axillofac Implants. 31, 799-806 (2016).
- Harrel, S. K., Wilson, T. G., Pandya, M., Diekwisch, T. G. H. Titanium particles generated during ultrasonic scaling of implants. J Periodontol. 90 (3), 241-246 (2019).
- Schwarz, F., Nuesry, E., Bieling, K., Herten, M., Becker, J. Influence of an Erbium, Chromium-Doped Yttrium, Scandium, Gallium, and Garnet (Er,Cr:YSGG) laser on the reestablishment of the biocompatibility of contaminated Titanium implant surfaces. J Periodontol. 77 (11), 1820-1827 (2006).
- Hakki, S. S., Tatar, G., Dundar, N., Demiralp, B. The effect of different cleaning methods on the surface and temperature of failed titanium implants: an in vitro study. Lasers Med Sci. 32 (3), 563-571 (2017).
- Chegeni, E., Espanã-Tost, A., Figueiredo, R., Valmaseda-Castellón, E., Arnabat-Domínguez, J. Effect of an Er,Cr:YSGG laser on the surface of implants: A descriptive comparative study of 3 different tips and pulse energies. Dent J. 8 (4), 109-118 (2020).
- Mei, L., Guan, G. Profilometry and atomic force microscopy for surface characterization. Nano TransMed. 2 (1), e9130017-e9130024 (2023).
- Martelo, J. B., Andersson, M., Liguori, C., Lundgren, J. Three-dimensional scanning electron microscopy used as a profilometer for the surface characterization of polyethylene-coated paperboard. Nord Pulp Paper Res J. 36 (2), 276-283 (2021).
- Kimoto, K., et al. Unsupervised machine learning combined with 4D scanning transmission electron microscopy for bimodal nanostructural analysis. Sci Rep. 14 (1), 2901-2909 (2024).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır