Method Article
In vitro Avaliação dos efeitos dos lasers de Er, Cr: YSGG e diodo usados no cilindro de titânio
Neste Artigo
Resumo
Neste estudo, lasers de Er, Cr: YSGG e diodo aplicados separadamente na superfície plana de um total de 96 cilindros de titânio especialmente projetados. Um termopar colocado na outra superfície e a temperatura foi medida. Rugosidade superficial analisada por perfilômetro, MEV e AFM.
Resumo
As doenças peri-implantares são problemas significativos associados aos implantes dentários. O objetivo deste estudo foi avaliar a rugosidade superficial e as mudanças de temperatura quando lasers de diodo e ítrio-escândio-escândio-gálio-granada dopados com cromo (Er,Cr:YSGG) são aplicados em cilindros de titânio no tratamento de doenças peri-implantares não cirúrgicas. Um total de 13 grupos, incluindo o grupo controle, foram formados com lasers de diodo de 940 nm (0,8 W-1,3 W-1,8 W) e Er,Cr:YSGG (1,5 W-2,5 W-3,5 W) em 6 diferentes modos de potência, 20s/W e 40 s/W, e oito cilindros de titânio foram tratados em cada grupo. Durante o processo, as temperaturas inicial e final foram registradas com um termopar colocado na ranhura apical do cilindro. Após a aplicação, a rugosidade (Ra) de todos os discos foi medida por um perfilômetro. As superfícies foram escaneadas por microscópio eletrônico de varredura (MEV) e microscópio de força atômica (AFM) para exame de superfície bidimensional e tridimensional. Quando avaliadas as mudanças de temperatura dos cilindros de titânio durante a irradiação, os cilindros irradiados com laser de diodo por 40 s foram significativamente maiores do que aqueles irradiados por 20 s. Nos cilindros tratados com Er,Cr:YSGG, a temperatura diminuiu em algumas amostras e aumentou minimamente em algumas amostras. Os valores do perfilômetro (Ra) não foram estatisticamente significativos em termos de rugosidade para todos os grupos. No entanto, as imagens de MEV mostraram derretimento e aumento do número de microporos nas superfícies tratadas. Com as limitações deste estudo in vitro , a aplicação do Er,Cr:YSGG e do diodo pode ser considerada uma abordagem segura para o manejo da peri-implantite, particularmente em termos de segurança térmica. Embora a rugosidade da superfície permaneça inalterada, o uso desses lasers resultou em mudanças de fusão e microporos na topografia do cilindro de Ti. Para determinar como essas configurações de laser afetam a diminuição bacteriana e a osseointegração, são necessárias pesquisas adicionais.
Introdução
Os implantes dentários são uma opção de tratamento comumente aceita para a substituição de dentes perdidos 1,2. A mucosite peri-implantar e a peri-implantite são classificadas como doenças peri-implantares. A mucosite peri-implantar é restrita aos tecidos moles, e não há evidência de perda óssea, com exceção da remodelação óssea fisiológica. A peri-implantite é uma condição patológica que está associada à placa bacteriana e afeta os tecidos ao redor dos implantes dentários. Distingue-se pela inflamação da mucosa peri-implantar e a conseqüente perda crescente do osso de suporte3. O principal fator etiológico para o início e progressão do distúrbio é a ruptura do biofilme da placa peri-implantar4. Numerosos estudos sobre doenças peri-implantares indicam que a prevalência de mucosite peri-implantar (MPI) varia de 9,7% a 64,6%, enquanto a prevalência de peri-implantite (P) varia entre 4,7% e 45%5.
Embora o acúmulo de placa seja o principal fator etiológico que causa a peri-implantite, seu tratamento é complicado pelas diversas características topográficas dos implantes. A base do tratamento não cirúrgico da peri-implantite é o manejo da infecção por meio do desbridamento da superfície do implante e da eliminação do biofilme aderente para diminuir a carga bacteriana abaixo do limiar causador da doença 6,7. A complexa micro e macrotopografia das interfaces de titânio e a anatomia do defeito ósseo limitam a descontaminação da superfície. A eficácia de diferentes técnicas de descontaminação mecânica (curetas, dispositivos ultrassônicos, abrasão com pó de ar, escovas de titânio), química (ácido cítrico, clorexidina, antimicrobianos) e física (laser, terapia fotodinâmica) foi avaliada em combinação8. Pesquisas atuais sugerem que o uso combinado de técnicas de intervenção não cirúrgica para peri-implantite é mais eficaz do que o desbridamento sozinho9. A incorporação de agentes antimicrobianos químicos ou antibióticos locais/sistêmicos na terapia mecânica demonstrou eficácia significativa; no entanto, essas intervenções podem resultar em possíveis consequências adversas10. À medida que a tecnologia a laser avançou, os lasers odontológicos tornaram-se cada vez mais populares devido aos seus efeitos anti-infecciosos, desintoxicantes e fáceis de usar nas superfícies dos implantes10,11.
O pico de absorção, o modo operacional do dispositivo e as propriedades do tecido afetam o aumento de calor durante a irradiação do laser. Uma investigação pré-clínica crucial revelou que uma elevação da temperatura para 50 °C por 1 min causou danos vasculares, enquanto um aumento para 60 °C levou à cessação do fluxo sanguíneo e subsequente necrose óssea12. Uma investigação in vitro descobriu que, após apenas 10 s de irradiação com laser de diodo, as superfícies dos implantes podem atingir temperaturas superiores ao limite de segurança óssea (10 °C). A viabilidade óssea pode ser comprometida por um aumento de temperatura de apenas 10 °C13.
Numerosos estudos recentes se concentraram em examinar o impacto benéfico dos lasers neste domínio 14,15,16,17,18. Vários comprimentos de onda do laser demonstram um impacto antibacteriano significativo e segurança nas superfícies do implante quando os parâmetros apropriados são aplicados. Várias variáveis, incluindo intensidade, frequência e comprimento de onda, influenciam a eficácia dos tratamentos a laser. Vários estudos demonstraram o efeito bactericida de vários comprimentos de onda do laser, incluindo CO2, Er:YAG, Er,Cr:YSGG e vários lasers de diodo, o que nos permite identificar os efeitos benéficos de diferentes lasers no tratamento da peri-implantite. Aoki et al 19,20,21. concluíram de sua revisão que a aplicação de laser facilita a limpeza da superfície em tratamentos peri-implantares não cirúrgicos e cirúrgicos, incluindo terapia regenerativa, e promove a cicatrização ativando as células do tecido circundante22.
Os lasers de diodo têm a capacidade de exercer um efeito bactericida nas superfícies do implante sem afetar o padrão de superfície do implante. Quando se trata de tratar a peri-implantite, o laser de diodo pode ser o caminho a percorrer, pois promove a cicatrização dos tecidos periodontais 23,24,25.
Érbio, dopado com cromo: os lasers de ítrio, escândio, gálio, granada (Er,Cr:YSGG) apresentam propriedades eficazes para a eliminação do biofilme e a descontaminação das superfícies dos implantes11. Fortes efeitos bactericidas e propriedades de regeneração óssea foram demonstrados por lasers de érbio sem causar danos mecânicos graças às suas propriedades movidas a água11,14.
Há escassez de dados sobre as alterações causadas pela irradiação a laser em implantes de titânio. Além disso, uma metodologia definitiva para a irradiação de superfícies de titânio ainda não foi definida, englobando parâmetros do laser, como potência e tempo de aplicação. Estudos anteriores mostraram que a aplicação do laser16 de Er,Cr:YSGG não teve efeito sobre a mudança de temperatura, no entanto, os estudos de laser de diodo excederam13 e não ultrapassaram16,26 o valor crítico. Diferentes resultados do efeito do tratamento com laser no valor de Ra da superfície de titânio estão disponíveis na literatura18,27. A hipótese nula do estudo é que não haverá diferença entre os lasers Er, Cr: YSGG e os lasers de diodo em termos de mudança de temperatura e rugosidade das superfícies de titânio usando. Este estudo teve como objetivo determinar parâmetros operacionais seguros monitorando a rugosidade da superfície e as variações de temperatura em material de titânio usando lasers de Er, Cr:YSGG e diodo em várias configurações de tempo e potência. A avaliação da mudança de temperatura foi realizada com um termopar, a rugosidade da superfície foi avaliada usando um perfilômetro e as alterações da superfície foram analisadas através das técnicas de MEV e AFM.
Protocolo
NOTA: Os cilindros de titânio, fabricados com o mesmo material dos implantes convencionais e projetados para replicar a superfície do implante com a tecnologia SLA, apresentam uma altura de 10 mm e um diâmetro de 5 mm. Uma cavidade medindo 7 mm de profundidade e 3 mm de largura está localizada no centro dos cilindros (Fig. 2). A largura de 3 mm reduz para 1 mm no ponto mais profundo. Medir a rugosidade da superfície de implantes padrão com um perfilômetro não é viável. Foi possível avaliar a eficácia do laser aplicado em uma superfície plana de 5 mm de diâmetro na parte superior do cilindro de titânio projetado pelo fabricante, utilizando o mesmo material que simula a superfície do implante. Além disso, para medir as mudanças de temperatura a partir do centro do cilindro, foi criada uma ranhura de 7 mm de profundidade e 3 mm de largura a partir do centro da superfície inferior do cilindro de titânio em direção às profundidades do cilindro, onde a ponta do termopar será colocada. Essa ranhura permite a avaliação da mudança de temperatura da superfície tratada de dentro do cilindro, em vez de depender da superfície externa. Imagens tridimensionais foram obtidas analisando as superfícies planas de cilindros de titânio especialmente produzidos usando um microscópio de força atômica (AFM). Foram utilizados lasers de diodo de 940 nm (0,8 W28, 1,3 W29, 1,8 W30) e 2,780 nm Er,Cr:YSGG (1,5 W31, 2,5 W31, 3,5 W32) em três potências diferentes de acordo com as recomendações da empresa, e 12 grupos foram formados com tempo de aplicação de 20 s e 40 s cada. Após a aplicação, um grupo controle foi adicionado para avaliação da rugosidade. Um suporte com suporte para o dedo foi impresso a partir de uma impressora tridimensional para manter o cilindro de Ti estável durante a aplicação (Tabela de Materiais).
1. tamanho Da Amostra
- Calcule o tamanho da amostra usando a análise de poder do programa G*Power. O número mínimo de amostras para cada grupo foi determinado como n=8 amostras para mudança de temperatura com tamanho de efeito d: 0,6906, desvio padrão 16,8, potência: 0,80 e α: 0,05.
NOTA: Neste estudo, um laser Er,Cr:YSGG equipado com um laser de diodo de 940 nm com uma ponta de 300 μm de diâmetro (ponta e3) e uma ponta elástica RFPT5-14 de disparo de 360° (580 μm de diâmetro e 14 mm de comprimento) foi usado como sistema de laser (Figura 1).

Figura 1: Instrumentos e equipamentos utilizados. (A) Laser de diodo, (B) Laser Er,Cr:YSGG, (C) Ponta E3, (D) Ponta RPTF5-14. Clique aqui para ver uma versão maior desta figura.
2. Determinação dos grupos de trabalho
- Tome o Watt recomendado de lasers para aplicação na bolsa na mucosite peri-implantar como condição ideal de uso. Além disso, inclua um valor mais baixo e um valor mais alto nos grupos de estudo em relação ao Watt recomendado. Os valores usados aqui são 1,5 W e 3,5 W para Er,Cr:YSGG e 0,8 W e 1,8 W para o laser de diodo.
- Determine o tempo de aplicação como 20 s e 40 s para avaliar o efeito do tempo de operação na mudança de temperatura. Os grupos de estudo são mostrados na Tabela 1.
| Nome do grupo | Tipo de laser | Número de amostras (n) | Watt (W) | Tempo(s) |
| E1 | Er, Cr: YSGG | 8 | 1,5 W | 20 |
| E2 | 8 | 2,5 W | 20 | |
| E3 | 8 | 3,5 W | 20 | |
| E4 | 8 | 1,5 W | 40 | |
| E5 | 8 | 2,5 W | 40 | |
| E6 | 8 | 3,5 W | 40 | |
| D1 | Diodo | 8 | 0,8 W | 20 |
| D2 | 8 | 1,3 W | 20 | |
| D3 | 8 | 1,8 W | 20 | |
| D4 | 8 | 0,8 W | 40 | |
| D5 | 8 | 1,3 W | 40 | |
| D6 | 8 | 1,8 W | 40 | |
| C | Controle | 8 |
Tabela 1: Informações dos grupos de estudo.
3. Preparação da configuração experimental
- Com o programa Rhinoceros (gráficos e design 3D), projete um suporte cilíndrico em 3D com uma cavidade ligeiramente com um diâmetro de 10 mm e uma espessura de 5 mm.
- Abra o aplicativo. Desenhe um círculo de 10 mm de diâmetro. Reduza o círculo em 50% de um eixo para criar uma elipse. Pressione Extuder e levante a elipse na terceira dimensão.
- Desenhe um círculo novamente para apoiar os dedos. Levante o segundo círculo na terceira dimensão com a chave da extrusora. Faça a altura menor que o primeiro círculo.
- Faça um furo de 10 mm no desenho elíptico com o comando booleano. Para suporte a termopares, faça uma linha em forma de L com o comando Sweep 1 e crie a 3ª dimensão.
- Desenhe um quadrado, amplie-o na 3ª dimensão com o comando extrusor e crie a base. Depois de imprimir o desenho, aplique silicone ao redor do orifício por onde virá o cilindro de Ti e seque-o. Isso manterá o cilindro no lugar enquanto o laser está sendo aplicado.
- Leve uma sala fechada com ar condicionado a uma temperatura de 27 °C. Fixe o suporte no qual os cilindros serão fixados no meio de uma banheira de plástico com fita dupla-face.
NOTA: Insira o cilindro de Ti, esprema o ar na superfície. - Coloque o termopar do termômetro na parte oca do cilindro de Ti colocado em sua ranhura no suporte.
- Prepare um cronômetro para acompanhar o tempo de aplicação. Registre os graus pelo 3º observador e acompanhe o tempo com o cronômetro.
4. Procedimento experimental
- Durante a aplicação do laser, use óculos de proteção para segurança do profissional. Insira a ponta RPTF5-14 para laser Er, Cr: YSGG. Insira a ponta E3 para laser de diodo.
- Ligue o laser Er,Cr:YSGG. Selecione Modo Fechado Perio. Aplique lasers de 1,5 W, 2,5 W e 3,5 W por 20 s e 40 s cada. Existem 96 cilindros de Ti com laser aplicado. Irradie um cilindro de Ti com apenas um tipo de laser, um watt e uma vez.
- Ligue o laser de diodo. Selecione o modo de bolso Perio. Aplique laser de 0,8 W, 1,3 W e 1,8 W por 20 s e 40 s cada.
- Faça com que o 3º observador inicie o cronômetro quando o laser for iniciado. Avise-o quando o tempo acabar.
- Aplique a ponta do laser em um ângulo de 15° em relação à superfície, em contato, ziguezagueando por toda a superfície pelo tempo planejado.
- Observe os valores de temperatura inicial e final durante a aplicação. Subtraia o valor da temperatura inicial do valor da temperatura final. Calcule a mudança de temperatura.
NOTA: Observe os valores de mudança de temperatura para um total de 12 grupos, 6 grupos de laser de Er, Cr:YSGG e 6 de diodo. - Manter as amostras em sacos transparentes com os números dos grupos escritos neles.
5. Imagem bidimensional e tridimensional de materiais
- Realize análises de microscópio eletrônico de varredura (SEM) e microscópio de força atômica (AFM) para avaliar e demonstrar mudanças na morfologia da superfície do cilindro de Ti.
NOTA: O instrumento FEI Quanta FEG 250 foi usado. - Não revestir as amostras antes de serem colocadas no MEV. Existem 13 grupos, incluindo 1 grupo de controle, 6 grupos de laser de diodo e 6 grupos de laser Er, Cr: YSGG. Para o grupo de controle, não execute nenhum tratamento, apenas tire imagens de superfície por AFM e SEM.
- Selecione aleatoriamente um cilindro de cada um dos 13 grupos de estudo. Insira-os no dispositivo SEM. Observe o local na plataforma e o código de exemplo para evitar a mistura de exemplos.
- Coloque o cilindro de Ti no dispositivo SEM com a superfície plana para cima. Realize análises usando o modo de baixo vácuo. Ajuste a pressão da câmara para 60 Pa durante a análise.
- Quando o dispositivo estiver totalmente pronto, grave imagens com ampliação de 250x, 1000x e 5000x de um ponto aleatório na superfície plana. Repita este procedimento para todas as amostras.
NOTA: Quando o dispositivo SEM terminar de aspirar, ele estará pronto para a coleta de imagens. - Para medição de AFM, selecione aleatoriamente um cilindro de Ti de cada grupo de estudo. Realize a medição no modo de rosqueamento.
- Coloque o cilindro de Ti no instrumento AFM. Coloque a tampa superior de forma que a ponta do instrumento fique sobre a amostra. Verifique se a luz vermelha da janela do instrumento está na superfície a ser fotografada.
- Defina a tensão para 2. Aproxime a ponta da amostra com o botão Aterrissar automaticamente. Inicie a digitalização pressionando o botão Iniciar digitalização .
- Tire uma imagem digital de 5 μm x 5 μm para cada amostra e registre a uma taxa de varredura lenta (1 Hz). Registre imagens tiradas com o instrumento AFM das superfícies planas dos cilindros de Ti. O instrumento do AFM visualiza a áreade 25 μm 2.
6. Medição da rugosidade da superfície
NOTA: O dispositivo Surftest SJ 201, Mitutoyo, Tóquio, Japão, foi usado aqui.
- Defina a resolução do perfilômetro para 0,01 mm, o comprimento transversal para 3,0 mm e o diâmetro da ponta do pino de registro diamantado para 5 μm. Defina a velocidade de medição para 0.5 mm/s para determinar o valor Ra.
- Fixe o cilindro de Ti com um suporte, use o presel e fixe o cilindro de Ti segurando-o pela superfície lateral. Coloque a agulha do perfilômetro em contato com a superfície de Ti.
- Pressione o botão Iniciar. Salve o valor Ra encontrado. Repita a medição 5x em direções diferentes na superfície plana de cada cilindro (Figura 2). Para obter as várias direções, mova o cilindro de Ti em torno de si mesmo com a ajuda de uma pré-venda. Repita para todo o comprimento do cilindro de Ti.
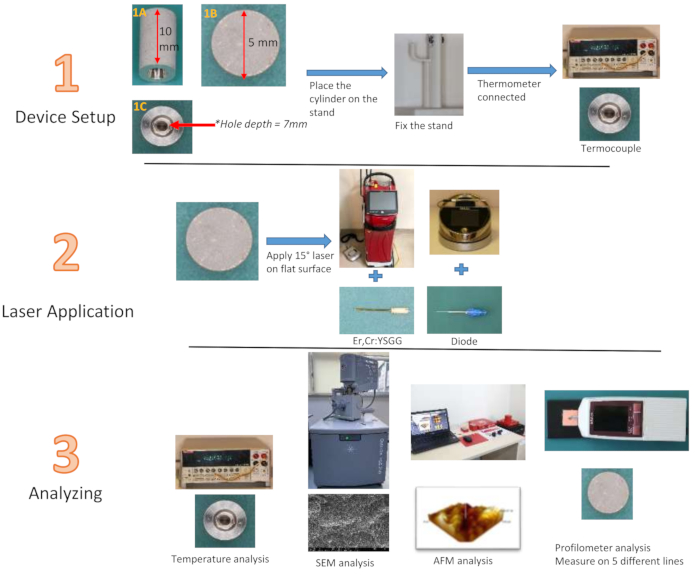
Figura 2: Fluxograma dos grupos de estudo. (1A) Vista lateral do cilindro Ti, (1B) vista superior, (1C) vista inferior Clique aqui para ver uma versão maior desta figura.
7. Análise estatística
- Realizar análise estatística utilizando o programa SPSS-Windows statistical package e aplicar os testes de Kruskal-Wallis e Mann-Whitney. Defina o nível de confiança estatística em 95% (α = 0,05).
Resultados
Na avaliação baseada nos tempos de aplicação de 20 segundos e 40 segundos, observou-se diferença estatisticamente significativa. Observou-se que a mudança de temperatura nas superfícies do cilindro de Ti aplicado a laser de 40 s foi maior do que na aplicação do laser de 20 s (p=0,037; Figura 3).
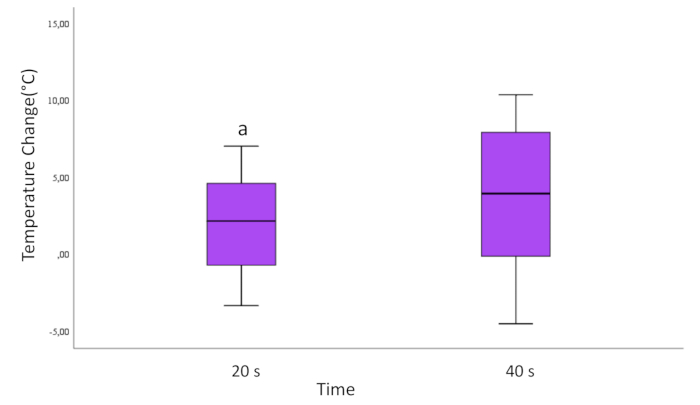
Figura 3: Mudança de temperatura de acordo com o tempo para todas as amostras. As linhas que sobem e descem da caixa mostram os valores mínimo e máximo dos dados. A linha horizontal dentro da caixa representa a mediana dos dados. Marcas redondas são discrepantes.
a=Diferença estatisticamente significativa em comparação com o grupo de 40 s. (pág<0,05)
Clique aqui para ver uma versão maior desta figura.
Analisamos a mudança de temperatura categorizando-os em dois grupos com base nos tipos de laser (Er, Cr: YSGG e diodo). Observou-se que a mudança de temperatura em cilindros de Ti usando um laser de diodo foi maior do que em cilindros que aplicam o laser de Er,Cr:YSGG. Os resultados são estatisticamente significativos (p=0,001; ver Figura 4). Na avaliação dos cilindros de Ti testados apenas para aplicação de laser de diodo, os resultados indicaram que a aplicação de laser de diodo de 40 s produziu resultados significativamente maiores em comparação com a aplicação de 20 s em todos os valores de Watt (p < 0,001; Figura 4). A linha vermelha dentro da caixa na figura indica o valor mediano. As barras na parte superior e inferior indicam os valores de temperatura máxima e mínima.

Figura 4: Variação de temperatura por tipos de laser e tempo para todas as amostras. As linhas que sobem e descem da caixa mostram os valores mínimo e máximo dos dados. A linha horizontal dentro da caixa representa a mediana dos dados. Marcas redondas são discrepantes.
a=Diferença estatisticamente significativa em comparação com o grupo de díodos. (pág<0,05)
b= Diferença estatisticamente significativa em comparação com o laser de diodo 40 s. (p<0,05)
Clique aqui para ver uma versão maior desta figura.
A última avaliação estatística da mudança de temperatura foi realizada com base no valor de Watt. Diferenças significativas foram observadas quando se investigaram apenas os valores de Watt (p < 0,001) e Watt-tempo (p < 0,001) nos grupos que utilizaram o laser Er,Cr:YSGG. Na aplicação do laser de Er,Cr:YSGG, observou-se que o tempo por si só não impactou significativamente na mudança de temperatura (p = 0,959). Ao avaliar a variação de temperatura em todos os cilindros de Ti expostos ao laser de diodo, levando-se em consideração as variáveis Watt, tempo e Watt-tempo, observou-se diferença estatisticamente significativa (p < 0,05). A faixa de temperatura dos grupos de laser de diodo com 1,8 Watt aplicado nas superfícies do cilindro de Ti foi marcadamente maior do que nos grupos de laser de diodo com 0,8 Watt aplicado (p = 0,006; Figura 5).
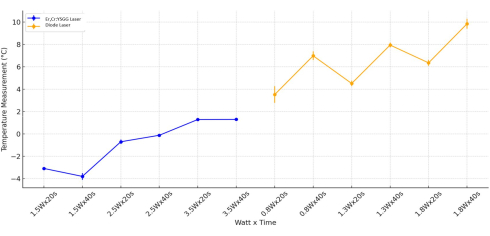
Figura 5: Análise combinada de temperatura. A análise foi feita para os tipos de Er, Cr:YSGG e Laser de Diodo por Watt e Tempo. Clique aqui para ver uma versão maior desta figura.
Análise de imagem
Nas imagens de MEV, uma estrutura porosa de tamanho mícron foi observada em todos os grupos, que é a aparência esperada de superfícies de implantes jateadas e ácidas e ásperas. Com ampliação de 5000x, as superfícies de titânio tratadas com laser mostraram aumento visível dos poros do tamanho de mícrons em comparação com o grupo controle (círculos vermelhos). Com aumento de 250x e 1000x, as superfícies de titânio tratadas com lasers de Er, Cr:YSGG e diodo por 40 s apresentaram mais fusão do que aquelas tratadas por 20 s (Figura 6). Nas imagens AFM, a distribuição das reentrâncias superficiais no grupo controle foi mais homogênea do que nos grupos tratados com laser (Figura 7, Figura 8). Desde que as imagens do AFM visualizaram somente uma área muito pequena de 25μm2 da superfície plana do cilindro titanium, nós não poderíamos obter um resultado detalhado sobre a superfície inteira.

Figura 6: Imagens de MEV de todos os grupos de estudo. Os 6 grupos de laser de diodo são rotulados como D1-D6, enquanto os 6 grupos de laser Er,Cr: YSGG são rotulados como E1-E6. As imagens são tiradas com ampliação de 250x, 1000x, 5000x. Clique aqui para ver uma versão maior desta figura.

Figura 7: Imagem AFM do grupo de controle. Clique aqui para ver uma versão maior desta figura.

Figura 8: Imagens AFM de todos os grupos de estudo. Os 6 grupos de laser de diodo são rotulados como D1-D6, enquanto os 6 grupos de laser Er,Cr: YSGG são rotulados como E1-E6. Clique aqui para ver uma versão maior desta figura.
Resultados de rugosidade da superfície
O parâmetro rugosidade não apresentou diferença estatisticamente significativa nas variáveis tipo de laser (p = 0,841), Watt (p = 0,900), tempo (p = 0,399) e na avaliação das variáveis tipo de laser, Watt e tempo em conjunto (p = 0,924; Figura 9).

Figura 9: Análise de rugosidade por tipo de laser, watt e tempo. Clique aqui para ver uma versão maior desta figura.
Considerando esses resultados, podemos concluir que os lasers de Er,Cr:YSGG e diodo são seguros para descontaminar a superfície de titânio na doença peri-implantar. A variação de temperatura foi inferior a 10 °C, indicando que os parâmetros estavam dentro da faixa segura. Ao mesmo tempo, o valor do perfilômetro não mudou significativamente, indicando que não há desvantagens em termos de rugosidade da superfície. Alterações faciais foram detectadas na análise de imagem, mas isso não pôde ser apoiado pela análise de rugosidade. Os resultados do estudo sustentam que os parâmetros do laser usados estão dentro da faixa segura.
a=Diferença estatisticamente significativa em comparação com o grupo de díodos. (pág<0,05)
b= Diferença estatisticamente significativa em comparação com o laser de diodo 40 s. (p<0,05)
Discussão
Uma discussão significativa está em andamento sobre o método ideal para descontaminar superfícies de implantes no tratamento da peri-implantite. Publicações anteriores propuseram a utilização de medicamentos locais ou sistêmicos, aplicação de laser, limpeza mecânica e/ou química e implantoplastia. Os resultados do nosso estudo revelaram que todas as temperaturas medidas aumentam abaixo do limite crítico de segurança de 10 °C13. No entanto, tendo em mente que este é um estudo in vitro e nem sempre pode replicar condições clínicas, observou-se que o uso do laser de Er,Cr:YSGG e do laser de diodo causou alterações de fusão e microporos na topografia do implante, enquanto a rugosidade da superfície não se alterou.
O uso dos lasers Ho:YAG e Nd:YAG33 para descontaminação foi relatado como inadequado devido aos efeitos de superfície; no entanto, os lasers Er,Cr:YSGG34 e os lasers de diodo18 foram considerados eficazes para esse fim. O laser de diodo aumenta a cicatrização nos tecidos circundantes por meio da expressão de HBD-2 estimulada pela sinalização TGF-β1. O estudo revelou uma redução na rugosidade superficial e na colonização por P. gingivalis, juntamente com um aumento na viabilidade dos fibroblastos e na diferenciação dos osteoblastos, após a aplicação do laser Er,Cr:YSGG em zigue-zague na superfície do titânio35. Os resultados deste estudo mostraram que o laser Er,Cr:YSGG não causou nenhum dano térmico às superfícies de titânio em configurações de energia de até 3,5 W até 40 s. Esse achado se correlaciona com uma revisão da literatura publicada por Smeo et al.36, que determinou que os lasers de érbio podem exercer um impacto antibacteriano sem exceder o limite crítico de temperatura quando utilizados com os parâmetros corretos do laser.
Os parâmetros do laser de diodo de 940 nm nesta investigação foram 0,8 W, 1,3W e 1,8 W, que incluíram diferentes potências e tempos de irradiação de 20 s e 40 s13. Em dois estudos diferentes que avaliaram o uso de lasers de diodo em superfícies de titânio, 20 s37 e 40 s38 foram utilizados como tempo de aplicação. Da mesma forma, lasers de Er,Cr:YSGG aplicados em superfícies de titânio e dente foram utilizados com tempos de aplicação de 20 s39 e 40 s40. Em um estudo, um laser de diodo excedeu a temperatura crítica em 18 segundos13. Em aplicações de laser de diodo, tem sido recomendado evitar a exposição prolongada à superfície radicular para evitar danos térmicos à polpa (limiar crítico de 5,6 °C)28,41. Um estudo avaliando o efeito do uso de vários lasers na mudança de temperatura das superfícies de titânio relatou que os lasers de Er:YAG, CO2, Nd:YAG e diodo não excederam a mudança crítica de temperatura de 10°C em um tanque de água42. Da mesma forma, neste estudo, os grupos de lasers de diodo de 940 nm geraram um aumento de temperatura significativamente mais rápido; no entanto, os valores finais de temperatura estavam abaixo do limite crítico. Na aplicação de um laser de diodo de 940 nm, o aumento da temperatura pode ser diminuído selecionando uma potência reduzida e minimizando o tempo de irradiação. Esses resultados indicam uma relação positiva entre o aumento da densidade de potência/energia 13,43,44 e a temperatura elevada na ausência de resfriamento a água, enfatizando a importância do resfriamento a água durante a irradiação como o laser Er,Cr:YSGG 16,45.
A perfilometria mecânica e óptica 3D (contato e sem contato) são os métodos in vitro mais populares para medição quantitativa da nanotopografia do material odontológico e rugosidade da superfície do implante, enquanto as imagens de MEV são o padrão-ouro para avaliação qualitativa31. A medição da rugosidade com um perfilômetro de contato pode causar danos à superfície e levar a medições imprecisas46. Embora a imagem SEM não tenha sido capaz de facilitar a análise quantitativa e qualitativa das amostras, as imagens AFM podem fornecer informações quantitativas em termos de rugosidade da superfície e profundidade 3D47. Alterações morfológicas foram observadas nas superfícies dos implantes após o tratamento com laser, caracterizadas por um aumento no diâmetro dos microporos, uma morfologia derretida e um aumento da prevalência de microporos sem caroço em comparação com o grupo controle. Nessas condições experimentais, a superfície do cilindro de Ti durante a análise de MEV revelou alterações na superfície. Além disso, essas alterações foram afetadas pelo tipo de laser, potência utilizada e tempo gasto na irradiação do laser. Os autores concordaram com a conclusão de que os níveis de dano superficial e o tempo nos lasers de diodo18 e Er,Cr:YSGG 21,48 se correlacionam com o aumento da potência. Pesquisas futuras devem examinar se essas modificações têm implicações terapêuticas.
A rugosidade da superfície do implante dentário, também conhecida como microtopografia, é um fator crucial que influencia a osseointegração. Em um estudo recente, as superfícies de titânio foram tratadas com quatro protocolos diferentes. As células-tronco mesenquimais e de superfície de titânio foram preservadas na superfície tratada com laser e os resultados de adesão das células-tronco foram melhores do que outras técnicas (escova Ti-Ni, fluxo de ar e broca dentária)49. Todos os valores de Ra do cilindro de Ti examinado foram reduzidos durante a irradiação do laser; no entanto, não foram observadas diferenças estatisticamente significativas antes e depois da irradiação. A irradiação do laser de diodo reduziu a rugosidade da superfície ao derreter a superfície de Ti quando níveis de potência maiores foram usados. Esses achados são consistentes com um estudo anterior de Stübinger et al.50, no qual um laser de diodo de 810 nm foi usado para descontaminar a superfície do implante e não mostrou efeito significativo na superfície, embora seja contraditório com os resultados do estudo realizado por Kim et al.51 e Rezeka et al.17, usando comprimento de onda de 940 nm quando tratado com potências de 2 e 3 W e observou aumento da rugosidade da superfície com a aplicação do laser.
Este estudo é limitado pela falta de testes celulares e microbiológicos. O presente estudo tem como objetivo avaliar as mudanças topográficas no cilindro de Ti após irradiação de diodo e laser de Er,Cr:YSGG; No entanto, as implicações biológicas dos vários tratamentos requerem mais investigações in vitro e in vivo . Outra limitação é que a análise estatística da rugosidade superficial realizada neste estudo envolve apenas dados do perfilômetro. A abordagem AFM mostrou-se eficaz na avaliação da eficácia de dois tipos de laser frequentemente utilizados em odontologia.
Conclusões
Em nossa investigação, nenhum dos aumentos de temperatura excedeu o limite fisiológico de 10 °C. Consequentemente, diferenças de temperatura estatisticamente significativas foram consideradas clinicamente irrelevantes. O tipo e a potência do laser não afetaram significativamente a AR; portanto, a irradiação de um laser de diodo de 0,8, 1,3 e 1,8 W e um laser Er,Cr:YSGG com 1,5 W, 2,5 W e 3,5 W por 20 s e 40 s pode limpar a superfície do Ti sem danos. No entanto, esses achados foram conduzidos in vitro, e ensaios clínicos serão necessários para verificar os resultados deste estudo. O presente estudo investigou várias técnicas que simulam um cenário clínico de desbridamento de implantes.
Divulgações
Os autores não têm conflitos de interesse a divulgar.
Agradecimentos
Os cilindros de titânio utilizados no estudo foram produzidos pela Naxis Implant.
Materiais
| Name | Company | Catalog Number | Comments |
| Atomic Force Microscopy | ezAFM | Compact AFM Model | |
| Diode | Biolase | Epic 10, 940 nm Wavelength | |
| E3 Tip | Fiber Diameter: 300 µm, Fiber Length: 9 mm | ||
| Er,Cr:YSGG Laser | Iplus | 2780 nm Wavelength | |
| Profilometer | Mitutoyo | Surftest SJ-201 Model | |
| RFPT-14 Tip | Outer Tip Diameter: 580 µm, Tip Length: 14 mm | ||
| Scanning Electron Microscope | FEI | Quanta FEG 250 Model | |
| Stand | Custom Design | Rhinoceros application, Flamix PLA filament, Bambulab X1C Device | |
| Thermometer | Keithley | 2000 Series Model, K tip termokulp | |
| Titanium Cylinder | Naxis | 10 mm height, 5 mm diameter, SLA Surface, Titanium |
Referências
- Guillaume, B. Dental implants: A review. Morphologie. 100 (331), 189-198 (2016).
- Henry, P. J. Tooth loss and implant replacement. Aust Dent J. 45 (3), 150-172 (2000).
- Berglundh, T., Armitage, G., Araujo, M. G., et al. Peri-implant diseases and conditions: Consensus report of workgroup 4 World Workshop on the Classification of Periodontal and Peri-Implant Diseases and Conditions. J Periodontol. 89 (1), S313-S318 (2018).
- Herrera, D., Berglundh, T., Schwarz, F., et al. Prevention and treatment of peri-implant diseases—The EFP S3 level clinical practice guideline. J Clin Periodontol. 50 (S26), 4-76 (2023).
- Guarnieri, R., Reda, R., Di Nardo, D., Pagnoni, F., Zanza, A., Testarelli, L. Prevalence of Peri-Implant Mucositis, Peri-Implantitis and Associated Risk Indicators of Implants with and without Laser-Microgrooved Collar Surface: A Long-Term (≥20 Years) Retrospective Study. J Pers Med. 14 (4), (2024).
- Figuero, E., Graziani, F., Sanz, I., Herrera, D., Sanz, M. Management of peri‐implant mucositis and peri‐implantitis. Periodontology 2000. 66 (1), 255-273 (2014).
- Tomasi, C., Wennström, J. L. Full-mouth treatment vs. the conventional staged approach for periodontal infection control. Periodontology 2000. 51 (1), 45-62 (2009).
- Baima, G., Citterio, F., Romandini, M., et al. Surface decontamination protocols for surgical treatment of peri‐implantitis: A systematic review with meta‐analysis. Clin Oral Implants Res. 33 (11), 1069-1086 (2022).
- Subramani, K., Wismeijer, D. Decontamination of titanium implant surface and re-osseointegration to treat peri-implantitis: a literature review. Int J Oral Maxillofac Implants. , Accessed August 4, 2024 (2012).
- Świder, K., Dominiak, M., Grzech-Leśniak, K., Matys, J. Effect of different laser wavelengths on periodontopathogens in peri-implantitis: A review of in vivo studies. Microorganisms. 7 (7), 189(2019).
- Mizutani, K., Aoki, A., Coluzzi, D., Yukna, R., Wang, C. Y., Pavlic, V., Izumi, Y. Lasers in minimally invasive periodontal and peri‐implant therapy. Periodontology 2000. 71 (1), 185-212 (2016).
- Eriksson, R. A., Albrektsson, T. The effect of heat on bone regeneration: An experimental study in the rabbit using the bone growth chamber. J Oral Maxillofac Surg. 42 (11), 705-711 (1984).
- Geminiani, A., Caton, J. G., Romanos, G. E. Temperature change during non-contact diode laser irradiation of implant surfaces. Lasers Med Sci. 27 (2), 339-342 (2012).
- Alpaslan Yayli, N. Z., Talmac, A. C., Keskin Tunc, S., Akbal, D., Altindal, D., Ertugrul, A. S. Erbium, chromium-doped: yttrium, scandium, gallium, garnet and diode lasers in the treatment of peri‐implantitis: Clinical and biochemical outcomes in a randomized-controlled clinical trial. Lasers Med Sci. 37 (1), 665-674 (2022).
- Peters, N., Tawse-Smith, A., Leichter, J., Tompkins, G. Laser therapy: The future of peri-implantitis management. J Periodontol. 22 (1), 1(2012).
- Alhaidary, D., Franzen, R., Hilgers, R. D., Gutknecht, N. First investigation of dual-wavelength lasers (2780 nm Er,Cr:YSGG and 940 nm diode) on implants in a simulating peri-implantitis situation regarding temperature changes in an in vitro pocket model. Photobiomodul Photomed Laser Surg. 37 (8), 508-514 (2019).
- Rezeka, M. A., Metwally, N. A., Abd El Rehim, S. S., Khamis, M. M. Evaluation of the effect of diode laser application on the hydrophilicity, surface topography, and chemical composition of titanium dental implant surface. J Prosthodont. 2024, 1-8 (2025).
- Khalil, M. I., Sakr, H. Implant surface topography following different laser treatments: An in vitro study. Cureus. 15 (5), e38731(2023).
- Tosun, E., Tasar, F., Strauss, R., Kivanc, D. G., Ungor, C. Comparative evaluation of antimicrobial effects of Er:YAG, diode, and CO2 on titanium discs: An experimental study. J Oral Maxillofac Surg. 70 (5), 1064-1069 (2012).
- Stübinger, S., Homann, F., Etter, C., Miskiewicz, M., Wieland, M., Sader, R. Effect of Er:YAG, CO and diode laser irradiation on surface properties of zirconia endosseous dental implants. Lasers Surg Med. 40 (3), 223-228 (2008).
- Park, J., Heo, S., Koak, J., Kim, S. K., Han, C. H., Lee, J. H. Effects of laser irradiation on machined and anodized titanium disks. Int J Oral Maxillofac Implants. 27 (6), Accessed September 22, 2024 1215-1221 (2012).
- Aoki, A., Mizutani, K., Schwarz, F., et al. Periodontal and peri-implant wound healing following laser therapy. Periodontol 2000. 68 (1), 217-269 (2015).
- Roncati, M., Lucchese, A., Carinci, F. Non-surgical treatment of peri-implantitis with the adjunctive use of an 810-nm diode laser. J Indian Soc Periodontol. 17 (6), 812-817 (2013).
- Romanos, G. E., Gutknecht, N., Dieter, S., Schwarz, F., Crespi, R., Sculean, A. Laser wavelengths and oral implantology. Lasers Med Sci. 24 (6), 961-970 (2009).
- Hauser-Gerspach, I., Stübinger, S., Meyer, J. Bactericidal effects of different laser systems on bacteria adhered to dental implant surfaces: An in vitro study comparing zirconia with titanium. Clin Oral Implants Res. 21 (3), 277-283 (2010).
- Hafeez, M., Calce, L., Hong, H., Hou, W., Romanos, G. E. Thermal effects of diode laser-irradiation on titanium implants in different room temperatures in vitro. Photobiomodul Photomed Laser Surg. 40 (8), 554-558 (2022).
- Koopaie, M., Kia Darbandsari, A., Hakimiha, N., Kolahdooz, S. Er,Cr:YSGG laser surface treatment of gamma titanium aluminide: Scanning electron microscopy-energy-dispersive X-ray spectrometer analysis, wettability and Eikenella corrodens and Aggregatibacter actinomycetemcomitans bacteria count - in vitro study. Proc Inst Mech Eng H. 234 (8), 769-783 (2020).
- Kayar, N. A., Hatipoǧlu, M. Could we set a convenient irradiation time to reduce the possibility of thermal pulp damage during diode laser as an adjunct to periodontal treatment? An in vitro analysis. Photobiomodul Photomed Laser Surg. 39 (7), 480-485 (2021).
- Barrak, H., Mahdi, S. S., Alkurtas, S. A., Size, P. Clinical applications of a 940 nm diode laser for laser troughing versus conventional method: A preliminary study. Iraqi J Laser. 23 (2), (2024).
- Beer, F., Körpert, W., Passow, H., et al. Reduction of collateral thermal impact of diode laser irradiation on soft tissue due to modified application parameters. Lasers Med Sci. 27 (5), 917-921 (2012).
- Schwarz, F., Nuesry, E., Bieling, K., Herten, M., Becker, J. Influence of an erbium, chromium-doped yttrium, scandium, gallium, and garnet (Er,Cr:YSGG) laser on the reestablishment of the biocompatibility of contaminated titanium implant surfaces. J Periodontol. 77 (11), 1820-1827 (2006).
- Al-Omari, W. M., Palamara, J. E. The effect of Nd:YAG and Er,Cr:YSGG lasers on the microhardness of human dentin. Lasers Med Sci. 28 (1), 151-156 (2013).
- Kreisler, M., Götz, H., Duschner, H., d’Hoedt, B. Effect of Nd:YAG, Ho:YAG, Er:YAG, CO2, and GaAlAs laser irradiation on surface properties of endosseous dental implants. Int J Oral Maxillofac Implants. 17 (5), 202-209 (2002).
- Kottmann, L., Franzen, R., Conrads, G., Wolfart, S., Marotti, J. Effect of Er,Cr:YSGG laser with a side-firing tip on decontamination of titanium disc surface: An in vitro and in vivo study. Int J Implant Dent. 9 (1), 7(2023).
- Yao, W. L., Lin, J. C. Y., Salamanca, E., et al. Er,Cr:YSGG laser performance improves biological response on titanium surfaces. Materials. 13 (3), 756(2020).
- Smeo, K., Nasher, R., Gutknecht, N. Antibacterial effect of Er,Cr:YSGG laser in the treatment of peri-implantitis and their effect on implant surfaces: A literature review. Lasers Dent Sci. 2 (2), 63-71 (2018).
- Fletcher, P., Linden, E., Cobb, C., Zhao, D., Rubin, J., Planzos, P. Efficacy of removal of residual dental cement by laser, ultrasonic scalers, and titanium curette: An in vitro study. Compend Contin Educ Dent. , (2025).
- Lollobrigida, M., Fortunato, L., Serafini, G., et al. The prevention of implant surface alterations in the treatment of peri-implantitis: Comparison of three different mechanical and physical treatments. Int J Environ Res Public Health. 17 (8), 2624(2020).
- Arora, S., Lamba, A. K., Faraz, F., Tandon, S., Ahad, A. Evaluation of the effects of Er,Cr:YSGG laser, ultrasonic scaler and curette on root surface profile using surface analyser and scanning electron microscope: An in vitro study. J Lasers Med Sci. 7 (4), 243-249 (2016).
- Jin, S. H., Lee, E. M., Park, J. B., Kim, K. K., Ko, Y. Decontamination methods to restore the biocompatibility of contaminated titanium surfaces. J Periodontal Implant Sci. 49 (3), 193-204 (2019).
- Kayar, N. A., Hatipoǧlu, M. Can we determine an appropriate timing to avoid thermal pulp hazard during gingivectomy procedure? An in vitro study with diode laser. Photobiomodul Photomed Laser Surg. 39 (2), 94-99 (2021).
- Monzavi, A., Fekrazad, R., Chinipardaz, Z., Shahabi, S., Behruzi, R., Chiniforush, N. Effect of various laser wavelengths on temperature changes during peri-implantitis treatment: An in vitro study. Implant Dent. 27 (3), 311-316 (2018).
- Valente, N. A., Calascibetta, A., Patianna, G., Mang, T., Hatton, M., Andreana, S. Thermodynamic effects of 3 different diode lasers on an implant-bone interface: An ex-vivo study with review of the literature. J Oral Implantol. 43 (2), 94-99 (2017).
- Leja, C., Geminiani, A., Caton, J., Romanos, G. E. Thermodynamic effects of laser irradiation of implants placed in bone: An in vitro study. Lasers Med Sci. 28 (6), 1435-1440 (2013).
- Strever, J. M., Lee, J., Ealick, W., et al. Erbium, chromium:yttrium-scandium-gallium-garnet laser effectively ablates single-species biofilms on titanium disks without detectable surface damage. J Periodontol. 88 (5), 484-492 (2017).
- Bourauel, C., Fries, T., Drescher, D., Plietsch, R. Surface roughness of orthodontic wires via atomic force microscope, laser specular reflectance, and profilometry. Eur J Orthod. 20 (1), Accessed February 13, 2025 79-92 (1998).
- Choi, S., Kim, J. H., Kim, N. J., et al. Morphological investigation of various orthodontic lingual bracket slots using scanning electron microscopy and atomic force microscopy. Microsc Res Tech. 79 (12), 1193-1199 (2016).
- Huang, H. H., Chuang, Y. C., Chen, Z. H., Lee, T. L., Chen, C. C. Improving the initial biocompatibility of a titanium surface using an Er,Cr:YSGG laser-powered hydrokinetic system. Dent Mater. 23 (4), 410-414 (2007).
- Furtsev, T. V., Koshmanova, A. A., Zeer, G. M., et al. Laser cleaning improves stem cell adhesion on the dental implant surface during peri-implantitis treatment. Dent J. 11 (2), 30(2023).
- Stübinger, S., Homann, F., Etter, C., Miskiewicz, M., Wieland, M., Sader, R. Effect of Er:YAG, CO and diode laser irradiation on surface properties of zirconia endosseous dental implants. Lasers Surg Med. 40 (3), 223-228 (2008).
- Kim, H. K., Park, S. Y., Son, K., et al. Alterations in surface roughness and chemical characteristics of sandblasted and acid-etched titanium implants after irradiation with different diode lasers. Appl Sci. 10 (12), 4167(2020).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoExplore Mais Artigos
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados