Method Article
כריתה לפרוסקופית של חצי הכבד השמאלי בשילוב כריתת אונה זנבית
In This Article
Summary
כולנגיוקרצינומה תוך-כבדית של האונה הזנבית מהווה אתגר עבור מנתחים רבים בשל מיקומה הייחודי. כאן, אנו מציגים פרוטוקול המציג את הפרטים שלב אחר שלב של כריתת המיהפטקטומיה השמאלית הלפרוסקופית בשילוב עם כריתת אונה זנבית עבור כולנגיוקרצינומה.
Abstract
כולנגיוקרצינומה תוך-כבדית (ICC) היא הגידול הממאיר הנפוץ של הכבד. כריתה כירורגית רדיקלית היא עמוד התווך של טיפול מרפא פוטנציאלי ל-ICC. כריתת כבד אנטומית עבור ICC באונה הזנבית היא אחת מכריתות הכבד הקשות ביותר. מכיוון שהגידול ממוקם עמוק ופולש בקלות לכלי הדם שמסביב, כגון עוקץ הכבד השמאלי, עוקץ הכבד הימני ווריד הכבד האמצעי. כריתת כבד אנטומית לפרוסקופית של האונה הזנבית לא רק מבטיחה שולי חתך שליליים אלא גם מציעה גישה זעיר פולשנית יותר למטופלים. טכניקה זו עומדת להפוך לבחירה המועדפת לניתוח רדיקלי של האונה הזנבית בעתיד. בפרוטוקול כירורגי זה, מטופל גבר בן 65 עם כולנגיוקרצינומה תוך כבדית (בגודל של כ-3.2 × 1.9 ס"מרבוע) הממוקם באונה הזנבית השמאלית עבר כריתה לפרוסקופית של הכבד השמאלי בשילוב עם כריתת אונה זנבית בהצלחה ללא סיבוכים לאחר הניתוח. בדיקה פתולוגית לאחר הניתוח הראתה כולנגיוקרצינומה עם פקקת גידול הנראית בכלי הדם. המטופל שוחרר ביום ה-14 לאחר הניתוח. כריתה לפרוסקופית של חצי הכבד השמאלי בשילוב עם כריתת אונה זנבית לטיפול באונה הזנבית ICC יכולה להתבצע בבטחה ואינה מוסיפה באופן משמעותי לתחלואה או לתמותה של ההליך.
Introduction
כולנגיוקרצינומה תוך-כבדית מקורה בתאי אפיתל של צינור המרה התוך-כבדי והיא כולנגיוקרצינומה המתרחשת מעל צינור המרה המשני של הכבד. שכיחות ICC שנייה רק לזו של קרצינומה הפטו-תאית (HCC), המהווה 10% עד 15% מסרטן הכבד הראשוני וכ-20% מסרטן דרכי המרה1. שכיחות ICC גדלה משנה לשנה בעולם, וגדלה ב-140% ב-40 השנים האחרונות2. כריתה כירורגית נותרה עמוד התווך של טיפול פוטנציאלי מרפא עבור ICC. עם זאת, רק ל-20% עד 30% מהחולים יש אפשרות לכריתה כירורגית. לאחר כריתה כירורגית, שיעור ההישרדות הכולל ל-5 שנים של חולי ICC הוא רק 20% עד 35%3. הסיבה לכך היא שגם אם מבוצעת כריתה רדיקלית, רק חולים מעטים יכולים להשיג שוליים שליליים4. חשוב במיוחד לחולי ICC מוקדמים לעבור ניתוח מרפא. הניתוח המרפא לחולי ICC קשור קשר הדוק לשולי הניתוח. שתי מטא-אנליזות אחרונות 5,6 הצביעו על כך שרוחב שוליים כירורגיים של >1 ס"מ קשור להישרדות כללית טובה יותר. מחקר7 שכלל 126 חולים הראה כי מרווח ≥1.0 ס"מ היה קשור להישרדות כללית טובה יותר (OS) והישרדות ללא הישנות (RFS).
בניתוחי ICC, כריתת כבד אנטומית, החשובה לפרוגנוזה של חולי ICC8, לא רק יכולה להשיג שוליים כירורגיים בטוחים אלא גם יכולה לכרות את פדיקול הכבד הפגום. מחקר9 דיווח כי מסלול החדירה הנפוץ ביותר לכולנגיוקרצינומה של האונה הזנבית הוא דרך רקמת חיבור סיבית לאורך מערכת גליסון, ולא דרך צינור המרה. במחקר קודם, Si et al.10 סקרו נתונים מ-702 חולי ICC ומצאו כי שכיחות הסיבוכים הייתה דומה בין כריתה אנטומית לכריתה לא אנטומית, וכריתה אנטומית הייתה קשורה להישרדות טובה יותר ללא מחלה והישרדות כוללת לאחר 1, 3 ו-5 שנים. מחקר אחר התואם נטייה11 על ICC זיהה כריתה לא אנטומית כגורם סיכון עצמאי ל-OS (עמ' < 0.05).
עם זאת, כריתה כירורגית של ה-ICC הזנבי יכולה להיות מאתגרת עבור המנתח. קשה מאוד למנתחים לחקור את האונה הזנבית בגלל מיקומה האנטומי הייחודי, כגון חדירתה העמוקה לפרנכימת הכבד וקרבתה לכלי דם עיקריים12 (הווריד הנבוב התחתון, ורידי הכבד האמצעיים או הימניים, וריד הפורטל והרצועה הוורידית). אלה יכולים להקשות על השגת שדה ראייה רחב במהלך הניתוח ולקבל קצה חיתוך בלתי נראה. בשנים האחרונות, עם המחקר המפורט של אנטומיה של הכבד, ההתפתחות המהירה של הטכנולוגיה הלפרוסקופית והקידום המתמשך של הרעיון של כריתה מדויקת של הכבד, הניהול הכירורגי של ICC גדל מכריתת אונה זנביתמבודדת 13,14 לכריתת חצי הכבד לפרוסקופית בשילוב עם כריתת אונה זנבית15המדווח לעתים רחוקות בספרות., יש צורך גדול בסרטונים של מבצעים מוצלחים כדי להנחות את השימוש הנרחב במבצעים כאלה בעתיד. כאן, אנו מציגים כריתה לפרוסקופית של חצי הכבד השמאלי בשילוב עם כריתת אונה זנבית לטיפול בכולנגיוקרצינומה תוך-כבדית באונה הזנבית.
גבר סיני בן 65 אושפז בבית החולים עם גוש כבד שזוהה במקרה על ידי אולטרסאונד בטן. בדיקה גופנית לא הראתה חריגות משמעותיות. בדיקות מעבדה, כולל בדיקות דם שגרתיות, בדיקות תפקודי כבד, קרישה ומדדי גידול (AFP, CEA, CA199), היו תקינות. טומוגרפיה ממוחשבת משופרת (CT) של הבטן העליונה הראתה צלשיפור חריג של 3.2 1.9 ס"מ 2 בצומת S1/4/8 והראתה כי וריד הכבד האמצעי (MHV) ווריד הכבד השמאלי (LHV) חולקים גזע משותף (איור 1A). הדמיית תהודה מגנטית משופרת (MRI) של הבטן העליונה חשפה גם גושבגודל 2.5 2.0 ס"מ באותו אזור, אך מרמז על ICC (איור 1B). לאחר השלמת ההערכה הטרום ניתוחית, החלטנו לבצע כריתה לפרוסקופית של חצי הכבד השמאלי בשילוב כריתת אונה זנבית כדי להבטיח שוליים כירורגיים שליליים.
Protocol
פרוטוקול זה עוקב אחר ההנחיות של ועדת האתיקה למחקר בבני אדם של בית החולים העממי מייג'ואו. התקבלה הסכמה מדעת מהמטופלים לשחרר מידע ונתונים הקשורים לטיפול זה.
1. הכנה טרום ניתוחית
- אסור על המטופל לאכול במשך 6 שעות ולשתות במשך שעתיים לפני הניתוח.
- יש למרוח את האנטיביוטיקה (1 גרם של Ceftriaxone sodium) דרך זריקה תוך ורידית במרפק כדי למנוע זיהום באופן מונע 30 דקות לפני חיתוך העור.
- השתמש באינטובציה של קנה הנשימה בהרדמה כללית. ניקוב וצנתור של העורק הרדיאלי הימני (גודל קטטר, 20 G) ואת וריד הצוואר הפנימי (גודל קטטר, 8 Fr) בהנחיית אולטרסאונד.
- יש לעקר את העור עם קרצוף על בסיס יוד 0.5% וסדינים סטריליים במגבות כדי לחשוף את אזור הניתוח במלואו. יש לחטא את אזור הניתוח ביודופור שלוש פעמים.
2. טכניקה כירורגית
- הגדרת פעולה
- חותכים את העור כ -10 מ"מ לאורך מתחת לטבור, ואז מכניסים מחט פנאומופריטונאום חד פעמית דרך החתך. הזריק CO2 לאחר שמחט הפנאומופריטונאום מחוברת למכונת הפנאומופריטונאום כדי לבסס את הפנאומופריטונאום.
- לאחר מכן, הכנס טרוקר ברזל 10 מ"מ לתוך החתך. שנה את המטופל ממצב שכיבה למצב שכיבה עם רגליים פשוקות, ראש מורם ב-30 מעלות וכפות רגליים מונמכות לאחר בדיקה ללא נזק לנקב.
הערה: לחץ הפנאומופריטונאום נקבע ל-12 מ"מ כספית. - הניחו שני טרוקרים בקוטר 12 מ"מ לקו האמצע הימני והשמאלי מעל 4 אצבעות הטבור (B ו-C), שני טרוקרים בקוטר 5 מ"מ לקו בית השחי הקדמי הימני התת-צלעי והקו התת-צלעי השמאלי (D ו-E), ראה איור 2.
- בצע חקר בטן באופן לפרוסקופי. בדוק אם יש פציעה בבטן ודימום דקירה; בדוק נוכחות של גרורות חוץ-כבדיות משמעותיות כדי להעריך את היתכנות הניתוח הרדיקלי.
- שלב החיפושים
- שחררו את החצי השמאלי של הכבד וחלקו את הרצועות העגולות והפלציפורמיות בחזרה לגובה הפוסה של וריד הכבד. מחלקים את הרצועה המשולשת השמאלית ואת הרצועה הכלילית השמאלית, ומשתרעים עד לזיהוי הגבול הרוחבי של וריד הכבד השמאלי.
- מהדקים את הרצועה העגולה הפרוקסימלית של הכבד.
- חשוף את הרצועה של הכבד בתריסריון עם הגישה לאומנטום הקטן ומקם באופן שגרתי רצועת חסימת זרימת דם בכבד. במידת הצורך, השתמש בשיטת פרינגל כדי לחסום לסירוגין את זרימת הדם בכבד.
- שלב דיסקציה
- נתח את הפדיקל השמאלי של הכבד בגישה החוץ-תקלית.
- לאחר הרמת האונה הצדדית השמאלית, חשוף את האונה הזנבית על ידי פתיחתה המלאה לאומנטום הקטן. לזהות, לקלוע ולנתח את פדיקל הכבד השמאלי באמצעות תופס לא טראומטי ומלקחיים בזווית ישרה של 10 מ"מ.
- כמה דקות לאחר מכן, צרו קו מסומן לפני הכריתה עם צריבה חשמלית שמבוססת על קו האיסכמיה של החצי השמאלי והימני של הכבד (איור 3A, B).
- השתמשו בסכין על-קולית כדי לחתוך את רקמת הכבד, החל משטח הכבד העליון מקדימה לאחור, עד שמפלס הפדיקל השמאלי והימני של הכבד נחשף במלואו לאורך הקו המסומן (איור 3C).
- תקן את הצינור המובנה בקוטר >4 מ"מ בעזרת קליפסים ונתק אותו עם סכין אולטרסאונד בקצה הדיסטלי.
- ניצול הזמן להפעלת הכבד, נתח את המרווח בין האונה הזנבית לווריד הנבוב התחתון (IVC) באמצעות גישה גבית. כאשר נתקלים בווריד הכבד הקצר (VHS), מהדקים אותו עם hem-o-lok ולאחר מכן נתק אותו בקצה הדיסטלי.
- אחרי החשיפה המלאה של IVC, סמנו את המישור הפרקאבלי הימני, שהוא השוליים הימניים הדמיוניים של האונה הזנבית (איור 3D).
- לאחר הסרת קו המתלה של פדיקול הכבד השמאלי, נתק את פדיקל הכבד השמאלי על ידי טעינה מחדש של סאטלר ליניארי (איור 4A).
- לאורך הקצה השבור של עוקץ הכבד השמאלי, חפשו את פדיקל הכבד של האונה הזנבית ונתחו אותו, ואז הדקו את הקצה הפרוקסימלי שלו עם שני hem-o-loks וחתכו את הקצה הדיסטלי שלו עם סכין אולטרה-סאונד דרך הגישה השמאלית (איור 4B).
- משוך את שער הכבד הראשון לכיוון ימינה כדי לחשוף את מישור הפרקאבל הימני. לאורך השוליים הימניים של האונה הזנבית, כפי שמסומן, חתכו את פרנכימת הכבד מתחת לצומת של פדיקל הכבד השמאלי והימני עד שנחשף הגזע המשותף של MHV ווריד הכבד השמאלי (LHV) (איור 4C).
- כאשר נתקלים בווריד הזנב, מהדקים אותו עם hem-o-lok ומתנתקים בקצהו הדיסטלי.
- לאחר מכן, השלם את החתך של תא המטען המשותף של MHV ו-LHV על ידי שימוש בטעינת חותך ליניארית כדי להפריד לחלוטין את הכבד השמאלי והאונה הזנבית, תוך הקפדה על פגיעה במתיחה בווריד הכבד האמצעי ובווריד הנבוב.
- לאחר המוסטזיס יסודי של הפצע, הניחו את הדגימה בשקית והוציאו אותה דרך חתך אנכי של 6 ס"מ סביב הטבור בבטן התחתונה. הניחו שני צינורות ניקוז על קטע הכבד ועל שקע ההפטורנל, בהתאמה.
- נתח את הפדיקל השמאלי של הכבד בגישה החוץ-תקלית.
תוצאות
התוצאה הרלוונטית של פעולה זו מוצגת בטבלה 1. האונה הזנבית הכוללת והכבד השמאלי של המטופל הוסרו תוך 200 דקות עם איבוד דם של 50 מ"ל וכ-1500 מ"ל של תחליף נוזלים. תפוקת השתן תוך הניתוחית הייתה 150 מ"ל. זמן המעבר של פרנכימת הכבד, כולל ניתוח פדיקל הכבד והרווח בין האונה הזנבית של הכבד לווריד הנבוב התחתון, היה 84 דקות. תמרון הפרינגל בוצע שלוש פעמים (זמן חסימת ההילר בכבד היה 10 דקות, 20 דקות ו-15 דקות, בהתאמה). כל תקופת ההחלמה לאחר הניתוח עברה בצורה חלקה, ללא סימנים של דליפת מרה ודימום לאחר הניתוח. שני נקזים הוסרו ביוםה-6 וה-10 לאחר הניתוח. המטופל שוחרר ביוםה-14 לאחר הניתוח.
הניתוח הפתולוגי חשף כולנגיוקרצינומה (pT1N0M0, שלב I,מהדורה 8 של AJCC)16, עם פקקת גידול גלויה בכלי הדם. דרגת MVI: M2 (קבוצת סיכון גבוהה). שולי הניתוח של הכבד היו שליליים. אימונוהיסטוכימיה הצביעה על חיוביות CK7, CK19, EMA, CK8, MSH6, MSH2, PMS2, MLH1, Ki67 (40%). על פי AJCC8 th edition16, המטופל חזר לבית החולים חודש לאחר הניתוח כדי לקבל כימותרפיה קבועה בגלל דרגת MVI.

איור 1: טומוגרפיה ממוחשבת (CT) והדמיית תהודה מגנטית (MRI). (A) וריד הכבד האמצעי (MHV) ווריד הכבד השמאלי (LHV) חלקו גזע משותף (חיצים אדומים וצהובים), כפי שמוצג על ידי טומוגרפיה ממוחשבת משופרת (CT) של הבטן העליונה במהלך שלב ההשהיה. (B) הדמיית הראייה העטרתית של דימות תהודה מגנטית משופרת (MRI) של הבטן העליונה הראתה שהגידול שממוקם בצומת S1/4/8 קשור קשר הדוק ל-MHV (חץ כחול). אנא לחץ כאן לצפייה בגרסה גדולה יותר של איור זה.
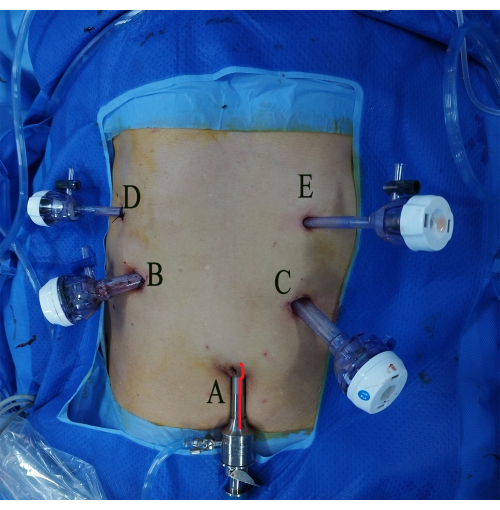
איור 2: חתך מיצוי דגימה ומיקום טרוקר. (A) חור התצפית. (B) הטרוקר של הקו האמצעי הימני היה חור הפעולה העיקרי עבור המפעיל. (C) הטרוקר של הקו האמצעי השמאלי היה חור הפעולה העזר עבור העוזר. (ד) הטרוקר של קו בית השחי הקדמי התת-צלעי הימני היה חור הפעולה העזר עבור המפעיל. (E) הטרוקר של הקו האמצעי התת-צלעי השמאלי היה חור הפעולה העיקרי עבור העוזר, ו(הקו האדום) החתך האנכי להסרת הדגימה. אנא לחץ כאן לצפייה בגרסה גדולה יותר של איור זה.
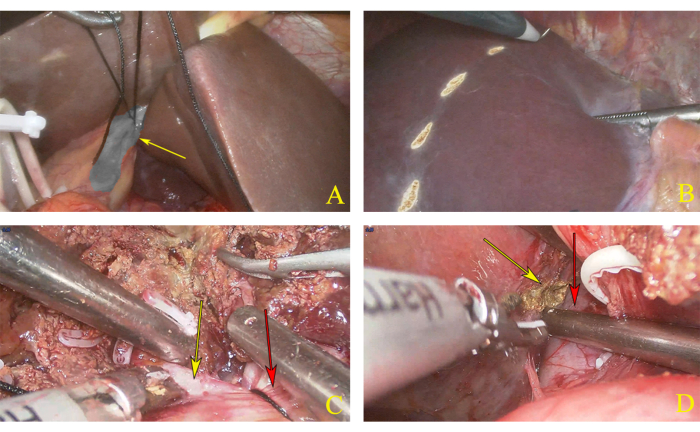
איור 3: דיסקציה של כריתת חצי הכבד השמאלית. (A) קשירה של עוקץ הכבד השמאלי. החץ הצהוב מציין את עוקץ הכבד השמאלי. (ב) קו טרום כריתה המסומן לפי הקו האיסכמי. (ג) מישור החתך. החץ הצהוב מציין את עוקץ הכבד הימני, והחץ האדום מציין את עוקץ הכבד השמאלי. (D) החץ הצהוב מציין את הקצה הימני של אונת הזנב, והחץ האדום מציין את הווריד הנבוב התחתון (IVC). אנא לחץ כאן לצפייה בגרסה גדולה יותר של איור זה.
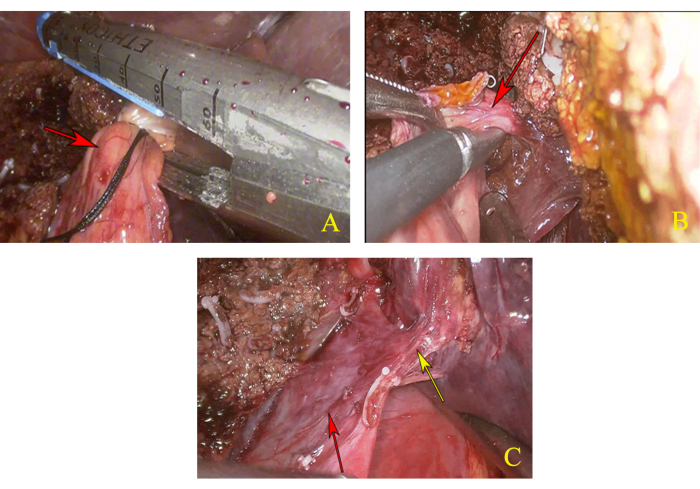
איור 4: דיסקציה של אונת הזנב. (A) נתק את עוקץ הכבד השמאלי. החץ האדום מציין את עוקץ הכבד השמאלי. (ב) אנטומיה ודיסקציה של עוקץ הכבד של האונה הזנבית. החץ האדום מציין את הפדיקל הכבדי של האונה הזנבית. (C) חשיפה מלאה של הגזע המשותף של וריד הכבד האמצעי (MHV) ווריד הכבד השמאלי (LHV). החץ הצהוב מציין את הגזע המשותף של MHV ו-LHV, והחץ האדום מציין IVC. אנא לחץ כאן לצפייה בגרסה גדולה יותר של איור זה.
| משתנה | תוצאה | |
| תוך ניתוחי | זמן פעולה (דקות) | 200 |
| איבוד דם תוך ניתוחי (מ"ל) | 50 | |
| עירוי דם (מ"ל) | 0 | |
| החלפת נוזלים (מ"ל) | 1500 | |
| תפוקת שתן (מ"ל) | 150 | |
| זמן חסימת ההילר בכבד (דקות) | 10, 20, 15 | |
| לאחר הניתוח | זמן שחרור (ימים) | 14 |
| סיבוכים לאחר הניתוח | ללא | |
| פתולוגי | אבחון | כולנגיוקרצינומה תוך-כבדית |
| סמנים חיוביים | CK7, CK19, EMA, CK8, MSH6, MSH2, PMS2, MLH1, Ki67(40%) | |
| סמנים שליליים | CEA, Hep, Arginase-1, HER-2 | |
| דרגת MVI | מ"ר | |
טבלה 1: תוצאות כירורגיות ופרטים לאחר הניתוח של המטופל.
Discussion
האונה הזנבית ICC פולשת לעתים קרובות למקטעי הכבד הסובבים או לפדיקל הכבד הסמוך, שעקרון הטיפול דומה לחלק מ-hilar cholangiocarcinoma17, ובשל מיקומה האנטומי והמאפיינים הביולוגיים שלה, האונה הזנבית ICC נוטה לפגוע במבנים שמסביב במהלך הניתוח, מה שמוביל לדימום מסיבי ולדליפת מרה לאחר הניתוח. אז, כריתת אונה זנבית לפרוסקופית היא אחת מכריתות הכבד הקשות ביותר, הדורשת מיומנות וניסיון גבוהים. דיווחנו על מקרה מוצלח של כריתת חצי הכבד השמאלית לפרוסקופית בשילוב עם כריתת אונה זנבית לטיפול באונה הזנבית ICC. המטופל שוחרר ללא סיבוכים לאחר הניתוח. שיפרנו את הבטיחות וההיתכנות של ההליך הכירורגי על ידי חידוד טכניקות מסוימות לאורך הניתוח. הערכה מקיפה לפני הניתוח ותכנון כירורגי קפדני הם בעלי חשיבות עליונה. השתמשנו בחסימה המיהפטית מתמשכת בשילוב עם תמרון פרינגל לסירוגין, התוחם את מישור הכריתה באמצעות תיחום איסכמי, ובכך מייעל את שימור תפקודי הכבד הנותרים וממזער את אובדן הדם תוך הניתוח. באופן מכריע, שילבנו מספר גישות כירורגיות כדי להקל על חשיפה טובה יותר של האונה הזנבית בכבד ומבני כלי הדם הקריטיים הסובבים אותה, מה שמבטיח ראייה אנטומית ברורה יותר ומשפר את הבטיחות הכירורגית הכוללת.
בשל מספר גורמים כמו כריתה מאתגרת לכריתת מקטע כבד משולבת או אפילו כריתה למחצה של הכבד, חדירת כלי דם של הגידול והצורך בדיסקציה של בלוטות הלימפה, אימוץ הטיפול בלפרוסקופיה ל-ICC, בהשוואה לקרצינומה של הכבד, התעכב יחסית. עם זאת, כריתה לפרוסקופית עבור ICC הראתה תוצאות טובות יותר לטווח קצר ותוצאות דומות לטווח ארוך בהשוואה לגישה הלפרוטומית18. הסיבה לכך היא שלפרוסקופיה יכולה לספק מגוון גישות כירורגיות, המאפשרות חשיפה ושליטה טובה יותר בכלי דם חיוניים. יתר על כן, קל להבחין בגרורות השתלת בטן במהלך חקירה לפרוסקופית, מה שהופך את שלב הגידול למדויק יותר. בנוסף, ניתן לזהות נגעים נסתרים בכבד גם במהלך ניתוח לפרוסקופי באמצעות צביעה פלואורסצנטית או אולטרסאונד תוך ניתוחי19. מטא-אנליזות שנערכו לאחרונה20 הצביעו על כך שלכריתת אונה זנבית לפרוסקופית יש יתרונות מרובים על פני ניתוח פתוח, במיוחד איבוד דם תוך ניתוחי ואשפוז. שני מחקרים 21,22 על הטיפול ב-ICC הציעו כי כריתה לפרוסקופית של האונה הזנבית היא הליך אפשרי ובטוח. עם זאת, יש צורך במחקרים נוספים כדי לבסס את היתרונות האמיתיים של לפרוסקופיה מכיוון שכריתת המיהפטקטומיה השמאלית הלפרוסקופית בשילוב עם ניתוח רדיקלי של האונה הזנבית לטיפול באונה הזנבית ICC עדיין נדירה יחסית.
קביעת השוליים הימניים של האונה הזנבית היא מאתגרת ביותר. הגישה המסורתית היא להשתמש בפדיקל גליסון האחורי הימני כמישור הגחון הימני של האונה הזנבית ולהשתמש ב-IVC כנקודת ייחוס למעבר פרנכימת הכבד בין ורידי הכבד האמצעיים והימניים על מנת לקבוע את הגבול הנכון לכריתת אונה זנבית פשוטה. עם זאת, חשוב לציין שהחלטות כירורגיות לא צריכות להתבסס אך ורק על מישור רעיוני זה. Kogure et al.23 הדגישו כי ורידי הכבד מתוחמים על ידי הכבד הימני ותהליך הזנב. Kumon et al.24 הציעו כי ורידי הכבד הקצרים בחלק הפרוואול משמשים כגבולות, אך אלה יכולים להיות מאתגרים לניתוח תוך ניתוחי. Ho et al.25 קבעו גבול בין התהליך הזנבי לאונה האחורית באמצעות חסימה של עוקץ הכבד התחתון הימני. רוב החוקרים26 חושבים שהמישור הפרה-וונטרלי הימני משמש בדרך כלל להגדרת השוליים הימניים של האונה הזנבית, מה שמתיישב עם הגישה הכירורגית המתוארת כאן.
קיימת מחלוקת האם דיסקציה של בלוטות הלימפה נחוצה במהלך ניתוח רדיקלי לחולים עם כולנגיוקרצינומה. למרות שבלוטות לימפה גרורתיות קשורות לערך פרוגנוסטי שלילי, כריתת לימפה נרחבת אינה מבוצעת באופן שגרתי במקרים בהם בלוטות הלימפה נראות לא חשודות מבחינה מקרוסקופית8. Ratti F et al.27 ערכו מחקר שהראה כי אין הבדל משמעותי ביעילות של דיסקציה לפרוסקופית של בלוטות הלימפה בהשוואה לניתוח פתוח, וגם ההבדל ביעילות ארוכת הטווח בין השניים אינו מובהק סטטיסטית. דיסקציה לפרוסקופית של בלוטות הלימפה אינה מובילה לשכיחות מוגברת או אף נמוכה יותר של סיבוכים, ואין הבדל משמעותי במספר דיסקציה של בלוטות הלימפה בהשוואה לניתוח פתוח.
עבור חולים עם ICC של אונה זנבית הניתנת לכריתה, כריתת אונה זנבית לפרוסקופית, או אפילו כריתה משולבת של מקטעי כבד אחרים, שהיא בטוחה ואפשרית, מייצגת הזדמנות טיפולית יקרת ערך. עם זאת, יש צורך במחקר נוסף כדי להבהיר את היעילות ארוכת הטווח של הניתוח, לקבוע את השוליים המתאימים לכריתה של האונה הזנבית ולהעריך האם יש צורך בדיסקציה של בלוטות הלימפה.
Disclosures
למחברים אין ניגודי אינטרסים לחשוף.
Acknowledgements
אנו מודים לרופאים המרדימים ולאחיות חדר הניתוח שסייעו בניתוח.
Materials
| Name | Company | Catalog Number | Comments |
| Bipolar radiofrequency excision hemostatic device | ERBE | 20195-136 | |
| Disposable trocar | Kangji Medical | 101Y.611 | |
| Endoscopic linear cutter reloads | Ethicon, LLC | ECR60W | |
| Laparoscopic system | STORZ | 26003BA | |
| Laparoscopic system | STORZ | TC200 | |
| Non-absorbable polymer ligation clips (Hem-o-lok) | Teleflex Medical | 544240 | |
| Pneumoperitoneum needle | Kangji Medical | 101Y.611 | |
| Ultrasound knife | Johnson | GEN11 | |
| Video system | SONY | LMD-3252SC |
References
- Rebecca, L., Angela, N. S., Ahmedin, G., , J. Cancer statistics, 2024. CA Cancer J Clin. 74 (1), 12-49 (2024).
- Paramita, D., et al. Global trends in incidence rates of primary adult liver cancers: A systematic review and meta-analysis. Front Oncol. 10, 171 (2020).
- Dimitrios, M., et al. Advances in the treatment of intrahepatic cholangiocarcinoma: An overview of the current and future therapeutic landscape for clinicians. CA Cancer J Clin. 73 (2), 198-222 (2022).
- Nuzzo, G., Giuliante, F., Ardito, F., Giovannini, I. Intrahepatic cholangiocarcinoma. Ann Surg. 249 (3), 541-542 (2009).
- Jiang, J. H., Fang, D. Z., Hu, Y. T. Influence of surgical margin width on survival rate after resection of intrahepatic cholangiocarcinoma: A systematic review and meta-analysis. BMJ Open. 13 (5), e067222 (2023).
- Dai, Y. S., et al. The influence of resection margin width in patients with intrahepatic cholangiocarcinoma: A meta-analysis. World J Surg Oncol. 21 (1), 16 (2023).
- Zhu, H., et al. Prognostic value of resection margin length after surgical resection for intrahepatic cholangiocarcinoma. Am J Surg. 222 (2), 383-389 (2021).
- Lauterio, A., et al. Current surgical management of peri-hilar and intra-hepatic cholangiocarcinoma. Cancers (Basel). 13 (15), 3657 (2021).
- Jiang, N., et al. Patterns of caudate lobe invasion of hilar cholangiocarcinoma: A panoramic histologic study of liver. Ann Surg Oncol. 29 (11), 6804-6812 (2022).
- Si, A., et al. Impact of anatomical versus non-anatomical liver resection on short- and long-term outcomes for patients with intrahepatic cholangiocarcinoma. Ann Surg Oncol. 26 (6), 1841-1850 (2019).
- Wang, C., et al. Anatomical resection improved the outcome of intrahepatic cholangiocarcinoma: A propensity score matching analysis of a retrospective cohort. J Oncol. 2022, 4446243 (2022).
- Huang, J., Sun, D., Xu, D., Zhang, Y., Hu, M. A comprehensive study and extensive review of the caudate lobe: The last piece of "jigsaw" puzzle. Asian J Surg. 47 (1), 1-7 (2024).
- Parikh, M., Han, H. S., Cho, J. Y., D'silva, M. Laparoscopic isolated caudate lobe resection. Sci Rep. 11 (1), 4328 (2021).
- Guo, L., et al. An inferior vena cava-priority approach in laparoscopic isolated hepatic caudate lobectomy. Langenbecks Arch Surg. 409 (1), 106 (2024).
- Wang, Z., et al. Laparoscopic right hemi-hepatectomy plus total caudate lobectomy for perihilar cholangiocarcinoma via anterior approach with augmented reality navigation: A feasibility study. Surg Endosc. 37 (10), 8156-8164 (2023).
- Chun, Y. S., Pawlik, T. M., Vauthey, J. N. 8th edition of the AJCC cancer staging manual: Pancreas and hepatobiliary cancers. Ann Surg Oncol. 25 (4), 845-847 (2018).
- Wang, D., et al. The value of total caudate lobe resection for hilar cholangiocarcinoma: A systematic review. Int J Surg. 110 (1), 385-394 (2024).
- Ratti, F., et al. Intrahepatic cholangiocarcinoma as the new field of implementation of laparoscopic liver resection programs. A comparative propensity score-based analysis of open and laparoscopic liver resections. Surg Endosc. 35 (4), 1851-1862 (2021).
- Dorovinis, P., et al. Safety and efficacy of laparoscopic caudate lobectomy: A systematic review. J Clin Med. 10 (21), 4907 (2021).
- Ding, Z., et al. Safety and feasibility for laparoscopic versus open caudate lobe resection: A meta-analysis. Langenbecks Arch Surg. 406 (5), 1307-1316 (2021).
- Wan, H. F., et al. Laparoscopic caudate lobectomy for cholangiocarcinoma of caudate lobe invading middle hepatic vein. Ann Surg Oncol. 27 (11), 4181-4185 (2020).
- Hu, Y. F., Hu, H. J., Ma, W. J., Jin, Y. W., Li, F. Y. Laparoscopic versus open liver resection for intrahepatic cholangiocarcinoma: A systematic review of propensity score-matched studies. Updates Surg. 75 (8), 2049-2061 (2023).
- Kogure, K., et al. The caudate processus hepatic vein: A boundary hepatic vein between the caudate lobe and the right liver. Ann Surg. 247 (2), 288-293 (2008).
- Kumon, M., et al. Definition of the caudate lobe of the liver based on portal segmentation. Glob Health Med. 2 (5), 328-336 (2020).
- Ho, K. M., et al. Laparoscopic total caudate lobectomy for hepatocellular carcinoma. J Laparoendosc Adv Surg Tech A. 27 (10), 1074-1078 (2017).
- Shen, X. Y., et al. Can we delineate preoperatively the right and ventral margins of caudate lobe of the liver. Ann Surg Treat Res. 97 (3), 124-129 (2019).
- Ratti, F., et al. Perioperative and long-term outcomes of laparoscopic versus open lymphadenectomy for biliary tumors: A propensity-score-based, case-matched analysis. Ann Surg Oncol. 26 (2), 564-575 (2019).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved