Method Article
Localización de objetivos funcionales específicos para la estimulación magnética transcraneal en ausencia de equipos de navegación
* Estos autores han contribuido por igual
En este artículo
Resumen
Este artículo describe cómo localizar objetivos específicos de la función para intervenciones o tratamientos repetitivos de estimulación magnética transcraneal cuando el equipo de navegación no está disponible.
Resumen
La estimulación magnética transcraneal repetitiva (EMTr) es una técnica no invasiva que modula la actividad neuronal en el cerebro. Los estudios han demostrado que la EMTr puede regular la plasticidad neuronal, promover la reorganización de la red neuronal y se ha aplicado ampliamente a trastornos neuropsiquiátricos como el accidente cerebrovascular. Aunque algunos estudios sugieren que la EMTr puede ayudar en la rehabilitación del accidente cerebrovascular, su eficacia sigue siendo incierta, posiblemente debido a las limitaciones en la localización tradicional del punto caliente del motor de la mano.
El punto caliente motor de la mano está determinado por los potenciales evocados motores (MEP), que reflejan la conductividad del tracto corticoespinal o piramidal, lo que representa el movimiento no voluntario. Por el contrario, los puntos de activación de la resonancia magnética funcional (fMRI) de una tarea motora definen objetivos específicos de la función, que involucran tanto la percepción como la ejecución motora, lo que representa el movimiento voluntario. Con base en esto, proponemos el concepto de objetivos específicos de la función, objetivos identificados a través de técnicas de imágenes cerebrales dirigidas a funciones específicas. Los objetivos específicos de la función exhiben una conectividad funcional más fuerte y extensa con las regiones del cerebro relacionadas con la cognición motora, lo que podría ofrecer efectos reguladores más efectivos que los puntos calientes.
Exploramos y validamos los efectos moduladores de las dianas específicas de la función en un estudio previo. Sin embargo, las instituciones que carecen de equipos de navegación no pueden utilizar estos objetivos específicos de la función. Por lo tanto, hemos desarrollado un método de localización no navegado para objetivos específicos de la función, diseñado específicamente para definir y localizar objetivos de rTMS en el hemisferio ipsilateral posterior al accidente cerebrovascular, abordando los desafíos que enfrentan las instituciones que carecen de equipos de navegación cuando aplican rTMS dirigidos específicos de la función.
Introducción
La estimulación magnética transcraneal repetitiva (EMTr) es una técnica de neuromodulación no invasiva que puede regular la actividad cerebral y se ha utilizado ampliamente en el tratamiento de trastornos neuropsiquiátricos, como en la rehabilitación de la disfunción motora de la mano en pacientes con accidente cerebrovascular. Algunos estudios han demostrado que la EMTr tiene efectos terapéuticos sobre las secuelas posteriores al ictus 1,2,3, pero su eficacia sigue siendo incierta. Una razón clave de esta incertidumbre es la dificultad para identificar objetivos de estimulación precisos. Los estudios de EMT dirigidos a la función motora a menudo se basan en el sistema internacional de electroencefalograma 10-20 para la localización, utilizando C3/C4 como objetivos de estimulación, o emplean objetivos individualizados, como el punto caliente motor de la mano. Sin embargo, estos métodos no pueden determinar con precisión las áreas corticales afectadas por la EMT. La EMTr dirigida guiada por resonancia magnética magnética funcional (fMRI) se ha utilizado ampliamente en el tratamiento de la depresión.
Nuestra investigación previa también exploró su aplicación en el tratamiento del síndrome de Tourette mediante la estimulación del área motora suplementaria4, pero aún no se ha aplicado al área motora primaria (M1). En el caso de la EMTr, M1 se distingue de otras regiones del cerebro porque contiene el punto caliente del motor de la mano. Las contracciones musculares inducidas por la EMT representan movimientos involuntarios, que reflejan la conducción de arriba hacia abajo a través de los tractos corticoespinales o piramidales. Por el contrario, los vóxeles máximos de activación definidos por la resonancia magnética funcional durante las tareas de golpeteo con los dedos están más conectados funcionalmente con las regiones del cerebro involucradas en la cognición motora, lo que representa movimientosvoluntarios. Por lo tanto, cuando se tratan los trastornos del movimiento, el uso de la "activación" relacionada con la tarea definida por la fMRI como objetivos específicos de la función puede conducir a mejores resultados terapéuticos 5,6. En nuestro trabajo anterior, comparamos los patrones de activación cerebral entre la tarea guiada visualmente y la tarea autoiniciada mediante resonancia magnética funcional y determinamos que la tarea autoiniciada se alinea más estrechamente con los requisitos del entrenamiento de rehabilitación activa6. Confirmamos este hallazgo mediante el reanálisis de un subconjunto de datos del estudio original (Figura 1).
Apuntar con precisión a áreas específicas de la función cerebral requiere herramientas de navegación precisas. Sin embargo, los sistemas actuales no solo son engorrosos de operar y limitados en funcionalidad, sino que los calibradores montados en la cabeza a menudo no permanecen estables durante los procedimientos, son propensos a cambiar y son costosos, a veces cuestan hasta un millón de yuanes chinos (CNY), aproximadamente 140,000 dólares estadounidenses (USD). Según una encuesta sobre los patrones de uso entre las instituciones miembros del Consorcio de Medicina de Precisión para la Terapia de Estimulación Magnética Transcraneal Guiada por Imágenes (PRECISE), estos inconvenientes han llevado a que las tecnologías de navegación se utilicen en menos del 5% de la investigación y la práctica clínica de TMS en China, a pesar de sus beneficios potenciales. Sin embargo, lo más importante es que estos sistemas solo se enfocan en "localizar" los sitios de estimulación sin abordar el problema crítico de "definir" el objetivo, es decir, seleccionar el área más apropiada para la estimulación. Dados los altos costos, la complejidad operativa y las demandas de tiempo, esta es la razón por la que estos dispositivos aún no han logrado una adopción clínica generalizada.
Para abordar el desafío de usar objetivos específicos de la función sin dispositivos de navegación, exploramos el método de rTMS dirigido y no navegado. Mediante el uso de fMRI, identificamos objetivos específicos de la función en la corteza motora y los proyectamos en la superficie del cuero cabelludo, lo que permitió la definición y localización de objetivos sin necesidad de equipo de navegación7. Si bien la EMTr no navegada no proporciona monitoreo en tiempo real durante todo el proceso, aborda los problemas de precisión en la localización de objetivos en condiciones clínicas donde los dispositivos de navegación no están disponibles. Este artículo profundiza en la justificación general del estudio y describe el proceso experimental completo, con un enfoque particular en la comparación de los efectos de los objetivos específicos de la función en la función cerebral en condiciones navegadas y no navegadas. Para verificar la viabilidad de la EMTr dirigida a la función específica, el estudio actual solo incluyó individuos sanos.
Protocolo
Este trabajo ha sido aprobado por el Comité de Ética de la Universidad Deportiva de Chengdu, y todos los participantes han dado su consentimiento informado por escrito (Figura 2). Este protocolo describe la EMTr dirigida específica de la función no navegada frente a la navegada.
1. Reclutamiento de participantes
- Reclutó a 10 participantes adultos diestros sanos (de 22 a 29 años, con 5 mujeres y 5 hombres; edad promedio de 24 ± 2 años). Excluir a un participante debido a un movimiento de la cabeza superior a 2,5 mm en traslación o 2,5 ° en rotación. Por último, incluir a 9 participantes en el análisis estadístico.
- Criterios de inclusión
- Reclutar participantes de 18 a 30 años, que sean diestros, que pasen las pruebas de seguridad de MRI y TMS, y que no tengan antecedentes de epilepsia u otros trastornos neurológicos o psiquiátricos.
- Asegúrese de que los participantes cumplan con criterios adicionales, como que no haya contraindicaciones para la resonancia magnética, que no haya antecedentes de lesiones cerebrales o enfermedades cardíacas graves, y que no estén tomando medicamentos antiepilépticos o anticoagulantes.
- Reclute participantes que no tengan trastornos de la conciencia, que no tengan objetos metálicos en el cuerpo (como marcapasos, implantes dentales metálicos o dispositivos intrauterinos), que no tengan claustrofobia grave ni embarazo, y cuya visión sea normal o esté corregida a la normalidad.
- Criterios de inclusión
- Criterios de exclusión de datos posteriores al experimento
- Excluya los datos de los participantes que no puedan completar el experimento o cuyo movimiento de la cabeza durante la exploración por resonancia magnética funcional supere los 2,5 mm de traslación o los 2,5° de rotación.
- Directrices para los participantes antes del experimento
- Asegúrese de que todos los participantes hayan firmado el formulario de consentimiento informado, que explica el propósito de la investigación, los procedimientos experimentales y los posibles efectos secundarios y riesgos involucrados.
- Realizar controles de seguridad para los participantes.
- Explique los procedimientos experimentales y las precauciones para garantizar la ejecución sin problemas del experimento.
- Aconseje a los participantes que eviten el alcohol, el café o el ejercicio vigoroso antes del experimento.
- Recuerde a los participantes que duerman lo suficiente y eviten quedarse despiertos hasta tarde.
2. Adquisición de datos de resonancia magnética funcional
NOTA: Todos los participantes se someten a una resonancia magnética en el Centro de Imágenes Cerebrales por Resonancia Magnética en el campus de Qingshuihe de la Universidad de Ciencia y Tecnología Electrónica de China, utilizando un escáner GE MR750 de 3T. Cada sesión de exploración incluye una imagen estructural ponderada en T1, una resonancia magnética funcional en estado de reposo (RS-fMRI) de 8 minutos y una resonancia magnética funcional Task-fMRI de 4 minutos. Los participantes reciben dos intervenciones de EMTr: una con navegación y otra sin ella, con un intervalo de 1 semana entre sesiones para eliminar los efectos residuales. Realizar resonancias magnéticas antes y después de cada intervención, con un total de cuatro exploraciones.
NOTA: Contrarreste la secuencia de las condiciones navegadas y no navegadas entre los participantes.
- Procedimientos de escaneo
- Antes de ingresar a la sala de resonancia magnética, coloque tapones para los oídos en los participantes para reducir el ruido y asegurarse de que se hayan retirado todos los objetos metálicos.
- Explique las tareas que los participantes deben realizar durante el escaneo.
- Asegúrese de que los participantes se acuesten en decúbito supino en la cama de exploración, con la cabeza firmemente fijada con almohadillas de espuma para minimizar el movimiento de la cabeza.
- Durante la exploración RS-fMRI, indique a los participantes que cierren los ojos, eviten el pensamiento deliberado y permanezcan despiertos para evitar quedarse dormidos.
- Exporte manualmente las imágenes a la unidad de red designada o al dispositivo de almacenamiento externo.
- Parámetros de escaneo
- Utilice los siguientes parámetros de exploración RS-fMRI: tiempo de repetición (TR) = 2.000 ms, tiempo de eco (TE) = 30 ms, ángulo de giro (FA) = 90°, campo de visión (FOV) = 220 mm × 220 mm, matriz = 64 x 64, grosor/espacio de corte = 3,4 mm/0 mm, con 41 cortes en total, cubriendo todo el cerebro, y 240 puntos de tiempo recopilados.
- Utilice los siguientes parámetros de escaneo de imágenes estructurales ponderadas en T1: secuencia de eco recordado en gradiente estropeado (SPRG), exploración sagital TR/TE = 8,2 ms/2,98 ms, FA = 8°, FOV = 256 mm x 256 mm, matriz = 256 x 256, grosor/espacio de corte = 1 mm/0 mm, con 166 cortes que cubren todo el cerebro.
- Utilice parámetros de exploración de task-fMRI que sean idénticos a los de la RS-fMRI, excepto que solo se recopilan 120 puntos de tiempo.
- Detalles de la ejecución de tareas
- Coloque a los participantes con las palmas de las manos hacia arriba y sosteniendo una caja de botones.
- Coloque toallas entre las cabezas de los participantes y la bobina para estabilizar sus cabezas y minimizar el movimiento.
- Diseño de bloques, tarea autoiniciada (4 min): Cuando aparezca una imagen de un "+" en la pantalla, pida a los participantes que descansen. Cuando aparezca una imagen de un reloj en la pantalla, indique al participante que presione el botón con el pulgar derecho cada 2 segundos, cronometrándolo él mismo (Figura suplementaria S1).
3. Medición del umbral del motor en reposo (RMT)
NOTA: Utilice la electromiografía de superficie (EMG) para registrar la amplitud del potencial evocado motorizado (MEP) del músculo abductor corto del pulgar derecho (APB), utilizando una bobina en forma de ocho de 70 mm conectada al estimulador Magstim Super Rapid2 para medir RMT con estimulación de pulso único.
- Retire todos los objetos metálicos antes de la prueba para evitar interferencias y garantizar la seguridad.
- Pida a los participantes que se sienten en una silla y se relajen por completo.
- Aplicar exfoliante y alcohol al 75% en las manos de los participantes.
- Coloque electrodos de superficie de plata/cloruro de plata (Ag/AgCl) en el abdomen muscular.
- Coloque el electrodo de referencia en la articulación metacarpofalángica, asegurándose de que la distancia entre electrodos esté entre 20 mm y 30 mm.
NOTA: Parámetros relevantes: Utilice electrodos con un diámetro de 9 mm para las mediciones. La señal EMG del músculo APB se amplifica 1.000 veces, se filtra entre 20 Hz y 2,5 kHz, y luego se digitaliza a través de una interfaz microdigital a una frecuencia de muestreo de 5 kHz. A continuación, los datos se almacenan en un ordenador y se muestran en una pantalla. - Cargue la imagen estructural T1 del individuo. Coloque la bobina sobre el área motora primaria contralateral, específicamente en la "rodilla media" del surco central, también conocida como la "perilla de la mano", que representa el área de la mano en la corteza motora primaria.
NOTA: Confirme la relajación muscular tanto visualmente como a través de la monitorización EMG. - Mueva la bobina alrededor de la "perilla manual" en incrementos de 0,5 cm.
- Coloque el mango en un ángulo de 45° con respecto al plano sagital medio para medir el MEP.
- Comience con una intensidad de estimulación por debajo del umbral, aumentándola en un 5% de la producción máxima de estímulo cada vez. Cuando la amplitud de pico a pico del MEP supere los 50 μV, disminuya la intensidad de la estimulación de forma escalonada en un 1% de la salida máxima.
- Registre la intensidad mínima de estimulación que evoca al menos cinco MEP mayores o iguales a 50 μV en 10 estimulaciones consecutivas de un solo pulso como RMT, con esta ubicación identificada como el punto caliente. Si no se puede determinar un punto caliente después de seis estimulaciones, mueva la bobina a la siguiente ubicación.
4. EMTr dirigida a funciones específicas de la función
- Defina el objetivo específico de la función individualizada.
- Después de abrir el software de preprocesamiento, haga clic en DPARSF 5.4 y, a continuación, seleccione DPARSF Advanced Edition para preprocesar los datos de estado de la tarea utilizando los parámetros específicos que se muestran en el archivo complementario 1. Realice correcciones de temporización de cortes y movimiento de cabezal. Correlacione el registro de las imágenes funcionales con imágenes estructurales y aplique un suavizado espacial con un ancho completo a la mitad del máximo (FWHM) de 6 mm.
NOTA: Ajuste los parámetros específicos de acuerdo con el modelo de máquina o la tarea de escaneo. - Abra SPM12 y haga clic en Coregister Estimate. Para la imagen de referencia, seleccione el archivo llamado "sub*crop_1.nii" de la carpeta T1Img. Para la imagen de origen, elija el archivo "mean*.nii" de la carpeta RealignParameter. Para la otra imagen, seleccione el archivo "ra*.nii" de la carpeta FunImgAR.
NOTA: Utilice el archivo de imagen funcional generado después de la corrección de movimiento y la corrección de tiempo de corte como la "Otra imagen". Se pueden seleccionar archivos alternativos en función del objetivo de la investigación. - Haga clic en Segmento | Volumes y seleccione el archivo llamado "sub*crop_1.nii" de la carpeta T1Img. En Campos de deformación, seleccione Invertir + Adelante y, a continuación, haga clic en Ejecutar. Repita este proceso para segmentar el archivo "sub*.nii" de la carpeta T1Img.
NOTA: Segmento "sub*crop_1.nii" para calcular el punto de activación de la tarea individual. Segmente "sub*.nii" para transformar la máscara de espacio estándar en espacio individual. - Haga clic en Suavizar, seleccione los archivos "ra*.nii" de la carpeta FunImgAR para la opción Imagen a suavizar e ingrese 6 6 6 en el campo FWHM .
- Realice análisis de primer nivel para obtener mapas de activación individuales e identificar el vóxel máximo de activación como objetivo de estimulación. Incluya los tres pasos siguientes:
- Cree una nueva carpeta llamada "indiv_act" y haga clic en Especificar 1er nivel. En el campo Directorio , seleccione la carpeta "indiv_act", haga clic en Unidades para diseño, elija Escaneos e ingrese 2 para el intervalo entre escaneos. En la sección Datos y diseño , seleccione los archivos "sra*.nii" en Escaneos; en la sección Condición , establezca el Nombre en pulsar (nombre personalizado), escriba 0 30 60 90 para el Inicio y establezca las Duraciones en 15. Haga clic en Varios regresores y seleccione el archivo "rp_a*.txt" de RealignParameters.
NOTA: Complete la información de inicio y duración de acuerdo con el diseño experimental real. - Estimación: En "Seleccionar SPM.mat", elija el archivo "SPM.mat" de la carpeta "indiv_act" y genere el mapa de activación de tarea individual, "spmT_0001".
- Haga clic en Resultados, seleccione el archivo "SPM.mat" de la carpeta "indiv_act", marque t-contrast y haga clic en Definir nuevo contraste. Introduzca un nombre personalizado en el campo de nombre, introduzca 1 0 en el campo de contraste , haga clic en Enviar | DE ACUERDO | Hecho. En Aplicar enmascaramiento, seleccione Ninguno; en Ajuste de valor p para control, elija Ninguno, con un valor de 0,001; Establezca el valor del umbral & extend en 0.
- Cree una nueva carpeta llamada "indiv_act" y haga clic en Especificar 1er nivel. En el campo Directorio , seleccione la carpeta "indiv_act", haga clic en Unidades para diseño, elija Escaneos e ingrese 2 para el intervalo entre escaneos. En la sección Datos y diseño , seleccione los archivos "sra*.nii" en Escaneos; en la sección Condición , establezca el Nombre en pulsar (nombre personalizado), escriba 0 30 60 90 para el Inicio y establezca las Duraciones en 15. Haga clic en Varios regresores y seleccione el archivo "rp_a*.txt" de RealignParameters.
- Haga clic en Normalizar (escribir) | Datos. En Campos de deformación, seleccione el archivo "iy_Crop_1" de la carpeta T1Img. En Imagen para escribir, elija la máscara de región cerebral M1. Introduzca los tamaños individuales de cuadro delimitador y vóxel.
NOTA: Introduzca los tamaños de cuadro delimitador y vóxel en función de las características específicas de los datos. - Haga clic en Correa (Rebanar), luego seleccione spmT_0001 de la carpeta "indiv_act" para Espacio de definición de imagen. Para Image to Reslice, elija el archivo "w*.nii" generado en el paso 4.1.6.
- Calcule el pico de activación de tareas individuales: en MATLAB, ejecute el código positivo de ordenación . Para InputName1, seleccione la ruta del archivo "rw*.nii" generado en el paso 4.1.7; para InputName2, seleccione la ruta del archivo "spmT_0001" de la carpeta "indiv_act"; en InputName3, seleccione la ruta de acceso de la carpeta de salida. La primera coordenada X con un valor negativo (el hemisferio izquierdo) en los resultados ordenados es el pico de activación de la tarea individual; Registre las coordenadas de este punto.
- Después de abrir el software de preprocesamiento, haga clic en DPARSF 5.4 y, a continuación, seleccione DPARSF Advanced Edition para preprocesar los datos de estado de la tarea utilizando los parámetros específicos que se muestran en el archivo complementario 1. Realice correcciones de temporización de cortes y movimiento de cabezal. Correlacione el registro de las imágenes funcionales con imágenes estructurales y aplique un suavizado espacial con un ancho completo a la mitad del máximo (FWHM) de 6 mm.
- Localice el destino específico de la función individualizada (navegado).
- Determine la intensidad de salida del estimulador en función del RMT del participante.
- Emplear un sistema de neuronavegación de seguimiento óptico estereotáctico sin marco, con el participante sentado cómodamente y usando un calibrador montado en la cabeza.
- Haga clic en la opción anatómica : Importar las imágenes estructurales ponderadas en T1 del participante en el sistema de navegación para el modelado de la cabeza.
- Haga clic en la opción Reconstrucción : Reconstruir la piel en la imagen.
- Haga clic en la opción Puntos de referencia : Utilice la herramienta de localización para marcar cuatro puntos de referencia (la nasión, la punta de la nariz y los puntos preauriculares a ambos lados) en la cabeza.
- Haga clic en la opción Objetivo : Identifique y establezca la trayectoria del objetivo en la región del cerebro. Localice el objetivo de estimulación en las imágenes individuales del participante. Después de colocarlo, mueva el objetivo para alinearlo con el punto de mira. Localización completa de TMS.
NOTA: Haga la bobina tangente al cuero cabelludo y alinee el foco de estimulación con el objetivo.
- Localice el destino específico de la función individualizada (no navegado).
NOTA: Todo el código para la localización del objetivo del cuero cabelludo se proporciona en Legajo Complementario 2.- Utilice SPM12 para segmentar la plantilla cerebral estándar del Instituto Neurológico de Montreal (MNI) (mni_icbm152_t1_tal_nlin_asym_09c.nii, ubicada en la carpeta Plantillas de DPABI) para obtener la mascarilla estándar para el cuero cabelludo. Los pasos específicos son los siguientes:
- Abra SPM12, haga clic en fMRI y, a continuación, seleccione Segmento en el menú emergente. En la interfaz de parámetros , haga clic en el botón Volúmenes , seleccione el archivo de plantilla de cerebro estándar (es decir, la plantilla de cerebro MNI) de la opción Volúmenes , y luego haga clic en Campos de deformación para seleccionar Inversa + Adelante.
- Delinee los bordes interiores y exteriores del cuero cabelludo estándar: en MATLAB, ejecute los bordes del código. En la ventana emergente, seleccione la imagen c5.nii , haga clic en Listo y genere el archivo "c5_edges.nii".
- Delinee la imagen del borde más externo del cuero cabelludo estándar: en MATLAB, ejecute el código outer_edge . En la interfaz emergente, seleccione el archivo c5_edges.nii y haga clic en Listo para generar el archivo "c5_outer_edge.nii", que representa el límite del cuero cabelludo en el espacio estándar.
- Utilice SPM12 para transformar el borde estándar del cuero cabelludo en un espacio individual. En la interfaz del menú , haga clic en Normalizar (Escribir) y, a continuación, en la interfaz de parámetros , haga clic en Datos. En Campos de deformación, seleccione el archivo iy_sub*.nii de la carpeta T1Img. Elija c5_outer_edge.nii para Imágenes para escribir e introduzca los tamaños individuales del cuadro delimitador y del vóxel.
- Convertir coordenadas corticales en coordenadas scalp: abra el código TransCortex2Scalp en MATLAB y ejecute la primera línea. En la interfaz emergente, introduzca las coordenadas del punto de activación de cada tarea y seleccione el archivo wc5_outer_edge.nii . Registre las coordenadas del cuero cabelludo.
- Abra DPABI_Viewer, haga clic en Capa subyacente y seleccione la imagen estructural T1 individual. Localice y registre las coordenadas de los cuatro puntos de referencia: los picos auriculares izquierdo y derecho, la nación y el inion.
- Defina el origen del cuero cabelludo: abra el código de intersección en MATLAB. En el editor, introduzca las coordenadas de los cuatro puntos de referencia en sus posiciones especificadas. Ejecute el código para calcular las coordenadas de intersección de la línea que conecta las puntas de los oídos izquierdo y derecho con la línea que conecta el nasion y el inion, luego registre las coordenadas.
- Mover el punto de intersección a lo largo del eje Z hasta el cuero cabelludo: Abra el código de origen en MATLAB. Introduzca las coordenadas del punto de intersección en la posición Definir punto H en el editor. Ejecute el código, luego seleccione el archivo wc5_outer_edge.nii en la ventana emergente para obtener las coordenadas de origen del cuero cabelludo O.
- Dibuja una línea que conecte las dos puntas de las orejas para definir el eje X, y una línea que conecte el nasion y la protuberancia occipital externa para definir el eje Y. El eje perpendicular a ambos define el eje Z. El plano bidimensional formado por el eje XY es el plano XY.
- Calcule la distancia real desde el origen del cuero cabelludo O hasta cada punto: Ejecute el código de distancia , seleccione el archivo wc5_outer_edge en la interfaz emergente y, en la ventana de comandos , siga las instrucciones para ingresar el origen del cuero cabelludo, el objetivo del cuero cabelludo y los cuatro puntos de referencia.
NOTA: "Cada punto" se refiere a los cuatro puntos de referencia del cuero cabelludo en el paso 4.3.4 y al objetivo del cuero cabelludo. Este código solo puede calcular la distancia del arco entre un punto y otro a la vez. Para calcular la distancia entre un par de puntos diferente, debe volver a ejecutar el código. - Calcule el ángulo entre la línea que conecta el objetivo del cuero cabelludo y el origen del cuero cabelludo y el eje X en el plano XY: Abra el calculate_angle_X_axis de código y ejecute la primera línea. En la ventana de comandos , introduzca las coordenadas del origen del cuero cabelludo y el objetivo de estimulación según se le indique.
- Utilice la regla de orientación (como se muestra en la figura 3) para fijar la posición de la regla suave correspondiente en función de la distancia y el ángulo calculados en los pasos anteriores. Marca el cuero cabelludo con un bolígrafo lavable. Completar la localización del objetivo de estimulación del cuero cabelludo (Figura 4).
- Utilice SPM12 para segmentar la plantilla cerebral estándar del Instituto Neurológico de Montreal (MNI) (mni_icbm152_t1_tal_nlin_asym_09c.nii, ubicada en la carpeta Plantillas de DPABI) para obtener la mascarilla estándar para el cuero cabelludo. Los pasos específicos son los siguientes:
- EMTr
- Seleccione el modo repetitivo para establecer los parámetros de estimulación, incluida la intensidad de la estimulación, la frecuencia (10 Hz), la duración (3 s), el número de pulsos en cada tren (30 pulsos), el tiempo de espera (12 s), el número de trenes (60 trenes) y el número total de pulsos entregados por día (1.800 pulsos).
- Guarde la sesión y presione el botón Ejecutar para iniciar la estimulación.
NOTA: La intensidad de la estimulación se establece de acuerdo con el RMT del participante, que en este estudio se establece en 100% RMT. - Dentro de la media hora después de que termine la estimulación, haga que el participante se someta a otra resonancia magnética, utilizando la misma secuencia de exploración que se usó antes de la estimulación.
5. Detección del efecto modulador rTMS (procesamiento y análisis de datos de resonancia magnética)
NOTA: Utilice software de preprocesamiento para realizar el preprocesamiento de datos RS-fMRI, que incluye los siguientes pasos específicos:
- Elimine los primeros 10 puntos de tiempo para lograr el equilibrio de la señal y permitir que los participantes se adapten al ruido del escáner.
- Corrija el retardo de tiempo de adquisición entre sectores.
- Realice la corrección del movimiento de la cabeza.
NOTA: Se pueden establecer diferentes límites de movimiento de la cabeza en función de los requisitos específicos del estudio. - Normalice las imágenes funcionales al espacio MNI utilizando la plantilla EPI.
- Elimina las señales molestas, incluidas las de la materia blanca, el líquido cefalorraquídeo y seis parámetros de movimiento de la cabeza.
- Elimine las tendencias lineales.
- Aplique el filtrado de paso de banda (0,01-0,1 Hz).
- Realice el suavizado espacial utilizando un kernel gaussiano con un FWHM de 6 mm.
- Calcule las métricas de actividad cerebral después del preprocesamiento, incluida la amplitud de la fluctuación de baja frecuencia (ALFF) y la conectividad funcional (FC). Calcule las diferencias en las métricas de actividad cerebral local (ALFF y FC) entre la pre-EMTr y la post-EMTr en condiciones navegadas y no navegadas, y realice pruebas t pareadas en los mapas de diferencias (corrección GRF, vóxel p < 0,001, clúster p < 0,05).
Resultados
Los resultados de la prueba t pareada y el ANOVA de dos factores indicaron que no hubo diferencias significativas en los cambios en ALFF o FC antes y después de la EMTr tanto en condiciones navegadas como no navegadas (corrección GRF, vóxel p < 0,001, cluster p < 0,05). No se observaron diferencias significativas entre las condiciones de navegación y las de no navegación. Este resultado se alinea con nuestras expectativas, lo que indica que nuestro método de no navegación no tiene una desventaja significativa en comparación con el método de navegación. Para evitar hacer afirmaciones infundadas de que no hay diferencias significativas, presentamos aquí los mapas de la prueba t de una muestra para ambas condiciones de EMTr (sin corregir, vóxel p < 0,05) (Figura 5). Estos resultados no sobreviven a ningún tipo de ajuste de comparación múltiple, como la corrección FDR o GRF. Para evaluar la equivalencia de los cambios en la función cerebral inducidos por los métodos no navegado y navegado, se realizó un análisis de potencia utilizando la d de Cohen. Los resultados indicaron que el valor d de Cohen para ALFF fue de 0,22, mientras que el valor d de Cohen para FC fue de 0,56.

Figura 1: Resultados de las pruebas t pareadas. (A) Las diferencias entre la conectividad funcional basada en activación y la conectividad funcional basada en puntos de acceso APB (corrección GRF, p < de vóxel único 0,001, p de nivel de clúster < 0,05). (B) Las diferencias en la activación cerebral entre las tareas de golpeteo con los dedos autoiniciadas y guiadas visualmente en 25 participantes (corrección FDR, q < 0,05). (C) Las diferencias entre la conectividad funcional autoiniciada y la conectividad funcional basada en la activación del estado guiada visualmente en 35 participantes (corrección GRF, p < vóxel único 0,001, p de clúster < 0,05). La Figura 1A fue adaptada de Wang et al. (2020)5; La figura 1B,C se preparó extrayendo un subconjunto diferente de datos de Wang et al. (2023)6. Abreviaturas: APB = Abductor Pollicis Brevis; GRF = campo aleatorio gaussiano; FDR = Tasa de Falsos Descubrimientos. Haga clic aquí para ver una versión más grande de esta figura.
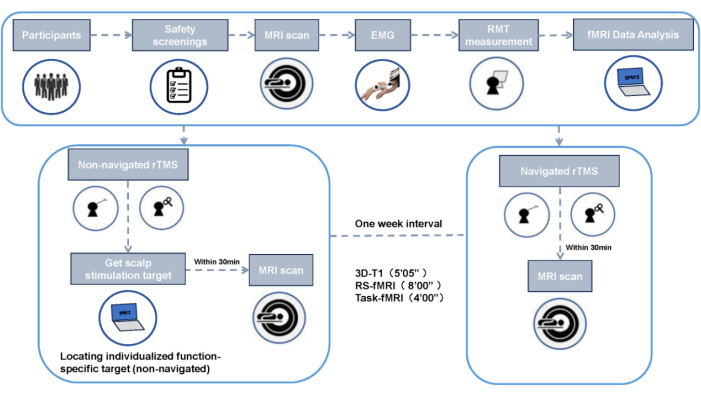
Figura 2: Diagrama de flujo del diseño experimental. Haga clic aquí para ver una versión más grande de esta figura.

Figura 3: Diagrama esquemático de la regla de segmentación. (A) Vista frontal de la regla de orientación. 1. Mango; 2. Punto de anclaje del cuero cabelludo (es decir, el origen del cuero cabelludo en el plano XY); 3. Regla de medición rígida (material acrílico); 4. Regla de medición giratoria y flexible (material de silicona). (B) Vista ampliada del punto de anclaje del cuero cabelludo (es decir, una vista ampliada de 2 en A). (C) Vista ampliada de la regla de medición flexible (es decir, vistas ampliadas de 3 y 4 en A). Haga clic aquí para ver una versión más grande de esta figura.

Figura 4: Conversión del objetivo cortical específico de la función al objetivo del cuero cabelludo específico de la función. El punto rojo representa el objetivo cortical específico de la función, el punto verde representa el objetivo del cuero cabelludo específico de la función y el punto azul indica el origen del sistema de coordenadas 2D en el cuero cabelludo. Haga clic aquí para ver una versión más grande de esta figura.

Figura 5: Resultados de las pruebas t de una muestra. (A) Efectos moduladores de la EMTr no navegada sobre la función cerebral (p < 0,05, sin corregir). (B) Efectos moduladores de la EMTr sobre la función cerebral (p < 0,05, sin corregir). Abreviaturas: FC = conectividad funcional; ALFF = amplitud de la fluctuación de baja frecuencia; EMTr = estimulación magnética transcraneal repetitiva. Haga clic aquí para ver una versión más grande de esta figura.
Archivo complementario 1: Parámetros utilizados en la edición avanzada de DPARSF, como se menciona en la sección 4.1.1 del protocolo. Haga clic aquí para descargar este archivo.
Archivo complementario 2: Carpeta zip que contiene el código MATLAB utilizado en este estudio. Haga clic aquí para descargar este archivo.
Figura complementaria S1: Tarea de golpeteo con los dedos autoiniciada. La tarea consistió en ocho bloques, cada uno con una duración de 30 s, lo que resultó en una duración total de 4 min. Haga clic aquí para descargar este archivo.
Discusión
En este estudio, proponemos el concepto de dianas específicas de función, que son regiones cerebrales asociadas a funciones específicas identificadas mediante técnicas de neuroimagen. Inspirados en estudios previos 8,9,10, desarrollamos un nuevo conjunto de herramientas 7,11,12 para localizar objetivos del cuero cabelludo correspondientes a áreas corticales específicas de la función, lo que permite una EMTr dirigida a la función específica sin necesidad de equipos de navegación. En comparación con la estimulación con equipos de navegación, no se observaron diferencias significativas en los efectos de la función cerebral. Esto sugiere que, en ciertos casos, nuestro método puede lograr un rTMS específico de la función individualizada sin la necesidad de costosos equipos de navegación.
Pasos esenciales en el protocolo experimental
Para garantizar la precisión de la localización de rTMS no navegada, el operador debe alinear la escala de la regla de orientación con los puntos de referencia del oído izquierdo y derecho, la nación y el inion. La báscula debe presionarse firmemente contra la superficie del cuero cabelludo para minimizar los errores de medición causados por el grosor del cabello. Este proceso es crucial para mejorar la precisión de la localización y garantizar una orientación precisa del sitio de estimulación.
Mejoras en el método experimental y posibles problemas técnicos
Dado que este método es una versión avanzada de una técnica previamente desarrollada11, hasta el momento no se han identificado áreas de mejora. En cuanto a los posibles problemas técnicos, las diferencias individuales en la forma del cráneo pueden dar lugar a protuberancias occipitales menos prominentes en algunos participantes, lo que podría dar lugar a errores de localización. En tales casos, se puede omitir la protuberancia occipital y se pueden utilizar otros puntos de referencia (como los marcadores de la oreja izquierda y derecha y la nasión) para la localización sin comprometer la precisión, ya que la redundancia ya se ha tenido en cuenta en la fase de desarrollo.
Limitaciones del método rTMS no navegado
La principal diferencia en comparación con la EMTr navegada es la imposibilidad de controlar la distancia relativa y la dirección de la bobina al objetivo de estimulación en tiempo real. Sin embargo, incluso con el rTMS navegado, el monitoreo en tiempo real aún requiere que los operadores experimentados realicen ajustes manuales.
Importancia del método experimental en relación con los métodos existentes
En comparación con los equipos de navegación, nuestro método no requiere un posicionamiento prolongado ni una calibración del equipo. En su lugar, los usuarios simplemente introducen los datos de la resonancia magnética en el script de código y luego calculan las distancias correspondientes a través del código, después de lo cual el posicionamiento se completa rápidamente con una herramienta de medición. Según nuestra experiencia, este método ahorra al menos 15 minutos en comparación con los complejos procedimientos involucrados en la navegación. Los equipos de navegación generalmente requieren hardware costoso y capacitación especializada, mientras que nuestro método solo requiere imágenes de resonancia magnética y cálculos estándar para lograr una localización rápida, conveniente y precisa, lo que reduce significativamente tanto los costos iniciales como la complejidad operativa.
En términos de costo, nuestra herramienta de medición ha recibido una patente de invención (ZL202411874788.9)12., que ayuda a proteger la propiedad intelectual pero no aumenta significativamente los costos de producción. El modelado 3D está actualmente en marcha, y pronto podremos imprimir la herramienta en 3D para nuestros colaboradores clínicos. Las consideraciones de costes se integraron en la fase de diseño desde el principio. Para los no colaboradores que deseen comprar la herramienta, el precio es de solo 500 CNY (aproximadamente 70 USD), que sigue siendo asequible a pesar de la protección de la patente.
Importancia y posibles aplicaciones del método en campos de investigación específicos
En los últimos años, la intervención y el tratamiento de la EMTr han ganado cada vez más popularidad tanto en el campo de la investigación como en el clínico. Como todas las técnicas terapéuticas, el desarrollo se está moviendo hacia tratamientos precisos e individualizados dirigidos a funciones específicas. Sin embargo, los sistemas y equipos de navegación son caros, y la mayoría de los hospitales de China no tienen acceso a estos dispositivos. Este método aborda el problema de la EMTr individualizada y específica de la función sin necesidad de navegación. Proyecta las coordenadas corticales del objetivo en el cuero cabelludo y utiliza una herramienta para marcar las coordenadas en la superficie del cuero cabelludo. El método de focalización cortical basado en fMRI utilizado en este enfoque es idéntico a las coordenadas objetivo de fMRI empleadas por los sistemas y equipos de navegación a nivel internacional. Aunque no puede controlar la distancia relativa y la dirección en tiempo real entre la bobina y el objetivo de estimulación, sigue ofreciendo ventajas sobre los métodos clínicos actuales de "orientación ciega" (como el uso de puntos de referencia anatómicos en la superficie de la piel o la selección del punto caliente del motor manual). Este método sirve como un enfoque de transición entre la navegación precisa en tiempo real y la "orientación ciega". Para instituciones clínicas sin sistemas y equipos de navegación, puede resolver problemas clínicos prácticos. Este método promoverá significativamente el tratamiento de precisión de la EMT guiado por fMRI, lo que conducirá al descubrimiento de objetivos de estimulación más efectivos y mejorará la eficacia de los tratamientos para diversos trastornos neurológicos y psiquiátricos.
Divulgaciones
Los autores no tienen conflictos de intereses que declarar.
Agradecimientos
Este estudio contó con el apoyo del Programa de Apoyo a la Ciencia y la Tecnología de la Provincia de Sichuan (No. 2024ZYD0189). Los autores desean agradecer al Consorcio de Medicina PREcision para la Estimulación magnética transcraneal guiada por imágenes (PRECISE) por su orientación profesional.
Materiales
| Name | Company | Catalog Number | Comments |
| Brainsight Neuronavigation system | Rogue Research Inc. | KITBSF0104 | |
| DPABI_V7.0 toolkit | DeepBrain | for RS-fMRI and task-based fMRI data analysis | |
| Magstim Rapid2 | The MAGSTIM Company Limited | 3012-00 | |
| SPM12 (7771) | Wellcome Centre for Human Neuroimaging | for RS-fMRI and task-based fMRI data analysis | |
| The Brainsight 2 channel electromyography acquisition device | Rogue Research Inc. | NTBX001001 |
Referencias
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoExplorar más artículos
This article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados