Method Article
Esplenectomía laparoscópica con desvascularización pericárdica por hiperesplenismo y hemorragia esofágica por várices esofágicas por hipertensión portal
* Estos autores han contribuido por igual
En este artículo
Resumen
Con el rápido avance de las técnicas laparoscópicas, los beneficios mínimamente invasivos de la esplenectomía laparoscópica combinada con la desvascularización pericárdica se han vuelto cada vez más evidentes. En este contexto, presentamos un protocolo para la realización de la esplenectomía laparoscópica junto con la desvascularización pericárdica para tratar el hiperesplenismo y la hemorragia esofágica por várices derivada de la hipertensión portal.
Resumen
El hiperesplenismo y la hemorragia esofágica por várices causadas por la hipertensión portal son complicaciones frecuentes y graves de la cirrosis descompensada. En los últimos años, con la aplicación generalizada de diversos métodos terapéuticos como los fármacos, la endoscopia, la embolización de la arteria esplénica, la derivación portal intrahepática transyugular y el trasplante hepático, el papel de la cirugía en el tratamiento de la hipertensión portal ha disminuido gradualmente y las indicaciones para el tratamiento quirúrgico se han definido de manera más estricta. Sin embargo, de acuerdo con la práctica clínica en China, el tratamiento quirúrgico de la hipertensión portal todavía tiene un papel importante que otros tratamientos no pueden reemplazar por completo. De hecho, el tratamiento quirúrgico de la hipertensión portal se realiza ampliamente en hospitales de todos los niveles en China, salvando numerosas vidas. La esplenectomía combinada con la desvascularización pericárdica (DPS) es el método quirúrgico más común para tratar el hiperesplenismo y la hemorragia esofágica por várices causada por la hipertensión portal. La práctica clínica a largo plazo ha demostrado que el SPD es un tratamiento seguro y eficaz para el hiperesplenismo y la rotura y hemorragia esofágica de las várices debidas a la hipertensión portal. Con el rápido desarrollo de las técnicas laparoscópicas, las ventajas mínimamente invasivas de la esplenectomía laparoscópica combinada con la desvascularización pericárdica (LSPD) se han vuelto cada vez más evidentes. Sin embargo, el desempeño exitoso de LSPD depende principalmente de la habilidad y competencia del cirujano. En este contexto, este artículo presenta técnicas detalladas para LSPD.
Introducción
China tiene un alto número de casos de hepatitis, y los pacientes con hepatitis a menudo desarrollan cirrosis1. La hipertensión portal es una complicación frecuente de la cirrosis hepática 2,3. Las manifestaciones clínicas comunes incluyen esplenomegalia, hiperesplenismo, derrame peritoneal, circulación colateral portal-sistémica y gastroenteropatía hipertensiva portal 3,4,5. La rotura y hemorragia de las várices esofágicas y gástricas es la complicación más crítica y la principal causa de muerte en la cirrosis descompensada 6,7,8.
En los últimos años, con el uso generalizado de diversos métodos terapéuticos como los fármacos, la endoscopia, la embolización de la arteria esplénica, la derivación portal intrahepática transyugular y el trasplante hepático, el papel de la cirugía en el tratamiento de la hipertensión portal ha disminuido gradualmente y las indicaciones para el tratamiento quirúrgico se han limitado más estrictamente 6,9,10,11,12,13 . Sin embargo, el uso prolongado del tratamiento quirúrgico para la hipertensión portal, en particular la esplenectomía combinada con la desvascularización pericárdica (DPS), ha salvado numerosas vidas y sigue desempeñando un papel indispensable en China14,15. La práctica quirúrgica a largo plazo ha demostrado que la DPS es segura y eficaz, con una baja incidencia de resangrado y encefalopatía hepática 6,9,14,15,16.
Con la popularización de la cirugía mínimamente invasiva y los avances en las técnicas laparoscópicas, la esplenectomía laparoscópica combinada con la desvascularización pericárdica (DSPPD) ya se ha aplicado en la práctica clínica 17,18,19,20,21. Sin embargo, el LSPD impone mayores exigencias a la competencia técnica del cirujano. Teniendo en cuenta esto, el presente artículo proporciona técnicas detalladas para la LSPD en el tratamiento del hiperesplenismo y la hemorragia esofágica por várices causadas por la hipertensión portal.
Protocolo
Se incluyeron en este estudio un total de 8 pacientes que se sometieron a LSPD entre octubre de 2012 y septiembre de 2022. Las operaciones fueron aprobadas por la junta de revisión institucional del Primer Hospital Afiliado de la Universidad de Jinan. Todos los pacientes dieron su consentimiento informado por escrito. Los consumibles y equipos necesarios para el estudio se enumeran en la Tabla de Materiales.
1. Criterios de inclusión
- Incluir pacientes con esplenomegalia (el bazo mide más de 12 cm en cualquier diámetro) e hiperesplenismo (recuento de plaquetas menor de 75 × 109/L) causados por hipertensión portal.
- Incluir pacientes con antecedentes de hemorragia digestiva alta y mala respuesta al tratamiento conservador.
- Incluir pacientes con función hepática de Child-Pugh grado A o B6.
2. Criterios de exclusión
- Excluir pacientes con función hepática de grado C6 de Child-Pugh, o con encefalopatía hepática, ictericia grave, disfunción grave de la coagulación y ascitis masiva.
- Excluir a los pacientes con trombo extenso de la vena porta principal, la vena esplénica y la vena mesentérica superior.
- Excluir a los pacientes con disfunción cardíaca, pulmonar, renal y otros órganos vitales.
- Excluir a los pacientes que no pudieron tolerar la anestesia general o el neumoperitoneo.
3. Preparación preoperatoria
- Realizar análisis de sangre preoperatorios, incluyendo pruebas de función hepática y renal, un hemograma completo, una prueba de función de coagulación, grupos sanguíneos y pruebas cruzadas.
- Realizar electrocardiograma, radiografía de tórax, ecografía Doppler color cardiovascular y hepatobiliar y tomografía computarizada (TC) de la parte superior del abdomen antes de la cirugía.
4. Técnica quirúrgica
- Posición del paciente y de los cirujanos
- Después de la intubación traqueal y la anestesia general (realizada de acuerdo con los protocolos aprobados institucionalmente), coloque al paciente en decúbito supino con las piernas abiertas de 45° a 60°. Realice la desinfección de rutina con una solución de povidona yodada.
- Asegúrese de que el cirujano esté colocado en el lado derecho del paciente, el asistente esté en el lado izquierdo y el soporte del endoscopio esté colocado entre las piernas del paciente. La posición de los cirujanos se puede ajustar de acuerdo con los hábitos personales.
- Establecimiento del neumoperitoneo y disposición del trócar
- Realizar una incisión longitudinal de 10 mm por debajo del ombligo, inyectar gas de dióxido de carbono a través de una aguja de neumoperitoneo y mantener una presión abdominal de 12 mmHg (Figura 1).
- Inserte un trócar de 10 mm y el laparoscopio por debajo del ombligo. Bajo la visualización directa proporcionada por el laparoscopio, coloque un trocar de 12 mm en el abdomen medio izquierdo y derecho, respectivamente. Posteriormente, coloque un trócar de 5 mm en la parte superior izquierda y derecha del abdomen, respectivamente (Figura 1).
- Ligadura de la arteria esplénica
- Incidir los ligamentos gastrocólico y gastrosplénico con un bisturí ultrasónico-armónico (Figura 2A,B). Ligar, cortar los vasos gastroepiploicos izquierdos y gástricos cortos para exponer el saco omental menor y el páncreas (Figura 2C).
- Incisión en el peritoneo posterior en el margen superior del páncreas. Diseccionar y ligar la arteria esplénica (Figura 2D).
NOTA: Después de la ligadura de la arteria esplénica, el color de la superficie del bazo se convierte en un cambio isquémico, lo cual es útil para reducir el sangrado durante la esplenectomía.
- Esplenectomía
- Comenzando desde el polo inferior del bazo, corte el ligamento esplenocólico (Figura 3A). Levantar ventralmente el polo inferior del bazo y cortar el ligamento esplenorenal (Figura 3B).
- Cerca del pedículo esplénico, separe la cola del páncreas del pedículo esplénico. Cerca del polo superior del bazo, corte el ligamento esplenofrénico (Figura 3C).
NOTA: En este punto, el bazo está completamente libre. - Cortar el pedículo esplénico con un dispositivo de grapado lineal con un cartucho (altura 2,6 mm, longitud 60 mm) (Figura 3D).
NOTA: Al cortar el pedículo esplénico, preste atención para evitar daños en la cola pancreática y prevenir la fuga pancreática después de la cirugía.
- Desvascularización pericárdica
NOTA: La desvascularización de los vasos gastroepiploicos izquierdos y gástricos cortos se ha realizado en los pasos anteriores (Figura 2A,B).- Levanta y tira del estómago hacia el lado cefálico. Diseccionar y exponer los vasos gástricos izquierdos en la parte posterior del estómago. Libar y cortar los vasos gástricos izquierdos (Figura 4A).
- Disociar la pared posterior del estómago hacia el cardias. Libar y cortar los vasos gástricos posteriores (Figura 4B).
- Tira del estómago hacia la parte inferior izquierda. Incisión en el epiplón menor y la serosa anterior del cardias.
- Diseccionar y exponer las ramas de la vena coronaria gástrica que ingresan a la pared gástrica. Libar y cortar las ramas gástricas de la vena coronaria (Figura 4C).
- Incisión en la serosa esofágica anterior subfrénica. Diseccionar y disociar la parte inferior del esófago con una longitud no inferior a 6 cm. Libar y cortar los vasos frénicos inferiores y las ramas esofágicas de la vena coronaria (Figura 4D,E).
NOTA: Preste atención a la posible presencia de ramas esofágicas anormalmente superiores de la vena coronaria; si está presente, se requiere ligadura e incisión (Figura 4F).
- Extracción de muestras y finalización de la cirugía
- Revise cuidadosamente si quedan vasos varicosos alrededor del cardias (Figura 5A). Cargue el bazo resecado en una bolsa de muestras (Figura 5B).
- Enjuague el campo quirúrgico con solución salina estéril (Figura 5C). Examine cuidadosamente si hay sangrado activo, lesiones colaterales pancreáticas y gastrointestinales. Coloque un tubo de drenaje debajo del diafragma izquierdo (Figura 5D).
- Retire los trócares y extienda la incisión umbilical hasta aproximadamente 3 cm de longitud. Triture el bazo dentro de la bolsa de muestras y retírela. Complete la cirugía suturando las incisiones de la pared abdominal.
5. Procedimientos postoperatorios
- Controle continuamente la frecuencia cardíaca, la presión arterial, la frecuencia respiratoria y la temperatura.
- Administrar antibióticos intravenosos, somatostatina y medicamentos hepatoprotectores después de la cirugía.
- Revise regularmente el sitio de la incisión en busca de signos de infección, como enrojecimiento, hinchazón o secreción.
- Si no se produce una fuga pancreática, retire el tubo de drenaje abdominal en 5-7 días después de la cirugía.
- Revise el recuento de plaquetas con regularidad. La anticoagulación o el tratamiento antiplaquetario se prescriben si el recuento de plaquetas es demasiado alto o si hay trombosis venosa.
Resultados
Se incluyeron 8 pacientes (edad media: 50,75 años ± 6,43 años), de los cuales 6 eran hombres (75,0%) y 2 mujeres (25,0%). La causa de la hipertensión portal en los ocho pacientes con cirrosis fue la hepatitis viral. Hubo 5 pacientes (62,5%) con función hepática clasificada como grado A de Child-Pugh y 3 pacientes (37,5%) con grado B de Child-Pugh. El eje mayor medio del bazo para los pacientes fue de 196,50 mm ± 12,39 mm. Los recuentos medios de glóbulos blancos, hemoglobina y plaquetas fueron (3,33 ± 0,81) × 109/L, 79,38 ± 10,85 g/L y (48,13 ± 10,37) ×10 9/L, respectivamente (Tabla 1).
Todos los pacientes se sometieron con éxito a la LSPD sin conversión a cirugía abierta. El tiempo medio quirúrgico fue de 215,63 min ± 50,19 min, con una pérdida sanguínea intraoperatoria media de 128,75 mL ± 44,22 mL. El tiempo medio de drenaje postoperatorio fue de 5,50 ± 0,76 días, y la estancia hospitalaria postoperatoria media fue de 6,50 ± 0,76 días. La tasa de complicaciones postoperatorias fue del 25,0%, incluyendo 1 caso de infección pulmonar y 1 caso de ascitis (Tabla 2).
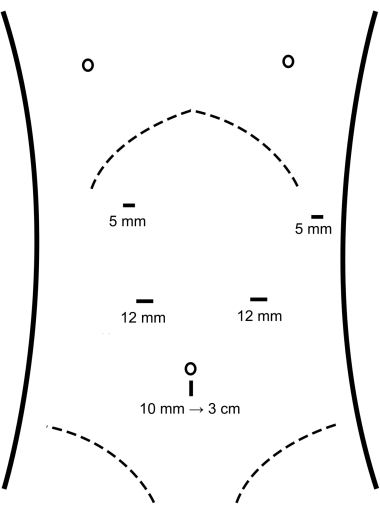
Figura 1: La disposición del trocar. Haga clic aquí para ver una versión más grande de esta figura.
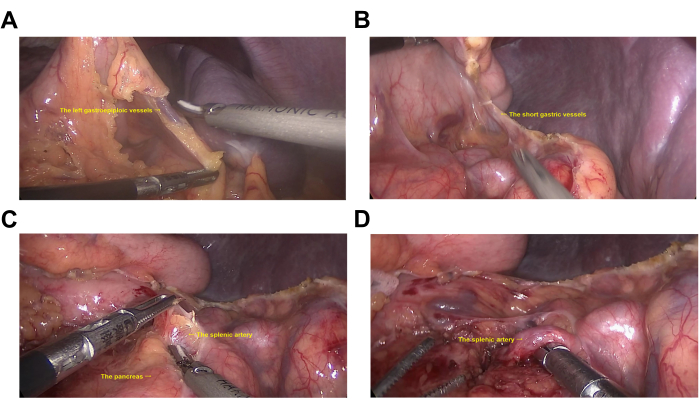
Figura 2: Ligadura de la arteria esplénica. (A) Los vasos gastroepiploicos izquierdos. (B) Los vasos gástricos cortos. (C) El páncreas y la arteria esplénica. (D) La arteria esplénica. Haga clic aquí para ver una versión más grande de esta figura.

Figura 3: Esplenectomía. (A) El ligamento esplenocólico. (B) El ligamento esplenorenal. (C) El ligamento esplenofrénico. (D) El pedículo esplénico. Haga clic aquí para ver una versión más grande de esta figura.

Figura 4: Desvascularización pericárdica. (A) Los vasos gástricos izquierdos. (B) Los vasos gástricos posteriores. (C) La rama gástrica de la vena coronaria. (D) Los vasos frénicos inferiores. (E) rama esofágica de la vena coronaria. (F) La rama esofágica de la vena coronaria. Haga clic aquí para ver una versión más grande de esta figura.
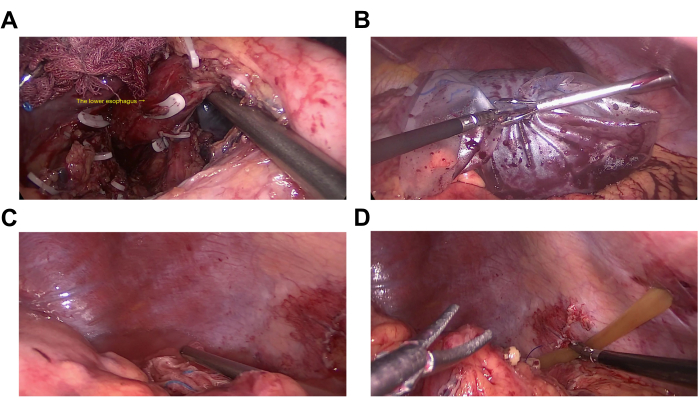
Figura 5: Extracción de la muestra y finalización de la cirugía. (A) Examen cuidadoso de los vasos varicosos restantes alrededor del cardias. (B) El bazo resecado se carga en una bolsa de muestras. (C) El campo quirúrgico se enjuaga con solución salina estéril. (D) Se coloca un tubo de drenaje debajo del diafragma izquierdo. Haga clic aquí para ver una versión más grande de esta figura.
| Sexo (n) | |
| Masculino | 6 (75.0%) |
| Hembra | 2 (25.0%) |
| Edad (años) | 50,75 ± 6,43 |
| Etiología (s/f) | |
| Hepatitis virales | 8 (100.0%) |
| Enfermedad hepática alcohólica | 0 (0.0%) |
| Enfermedad del hígado graso no alcohólico | 0 (0.0%) |
| Colestasis | 0 (0.0%) |
| Droga o toxina | 0 (0.0%) |
| Grado Child-Pugh (n) | |
| Un | 5 (62.5%) |
| B | 3 (37.5%) |
| Eje mayor del bazo (mm) | 196,50 ± 12,39 |
| Glóbulos blancos (× 109/L) | 3,33 ± 0,81 |
| HGB (g/L) | 79,38 ± 10,85 |
| PLT (× 109/L) | 48,13 ± 10,37 |
Tabla 1: Características clínicas de los pacientes. leucocitos = glóbulos blancos; HGB = hemoglobina; PLT = plaquetas.
| Tiempo de operación (minutos) | 215,63 ± 50,19 |
| Pérdida de sangre intraoperatoria (mL) | 128,75 ± 44,22 |
| Tiempo de drenaje postoperatorio (días) | 5,50 ± 0,76 |
| Estancia hospitalaria postoperatoria (días) | 6,50 ± 0,76 |
| Complicaciones postoperatorias (n) | 2 (25.0%) |
| Infección de la incisión | 0 (0.0%) |
| Infección pulmonar | 1 (12.5%) |
| Infección abdominal | 0 (0.0%) |
| Sangrado postoperatorio | 0 (0.0%) |
| Ascitis | 1 (12.5%) |
| Fuga pancreática | 0 (0.0%) |
| Trombosis portal | 0 (0.0%) |
Tabla 2: Evolución quirúrgica de los pacientes.
Discusión
Una gran proporción de personas en China sufren de hepatitis crónica, que es un factor importante que conduce a la cirrosis hepática 1,2. Los pacientes con cirrosis hepática avanzada a menudo experimentan hipertensión portal, lo que resulta en una serie de complicaciones, como esplenomegalia, hiperesplenismo, derrame peritoneal, circulación colateral portal-sistémica y gastroenteropatía hipertensiva portal 3,4,5. Entre estas, la rotura y hemorragia de las várices esofágicas y gástricas es la complicación más crítica y la principal causa de muerte en la cirrosis descompensada 6,7,8. De acuerdo con reportes de literatura previa, la tasa de mortalidad para el primer episodio hemorrágico es de alrededor del 20%12,22. Además, la tasa de resangrado de várices es de casi el 60%, con una tasa de mortalidad del 30%23.
En los últimos años, diversos métodos terapéuticos como los fármacos, la endoscopia, la embolización de la arteria esplénica, la derivación portal intrahepática transyugular y el trasplante hepático han sido cada vez más utilizados en el tratamiento de la hipertensión portal 6,9,10,11,12,13. Debido al desarrollo desequilibrado de las instituciones médicas a todos los niveles en China, la esplenectomía combinada con la desvascularización pericárdica (DPS) todavía desempeña un papel indispensable en el tratamiento del hiperesplenismo y la hemorragia esofágica por várices causada por la hipertensión portal14,15. Hassab propuso por primera vez el SPD para el tratamiento de la hipertensión portal en 196624. La SPD alivia la destrucción excesiva de las células sanguíneas mediante la eliminación del bazo hiperfuncional y corrige manifestaciones clínicas como trombocitopenia, anemia y granulocitopenia. Mientras tanto, el SPD puede controlar el sangrado al bloquear el flujo sanguíneo anormal entre la vena porta y la vena ácigos. Después de más de medio siglo de práctica clínica, la DPS ha demostrado tener ventajas como alta seguridad, efecto hemostático definitivo, bajo riesgo de resangrado y baja incidencia de encefalopatía hepática 6,9,14,15,16.
La cirugía abierta tradicional implica un trauma más grande, una mayor pérdida de sangre intraoperatoria, tiempos de recuperación postoperatorios más largos y una mayor probabilidad de complicaciones como la ascitis y la trombosis de la vena porta, que ya no satisfacen la demanda de procedimientos mínimamente invasivos y de recuperación rápida. La primera esplenectomía laparoscópica fue reportada en 1991 por Delaitre et al.25. Sin embargo, solo existen un número limitado de estudios sobre la esplenectomía laparoscópica combinada con la desvascularización pericárdica (DSPPD) para el tratamiento de la hipertensión portal 17,18,19,20,21. La LSPD impone mayores exigencias a la competencia técnica del cirujano, lo que presenta ciertas limitaciones para el desarrollo de esta técnica. A la luz de esta situación, el presente artículo proporciona técnicas detalladas para la LSPD en el tratamiento del hiperesplenismo y la hemorragia esofágica por várices causadas por la hipertensión portal.
En los casos presentes, se incluyeron pacientes con esplenomegalia e hiperesplenismo por hipertensión portal. Todos los pacientes tenían antecedentes de hemorragia digestiva alta y una mala respuesta al tratamiento conservador. La cirugía preventiva sigue siendo controvertida; Por lo general, no se recomienda para pacientes sin antecedentes de hemorragia gastrointestinal. Las controversias pertinentes deben resolverse mediante nuevos estudios prospectivos que aporten más pruebas.
Existen varios enfoques quirúrgicos para la esplenectomía; Recomendamos la ligadura de la arteria esplénica como prioridad. La posición de la arteria esplénica es relativamente fija, lo que facilita la disección y ligadura de la arteria en el margen superior del páncreas sin una separación excesiva del tejido que podría provocar sangrado. Después de ligar la arteria esplénica principal, el bazo se encoge, aumentando el espacio operativo, lo que facilita la elevación del bazo. Además, priorizar el tratamiento de la arteria esplénica principal puede ayudar a evitar la rotura y hemorragia de la vena varicosa que puede afectar el campo quirúrgico durante la disección de los vasos pediculares esplénicos secundarios, reduciendo significativamente la incidencia de conversión y garantizando la seguridad de la cirugía.
Se debe tener cuidado de proteger la cola del páncreas, ubicada cerca del pedículo esplénico, al diseccionar los ligamentos periesplénicos para evitar lesiones pancreáticas y reducir el riesgo de complicaciones postoperatorias por fuga pancreática.
Cuando se trata de vasos sanguíneos de várices, deben separarse cerca de la pared del estómago y evitar tirones bruscos que podrían provocar desgarros y sangrado de las venas varicosas. Si se produce una hemorragia masiva durante la operación, se puede considerar la transfusión de sangre autóloga si las condiciones lo permiten. Para el esófago inferior, es importante asegurar una longitud de disociación de al menos 6 cm para exponer y ligar cualquier rama anormal del esófago superior de la vena coronaria. El recuento de plaquetas debe controlarse regularmente después de la cirugía, y los fármacos antiplaquetarios deben administrarse con criterio en función de la situación específica.
Este estudio presenta técnicas detalladas para la esplenectomía laparoscópica combinada con la desvascularización pericárdica (DSSPD) para el hiperesplenismo y la hemorragia esofágica por várices causada por hipertensión portal. Sobre la base de nuestra experiencia, la LSPD puede considerarse preliminarmente factible y segura para el tratamiento de la hipertensión portal. Sin embargo, debido al pequeño número de casos en este estudio, se necesita más investigación clínica para confirmar estos hallazgos. Una vez que más estudios clínicos validen su seguridad y eficacia, se espera que el LSPD se utilice más ampliamente en el futuro. Se recomienda que la LSPD sea realizada selectivamente por cirujanos experimentados.
Divulgaciones
Los autores no tienen nada que revelar.
Agradecimientos
Este trabajo fue apoyado por subvenciones del Proyecto de Planificación de Ciencia y Tecnología de Guangzhou (No. 2023A04J1917) y el Fondo Médico Conjunto de la Universidad de Jinan (No. YXZY2024018).
Materiales
| Name | Company | Catalog Number | Comments |
| 10-mm trocar | Xiamen Surgaid Medical Device Co., LTD | NGCS 100-1-10 | Sterile, ethylene oxide sterilized, disposable |
| 12-mm trocar | Xiamen Surgaid Medical Device Co., LTD | NGCS 100-1-12 | Sterile, ethylene oxide sterilized, disposable |
| 5-mm trocar | Xiamen Surgaid Medical Device Co., LTD | NGCS 100-1-5 | Sterile, ethylene oxide sterilized, disposable |
| Hem-o-lok | America Teleflex Medical Technology Co., LTD | 544240 | Sterile, ethylene oxide sterilized, disposable |
| Linear stapling device | America Ethicon Medical Technology Co., LTD | PSEE60A | Sterile, ethylene oxide sterilized, disposable |
| Pneumoperitoneum needle | Xiamen Surgaid Medical Device Co., LTD | NGCS 100-1 | Sterile, ethylene oxide sterilized, disposable |
| Suction and irrigation tube | Tonglu Hengfeng Medical Device Co., LTD | HF6518.035 | Sterile,dry heat sterilized, reusable |
| Ultrasounic-harmonic scalpel | Chongqing Maikewei Medical Technology Co., LTD | QUHS36S | Sterile, ethylene oxide sterilized, disposable |
Referencias
- Sun, N., He, F., Sun, J., Zhu, G. Viral hepatitis in China during 2002-2021: Epidemiology and influence factors through a country-level modeling study. BMC Public Health. 24 (1), 1820 (2024).
- Jeng, W. J., Papatheodoridis, G. V., Lok, A. S. F. Hepatitis B. Lancet. 401 (10381), 1039-1052 (2023).
- Iwakiri, Y., Trebicka, J. Portal hypertension in cirrhosis: Pathophysiological mechanisms and therapy. JHEP Rep. 3 (4), 100316 (2021).
- Gracia-Sancho, J., Marrone, G., Fernández-Iglesias, A. Hepatic microcirculation and mechanisms of portal hypertension. Nat Rev Gastroenterol Hepatol. 16 (4), 221-234 (2019).
- Simonetto, D. A., Liu, M., Kamath, P. S. Portal hypertension and related complications: Diagnosis and management. Mayo Clin Proc. 94 (4), 714-726 (2019).
- Lesmana, C. R. A., Raharjo, M., Gani, R. A. Managing liver cirrhotic complications: Overview of esophageal and gastric varices. Clin Mol Hepatol. 26 (4), 444-460 (2020).
- Mokdad, A. A., et al. Liver cirrhosis mortality in 187 countries between 1980 and 2010: A systematic analysis. BMC Med. 12, 145 (2014).
- Sepanlou, S. G., et al. The global, regional, and national burden of cirrhosis by cause in 195 countries and territories, 1990-2017: A systematic analysis for the Global Burden of Disease Study 2017. Lancet Gastroenterol Hepatol. 5 (3), 245-266 (2020).
- Magyar, C. T. J., et al. Surgical considerations in portal hypertension. Clin Liver Dis. 28 (3), 555-576 (2024).
- Zheng, S., et al. Liver cirrhosis: Current status and treatment options using Western or traditional Chinese medicine. Front Pharmacol. 15, 1381476 (2024).
- Garcia-Tsao, G., Abraldes, J. G., Berzigotti, A., Bosch, J. Portal hypertensive bleeding in cirrhosis: Risk stratification, diagnosis, and management: 2016 practice guidance by the American Association for the study of liver diseases. Hepatology. 65 (1), 310-335 (2017).
- de Franchis, R., Baveno VI, F. Expanding consensus in portal hypertension: Report of the Baveno VI Consensus Workshop: Stratifying risk and individualizing care for portal hypertension. J Hepatol. 63 (3), 743-752 (2015).
- Tripathi, D., et al. U.K. guidelines on the management of variceal haemorrhage in cirrhotic patients. Gut. 64 (11), 1680-1704 (2015).
- Yang, L. Progress and prospect of surgical treatment for portal hypertension. Chin J Pract Surg. 40 (2), 180-184 (2020).
- Zhang, C., Liu, Z. Surgical treatment of cirrhotic portal hypertension: Current status and research advances. J Clin Hepatol. 36 (2), 417-420 (2020).
- Qi, W. L., et al. Prognosis after splenectomy plus pericardial devascularization vs. transjugular intrahepatic portosystemic shunt for esophagogastric variceal bleeding. World J Gastrointest Surg. 15 (8), 1641-1651 (2023).
- Yan, C., Qiang, Z., Jin, S., Yu, H. Spleen bed laparoscopic splenectomy plus pericardial devascularization for elderly patients with portal hypertension. Wideochir Inne Tech Maloinwazyjne. 17 (2), 338-343 (2022).
- Chen, H., et al. Comparison of efficacy of laparoscopic and open splenectomy combined with selective and nonselective pericardial devascularization in portal hypertension patients. Surg Laparosc Endosc Percutan Tech. 28 (6), 401-403 (2018).
- Hong, D., et al. Comparison of two laparoscopic splenectomy plus pericardial devascularization techniques for management of portal hypertension and hypersplenism. Surg Endosc. 29 (12), 3819-3826 (2015).
- Cai, Y., Liu, Z., Liu, X. Laparoscopic versus open splenectomy for portal hypertension: a systematic review of comparative studies. Surg Innov. 21 (4), 442-447 (2014).
- Huang, J., Xu, D. W., Li, A. Can laparoscopic splenectomy and azygoportal disconnection be safely performed in patients presenting with cirrhosis, hypersplenism and gastroesophageal variceal bleeding? How to do it, tips and tricks (with videos). Curr Probl Surg. 61 (7), 101501 (2024).
- Magaz, M., Baiges, A., Hernández-Gea, V. Precision medicine in variceal bleeding: Are we there yet. J Hepatol. 72 (4), 774-784 (2020).
- Bosch, J., García-Pagán, J. C. Prevention of variceal rebleeding. Lancet. 361 (9361), 952-954 (2003).
- Terrosu, G., et al. Laparoscopic versus open splenectomy in the management of splenomegaly: our preliminary experience. Surgery. 124 (5), 839-843 (1998).
- Delaitre, B., Maignien, B. Splenectomy by the laparoscopic approach. Report of a case. Presse Med. 20 (44), 2263 (1991).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoExplorar más artículos
This article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados